Evidências Atuais, Limitações Diagnósticas e Estratégias para Casos Refratários
Dr. Arnaldo Schizzi Cambiaghi
Especialista em Ginecologia e Reprodução Humana – IPGO
Atualizado em 26/01/26
Índice
ToggleA endometrite crônica (EC) é uma condição inflamatória persistente do endométrio funcional caracterizada pela infiltração de plasmócitos CD138+, geralmente assintomática e frequentemente subdiagnosticada. Nas últimas décadas, passou a ser considerada uma possível causa de falhas reprodutivas como falha de implantação recorrente (RIF) e perda gestacional recorrente (RPL). No entanto, sua relevância clínica ainda é debatida, especialmente pela falta de padronização nos critérios diagnósticos e terapêuticos.
Este artigo analisa criticamente as evidências atuais, com base nos dados apresentados no 11º Congresso IVIRMA 2025 (Barcelona), com foco na apresentação do Dr. Andres Reig e nos achados de HogenEsch et. al. (2023).
Prevalência e Populações de Risco
Devido à ausência de critérios unificados (ex.: número de plasmócitos CD138+ por campo), é difícil determinar com precisão a prevalência real da EC.
HogenEsch et. al. (2023) relataram maior prevalência em mulheres com RPL e perdas gestacionais precoces.
Entretanto, a meta-análise não evidenciou melhora nas taxas de gravidez após tratamento da EC em pacientes com RIF.
Esses dados sugerem que a EC pode ter impacto clínico em subgrupos específicos, mas não de forma generalizável.
Diagnóstico: Limitações e Controvérsias
O diagnóstico de EC pode ser feito por:
- Biópsia endometrial com CD138+ (imuno-histoquímica);
- Cultura endometrial (baixa sensibilidade);
- PCR do microbioma (uso restrito a centros especializados).
Ainda não há consenso sobre o ponto de corte para diagnóstico (quantidade de plasmócitos), o que prejudica a indicação clara do tratamento.
Tratamento Convencional e Eficácia Variável
A abordagem padrão envolve antibióticos, com resultados heterogêneos. Segundo o IVIRMA 2025:
- A eficácia varia de 20% a 92%;
- Não há estudos sobre a segurança de múltiplos ciclos;
- Doxiciclina, metronidazol e ciprofloxacino são os regimes mais comuns.
Estudos observacionais sugerem possível benefício reprodutivo, mas sem confirmação por ensaios clínicos randomizados.
Exemplos:
- Cicinelli et. al. (2015): melhora na taxa de implantação com antibióticos (sem randomização);
- Bouet et. al. (2016): benefício em RPL, mas com amostra reduzida.
Casos Refratários: Alternativas Terapêuticas
Quando a EC persiste após 1 ou 2 ciclos antibióticos, outras estratégias devem ser consideradas:
1.1. Antibióticos de Segunda Linha
- Esquemas combinados (ex.: doxiciclina + metronidazol, ou dirigidos por cultura/PCR);
- Tratamento prolongado (14–21 dias).
1.2. Terapia com Probióticos
- Reposição de Lactobacillus crispatus por via vaginal ou oral;
- Correlação com maior taxa de implantação quando há dominância de lactobacilos.
1.3. Ressecção Mecânica do Endométrio
- Indicada em inflamações focais refratárias;
- Realizada por histeroscopia, com remoção superficial da mucosa inflamada;
- Útil quando há micropólipos persistentes, zonas hiperemiadas ou falha terapêutica com antibióticos.
1.4. Imunomodulação Experimental
- Corticoides, IVIG, tacrolimus ou terapia com células NK (uso empírico);
- Sem evidência robusta para indicação de rotina.
Controvérsia: Tratar ou não tratar a endometrite
Endometrite crônica: causa, cofator ou marcador?
A endometrite crônica ocupa hoje um lugar singular dentro da medicina reprodutiva: é, ao mesmo tempo, uma das condições mais investigadas dos últimos anos e uma das mais heterogêneas em resultados, definições e implicações clínicas.
De um lado, uma parte consistente da literatura associa a endometrite crônica a infertilidade, abortamento de repetição e, em alguns estudos, à falha de implantação. Trabalhos observacionais mostram maior prevalência de plasmócitos endometriais em mulheres com perdas gestacionais, menor taxa de implantação e piores desfechos reprodutivos. Em determinados subgrupos, especialmente quando há critérios histológicos mais rigorosos, inflamação persistente e confirmação de resolução após tratamento, observa-se melhora de taxas de gravidez e de nascido vivo. Esses dados sustentam a visão de que a endometrite pode, em contextos específicos, comprometer a receptividade endometrial, a tolerância imunológica e a comunicação embrião-endométrio.
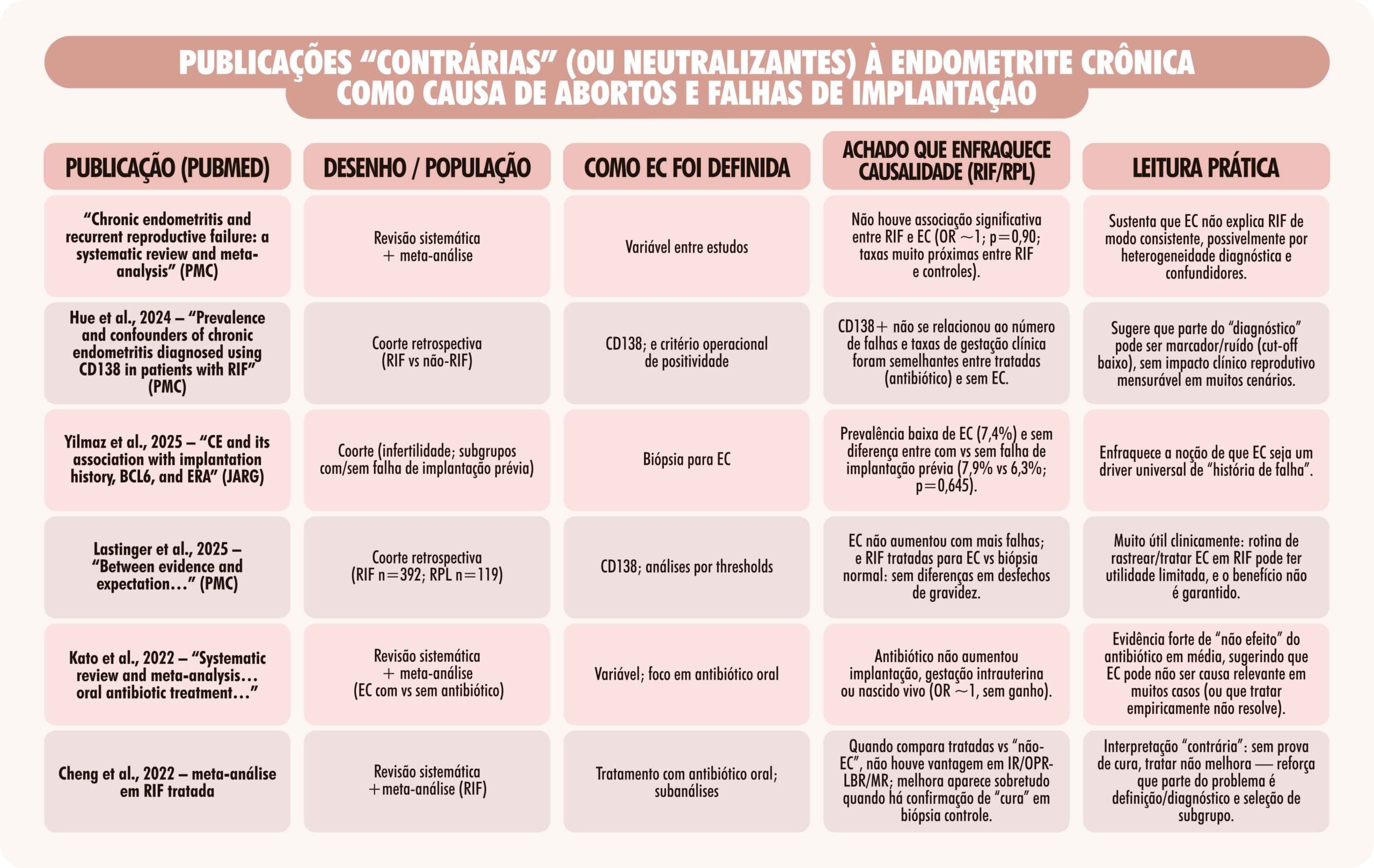
Por outro lado, cresce também o número de publicações que não confirmam essa relação de forma consistente, sobretudo nos quadros de falha de implantação recorrente. Meta-análises e grandes coortes mostram prevalências semelhantes de endometrite em mulheres com e sem falha de implantação, ausência de correlação entre número de falhas e presença de plasmócitos, e, em vários estudos, ausência de impacto significativo do tratamento antibiótico sobre taxas de implantação, gravidez clínica ou nascido vivo. Esses trabalhos questionam o papel causal direto da endometrite e sugerem que, em muitos cenários, ela pode representar apenas um achado concomitante, um marcador de alterações endometriais inespecíficas ou de outros processos subjacentes — como adenomiose, endometriose, disbiose, distúrbios imunológicos, alterações vasculares ou fatores embrionários.
Grande parte dessa controvérsia decorre de um problema central: a ausência de padronização diagnóstica. Os estudos utilizam diferentes métodos de biópsia, diferentes momentos do ciclo, distintos anticorpos e, principalmente, diferentes pontos de corte para definir positividade ao CD138. O que alguns classificam como endometrite, outros consideram um achado inflamatório mínimo sem significado clínico. Essa variabilidade transforma profundamente os resultados, inflaciona prevalências e dificulta a comparação entre trabalhos. Além disso, a maioria dos estudos é retrospectiva, com populações heterogêneas e múltiplos fatores de confusão.
Dessa forma, à luz da evidência atual, não é cientificamente sólido afirmar que a endometrite crônica seja, por si só, uma causa universal de falha de implantação ou de aborto. Tampouco é correto descartá-la como irrelevante. O que se impõe é uma leitura mais madura: a endometrite parece atuar, quando presente, como um possível fator modulador do ambiente endometrial, cuja importância varia conforme intensidade da inflamação, persistência do quadro, associação com outras patologias uterinas e contexto clínico da paciente.
O desafio contemporâneo deixa de ser “tratar ou não tratar a endometrite” e passa a ser identificar em quais mulheres ela é clinicamente significativa. Isso exige critérios diagnósticos mais robustos, avaliação integrada do útero, da microbiota, do perfil inflamatório e imunológico, além de estudos prospectivos bem desenhados que estratifiquem populações e utilizem desfechos reprodutivos sólidos.
Assim, a endometrite crônica não deve ser encarada nem como vilã universal da infertilidade, nem como achado irrelevante. Ela ocupa um território intermediário, ainda em construção científica, no qual a individualização da conduta, a integração com outros fatores uterinos e embrionários e a cautela frente a tratamentos empíricos indiscriminados representam, hoje, a postura mais tecnicamente responsável.
Discussão
A EC deve ser abordada com cautela. Estudos atuais sugerem que seu impacto nos desfechos reprodutivos está restrito a subgrupos, como pacientes com RPL, RIF severo e sintomatologia específica. A aplicação universal de testes ou tratamentos pode resultar em superdiagnóstico e uso desnecessário de antibióticos, com risco de disbiose e custo elevado.
A ressecção mecânica do endométrio pode representar uma alternativa terapêutica promissora, especialmente quando há sinais histeroscópicos persistentes e ausência de resposta clínica.
Conclusão
A EC é uma entidade clínica relevante em contextos específicos da infertilidade. Seu diagnóstico requer integração entre exames histológicos, moleculares e clínicos. O tratamento com antibióticos deve ser reservado a casos bem-documentados, enquanto a ressecção mecânica do endométrio e o uso de probióticos surgem como ferramentas úteis em casos refratários. Ensaios clínicos randomizados e protocolos unificados são fundamentais para orientar a prática clínica.
Perguntas e Respostas: Endometrite Crônica e Infertilidade
(Baseado nas apresentações do IVIRMA 2025 e literatura atual)
Nem sempre. Alguns estudos mostram associação, mas outros — inclusive revisões e coortes — não confirmam diferença consistente de prevalência em pacientes com falha de implantação, nem melhora clara de resultados apenas com tratar “porque deu CD138 positivo”. Hoje, entende-se que pode ser causa em subgrupos, mas não é explicação universal.
Principalmente por falta de padronização: momento da biópsia, número de amostras, técnica, interpretação e, sobretudo, o ponto de corte do CD138 (quantos plasmócitos definem endometrite). Um mesmo endométrio pode ser “positivo” em um estudo e “irrelevante” em outro, mudando completamente as conclusões.
Não obrigatoriamente. CD138 positivo pode significar desde inflamação mínima até inflamação persistente relevante. O tratamento tende a fazer mais sentido quando há quadro persistente, sintomatologia/achados uterinos associados (pólipos, sangramento, fluido, alterações histeroscópicas), história compatível (RPL, endométrio refratário) e, idealmente, quando há estratégia para confirmar resolução em casos selecionados.
A evidência é variável. Há estudos mostrando melhora quando a endometrite “cura” (biópsia de controle negativa), mas revisões também descrevem cenários em que antibiótico não aumenta implantação, gestação clínica ou nascido vivo em média. Por isso, a conduta mais robusta é individualizar: tratar quando há plausibilidade clínica e evitar “tratamento automático” em positividade mínima isolada.
A endometrite crônica (EC) é uma inflamação persistente do endométrio, o tecido que reveste internamente o útero. Mesmo sem causar sintomas aparentes, ela pode afetar negativamente a receptividade do útero, dificultando a implantação do embrião e aumentando o risco de abortos de repetição. Está especialmente relacionada a casos de falha de implantação em tratamentos de fertilização in vitro (FIV) e perdas gestacionais recorrentes.
Na maioria dos casos, a EC não apresenta sintomas claros. Quando ocorrem, podem incluir:
- Corrimento vaginal anormal;
- Dor pélvica discreta ou sensação de peso;
- Sangramento fora do período menstrual;
- Falhas reprodutivas repetidas sem causa aparente.
Existem três formas principais de diagnóstico:
- Biópsia endometrial com coloração CD138 (imuno-histoquímica): identifica células inflamatórias chamadas plasmócitos — é o método mais confiável;
- Histeroscopia diagnóstica: permite visualizar diretamente o interior do útero e identificar sinais como micropólipos, áreas avermelhadas e edema;
- Análise molecular (PCR ou microbioma endometrial): detecta desequilíbrios na flora uterina, útil em centros especializados.
Nem sempre. O tratamento é indicado especialmente em mulheres que:
- Tiveram falhas de implantação em FIV;
- Sofrem abortos repetidos;
- Apresentam alterações visíveis na histeroscopia;
- Têm inflamação comprovada por CD138 ou microbioma alterado.
Em mulheres férteis, sem sintomas e com diagnóstico incidental, o tratamento nem sempre é necessário.
O tratamento inicial geralmente inclui antibióticos orais, como:
- Doxiciclina: 100 mg, 2 vezes ao dia por 14 dias;
- Em alguns casos, associa-se com metronidazol ou amoxicilina-clavulanato.
Após o tratamento, recomenda-se uma nova biópsia ou histeroscopia para confirmar a cura.
Quando a inflamação persiste após um ou dois ciclos de antibióticos, consideram-se outras estratégias:
a) Antibióticos combinados e guiados por cultura ou PCR
- Podem ser usados antibióticos mais específicos conforme as bactérias detectadas (ex.: Gardnerella, Streptococcus, Ureaplasma).
b) Uso de probióticos vaginais
- Após o antibiótico, ajuda a restaurar a microbiota saudável do útero;
- Exemplo: Lactobacillus crispatus, 5 bilhões de UFC por dia durante 5 dias, depois 3 vezes por semana.
c) Ressecção mecânica do endométrio
- Em casos mais persistentes, é possível realizar uma histeroscopia para remover delicadamente a camada inflamada do endométrio, melhorando a receptividade.
d) Terapias imunológicas (uso experimental)
- Incluem corticoides, imunoglobulinas (IVIG) ou imunossupressores, mas só devem ser usados em casos selecionados.
É um procedimento feito por histeroscopia no qual o médico remove superficialmente áreas inflamadas ou anormais do endométrio. Indicado para:
- EC resistente a antibióticos;
- Casos com micropólipos persistentes;
- Planejamento de FIV em pacientes com falhas anteriores.
É minimamente invasivo, feito em consultório ou centro cirúrgico, e pode melhorar o ambiente uterino.
Sim, os probióticos podem ajudar principalmente após o uso de antibióticos. Eles favorecem o crescimento de bactérias benéficas (como Lactobacillus crispatus), reduzindo a chance de recidiva da inflamação e ajudando a equilibrar o ambiente uterino. Não substituem os antibióticos, mas são um complemento importante.
Infelizmente, sim. A EC pode recorrer, especialmente se:
- O foco infeccioso não foi completamente tratado;
- A flora uterina não foi restaurada;
- A paciente tem outras doenças inflamatórias (como endometriose).
Por isso, o seguimento após o tratamento é essencial, com nova avaliação endometrial antes de transferências embrionárias.
Sim, na maioria dos casos a EC tem cura com antibióticos e cuidados complementares. Quando tratada adequadamente, as chances de gravidez — seja natural ou por FIV — aumentam significativamente. Em casos refratários, estratégias como ressecção mecânica do endométrio e suporte imunológico têm mostrado bons resultados.
Resumo
A endometrite crônica (EC) tem sido associada à falha de implantação e perda gestacional recorrente, mas sua real relevância clínica permanece controversa. A ausência de critérios diagnósticos padronizados e a heterogeneidade nos estudos comprometem a definição da prevalência e dos benefícios do tratamento.
O objetivo deste artigo é revisar criticamente as evidências mais recentes sobre a importância clínica da EC, sua resposta ao tratamento antibiótico e as alternativas terapêuticas para casos refratários.
Métodos: Análise dos dados apresentados no 11º Congresso Internacional IVIRMA (2025), incluindo revisão dos estudos de HogenEsch et. al. (2023), Cicinelli et. al. e outros relevantes na literatura.
Resultados: A prevalência de EC é maior em populações de risco (RPL, RIF), mas meta-análises não confirmam benefício reprodutivo claro com o tratamento. A eficácia antibiótica é variável (20% a 92%) e há risco de disbiose. Para casos refratários, opções incluem ajustes terapêuticos, uso de probióticos, ressecção mecânica do endométrio e imunomodulação experimental.
A EC pode impactar negativamente a fertilidade em subgrupos específicos. O tratamento deve ser individualizado e guiado por critérios clínicos, microbiológicos e reprodutivos bem-definidos.
Palavras-chave: Endometrite crônica, infertilidade, falha de implantação, antibióticos, microbiota, ressecção endometrial.
Referências
- HogenEsch E, et. al. Chronic Endometritis: Does It Really Matter? Apresentado no 11th International IVIRMA Congress, Barcelona, 2025.
- Cicinelli E, et. al. Antibiotic treatment of chronic endometritis improves the pregnancy rate of infertile women with recurrent implantation failure. Fertil Steril. 2015;104(1):150–153.
- Bouet PE, et. al. Prevalence of chronic endometritis in women with recurrent miscarriage: A systematic review and meta-analysis. J Gynecol Obstet Hum Reprod. 2016;45(7):577–580.
- Kitaya K, et. al. Chronic endometritis and embryo implantation. Am J Reprod Immunol. 2019;82(2):e13182.
- Kyono K, et. al. Analysis of endometrial microbiota by 16S ribosomal RNA gene sequencing among infertile patients: A single-center pilot study. Reprod Med Biol.