Introdução
Cada vez mais casais homossexuais procuram clínicas de reprodução humana para terem filhos. Essa busca, que já não é fácil para os casais heterossexuais, é muito mais desgastante para os homoafetivos, pois, além de encarar as dificuldades comuns e já esperadas do tratamento, algumas vezes podem enfrentar preconceito. Entretanto, como essa situação tem sido cada vez mais comum, esses conflitos, que eram muito mais acentuados no passado, vêm sendo amenizados pela maior frequência desses atendimentos e com a demonstração, cada vez mais corriqueira e notória, desses relacionamentos tanto na vida real quanto na ficção (filmes, novelas, paradas etc).
Para esses casais que desejam constituir uma família, e não desejam a adoção, que têm suas peculiaridades não pertinentes a este E-BOOK, a única alternativa são os tratamentos de fertilização assistida em clínicas de reprodução humana. Para eles não existe a comemoração, a surpresa da gravidez inesperada, as tentativas assíduas para conseguir a gestação nem a frustração de um bebê que não vem.
Estes casais merecem uma atenção especial!
ESSE É UM CONTEÚDO EXTENSO PARA QUE VOCÊ TENHA TODOS OS DETALHES QUE FAZEM A DIFERENÇA!
Índice
ToggleA ética médica
Os seres humanos evoluem com o tempo e as pessoas e os princípios éticos se adaptam aos costumes da época. E, nesses casos, devem ser considerados tanto a ética social quanto a ética médica. A primeira é definida como um conjunto de valores morais e princípios que norteiam a conduta humana na sociedade. Serve para que haja um equilíbrio e bom funcionamento social, possibilitando que ninguém saia prejudicado. Neste sentido, embora não possa ser confundida com as leis, está relacionada com o sentimento de justiça social e deve agir desestimulando o preconceito. A ética médica restringe os atos médicos àquilo que o Conselho Federal de Medicina (CFM) determina ser certo ou errado e obriga os profissionais da saúde a seguirem rigorosamente as normas por eles fixadas. Estas normas ajudam a evitar alguns dos exageros e podem ser modificadas de acordo com a determinação deste conselho. Segue o link na íntegra da última resolução que poderá sofrer ajustes no futuro.
https://sistemas.cfm.org.br/normas/visualizar/resolucoes/BR/2017/2168
Abaixo, separamos os trechos da Resolução que têm maior importância para casais homoafetivos.
Resolução CFM N. 2.168, de 21 de setembro de 2017
Adota as normas éticas para a utilização das técnicas de reprodução assistida – sempre em defesa do aperfeiçoamento das práticas e da observância aos princípios éticos e bioéticos que ajudam a trazer maior segurança e eficácia a tratamentos e procedimentos médicos -, tornando-se o dispositivo deontológico a ser seguido pelos médicos brasileiros e revogando a Resolução CFM nº 2.121, publicada no D.O.U. de 24 de setembro de 2015, Seção I, p. 117.
O CONSELHO FEDERAL DE MEDICINA, no uso das atribuições conferidas pela Lei nº 3.268, de 30 de setembro de 1957, alterada pela Lei nº 11.000, de 15 de dezembro A ética médica de 2004, regulamentada pelo Decreto nº 44.045, de 19 de julho de 1958, e pelo Decreto nº 6.821, de 14 de abril de 2009, e associada à Lei nº 12.842, de 10 de julho de 2013, e ao Decreto nº 8.516, de 10 de setembro de 2015, CONSIDERANDO a infertilidade humana como um problema de saúde, com implicações médicas e psicológicas, e a legitimidade do anseio de superá-la;
Pacientes das técnicas de RA
- Todas as pessoas capazes, que tenham solicitado o procedimento e cuja indicação não se afaste dos limites desta resolução, podem ser receptoras das técnicas de RA, desde que os participantes estejam de inteiro acordo e devidamente esclarecidos, conforme legislação vigente.
- É permitido o uso das técnicas de RA para relacionamentos homoafetivos e pessoas solteiras, respeitado o direito a objeção de consciência por parte do médico.
- É permitida a gestação compartilhada em união homoafetiva feminina em que não exista infertilidade. Considera-se gestação compartilhada a situação em que o embrião obtido a partir da fecundação do(s) oócito(s) de uma mulher é transferido para o útero de sua parceira.
Doação de gametas ou embriões
- A doação não poderá ter caráter lucrativo ou comercial.
- Os doadores não devem conhecer a identidade dos receptores e vice-versa.
- A idade limite para a doação de gametas é de 35 anos para a mulher e de 50 anos para o homem.
- Será mantido, obrigatoriamente, sigilo sobre a identidade dos doadores de gametas e embriões, bem como dos receptores. Em situações especiais, informações sobre os doadores, por motivação médica, podem ser fornecidas exclusivamente para médicos, resguardando-se a identidade civil do(a) doador(a).
- As clínicas, centros ou serviços onde são feitas as doações devem manter, de forma permanente, um registro com dados clínicos de caráter geral, características fenotípicas e uma amostra de material celular dos doadores, de acordo com legislação vigente.
- Na região de localização da unidade, o registro dos nascimentos evitará que um(a) doador(a) tenha produzido mais de duas gestações de crianças de sexos diferentes em uma área de um milhão de habitantes. Um(a) mesmo(a) doador(a) poderá contribuir com quantas gestações forem desejadas, desde que em uma mesma família receptora.
- A escolha das doadoras de oócitos é de responsabilidade do médico assistente. Dentro do possível, deverá garantir que a doadora tenha a maior semelhança fenotípica com a receptora.
- Não será permitido aos médicos, funcionários e demais integrantes da equipe multidisciplinar das clínicas, unidades ou serviços participar como doadores nos programas de RA.
- É permitida a doação voluntária de gametas, bem como a situação identificada como doação compartilhada de oócitos em RA, em que doadora e receptora, participando como portadoras de problemas de reprodução, compartilham tanto do material biológico quanto dos custos financeiros que envolvem o procedimento de RA. A doadora tem preferência sobre o material biológico que será produzido.
Sobre a gestação de substituição (Cessão temporária do útero)
As clínicas, centros ou serviços de reprodução assistida podem usar técnicas de RA para criarem a situação identificada como gestação de substituição, desde que exista um problema médico que impeça ou contraindique a gestação na doadora genética, em união homoafetiva ou pessoa solteira.
- A cedente temporária do útero deve pertencer à família de um dos parceiros em parentesco consanguíneo até o quarto grau (primeiro grau – mãe/filha; segundo grau – avó/irmã; terceiro grau -tia/sobrinha; quarto grau – prima). Demais casos estão sujeitos à autorização do Conselho Regional de Medicina.
- A cessão temporária do útero não poderá ter caráter lucrativo ou comercial.
- Nas clínicas de reprodução assistida, os seguintes documentos e observações deverão constar no prontuário da paciente:
3.1. Termo de consentimento livre e esclarecido assinado pelos pacientes e pela cedente temporária do útero, contemplando aspectos biopsicossociais e riscos envolvidos no ciclo gravídico-puerperal, bem como aspectos legais da filiação;
3.2. Relatório médico com o perfil psicológico, atestando adequação clínica e emocional de todos os envolvidos;
3.3. Termo de Compromisso entre o(s) paciente(s) e a cedente temporária do útero (que receberá o embrião em seu útero), estabelecendo claramente a questão da filiação da criança;
3.4. Compromisso, por parte do(s) paciente(s) contratante(s) de serviços de RA, de tratamento e acompanhamento médico, inclusive por equipes multidisciplinares, se necessário, à mãe que cederá temporariamente o útero, até o puerpério;
3.5. Compromisso do registro civil da criança pelos pacientes (pai, mãe ou pais genéticos), devendo esta documentação ser providenciada durante a gravidez;
3.6. Aprovação do cônjuge ou companheiro, apresentada por escrito, se a cedente temporária do útero for casada ou viver em união estável.
Cuidados gerais para todos (Hábitos e estilos de vida)
Alimentação e atividade física
O estado nutricional e o estilo de vida podem causar grande influência na fertilidade, tanto feminina quanto masculina. O conjunto de hábitos e práticas diárias, como elevado consumo alcoólico, tabagismo, sedentarismo e consumo alimentar inadequado, pode afetar a saúde reprodutiva de ambos.
Com a diminuição na taxa de fertilidade da população mundial, e o aumento pela procura por tratamentos que melhorassem essa condição, o número de pesquisas na área cresceu. Diferentes estudos afirmam que o baixo peso (IMC menor que 17 kg/m2) e as condições de sobrepeso ou obesidade em mulheres (IMC maior que 25 kg/m2) estão associados a um aumento da infertilidade ou a desfechos gestacionais indesejados.
O estado nutricional e o estilo de vida masculino também exercem grande influência sobre a fertilidade. O conjunto de hábitos inadequados também pode afetar a saúde reprodutiva masculina. Acredita-se que os efeitos desses hábitos possam interferir negativamente na produção do sêmen, bem como na qualidade, quantidade e motilidade dos espermatozoides. Essas situações podem ocasionar alterações no funcionamento do sistema reprodutor e interferir negativamente na saúde reprodutiva de homens e mulheres. O casal saudável tem mais chances de engravidar. Esta é uma ótima forma de fortalecer os laços do casal em um projeto que, em última instância, é de ambos.
O padrão alimentar mediterrâneo vem sendo recomendado como um modelo de alimentação saudável. Este modelo é praticado em diferentes partes do mundo com efeitos benéficos para a saúde humana.
Vale ressaltar que a Dieta Mediterrânea não é apenas um padrão alimentar, mas também uma coleção de hábitos saudáveis tradicionalmente seguidos pelas populações dos países que se localizam ao redor do Mar Mediterrâneo, como Grécia, Espanha, Itália, Portugal, Marrocos, França e os demais ali localizados.
A Dieta Mediterrânea tradicional possui características marcantes que a transformaram no padrão alimentar mais saudável do mundo. Entre elas estão:
- Abundância de alimentos frescos e naturais (frutas, vegetais, pães, cereais, batatas, feijões, oleaginosas e sementes);
- Alimentos cultivados minimamente processados, respeitando a sazonalidade e a regionalidade;
- Frutas frescas ou doces contendo açúcares ou mel, como sobremesas típicas, consumidos apenas em quantidades moderadas;
- Azeite de oliva, como a principal fonte de gordura;
- Produtos lácteos (principalmente queijos e iogurte) consumidos em quantidades moderadas;
- Consumo médio de quatro ovos por semana;
- Elevado consume de peixes e frutos do mar;
- Carne vermelha consumida em baixas quantidades;
- Consumir sucos naturais de uva (orgânica);
- Evitar alimentos inflamatórios como aqueles que contenham glúten.
Praticar atividade física regularmente
A população da região mediterrânea era intensamente ativa na época em que se iniciaram as pesquisas sobre o padrão, o que demonstra que os bons hábitos não estavam exclusivamente associados ao padrão alimentar. Sendo assim, a prática regular de qualquer atividade física deve ser incentivada para todos os casais interessados em melhorar o estilo de vida em busca de uma gestação segura e bem-sucedida. Recomendamos, por exemplo, caminhadas de média intensidade, no mínimo, quatro vezes por semana, por 40 minutos.
Para saber mais detalhes:
www.ebookdietadafertilidade.com.br
www.ebookinflamaçõescronicas.com.br
Hábitos de vida inadequados
Tabagismo (cigarro): o cigarro é considerado o veneno reprodutivo mais potente do século 21. Vários estudos científicos comprovam seu efeito deletério sobre a saúde reprodutiva. A fumaça do cigarro contém centenas de substâncias tóxicas, incluindo nicotina, monóxido de carbono, polônio radioativo, alcatrão, fenol, ácido fórmico, ácido acético, chumbo, cádmio, zinco, níquel, benzopireno e substâncias radioativas, as quais afetam a função reprodutiva em vários níveis. No homem, alteram a produção dos espermatozoides e a qualidade do sêmen, além de levar ao aumento na fragmentação do DNA do espermatozoide, o que está associado a maior taxa de aborto e insucesso nos tratamentos de reprodução. Na mulher, o cigarro altera a motilidade tubária, a divisão das células do embrião, a formação do blastocisto, o muco cervical, a receptividade endometrial (mesmo com óvulos/embriões doados) e a implantação. A fertilidade é reduzida em 25% nas mulheres que fumam até 20 cigarros ao dia, e em 43% naquelas que fumam mais de 20 cigarros, ou seja, o declínio da fertilidade tem relação direta com a dose de nicotina. Durante a gestação, o fumo pode aumentar a incidência de placenta prévia, descolamento prematuro da placenta e parto prematuro. Deve-se sempre estimular as pessoas a pararem de fumar, especialmente os casais que estão tentando engravidar, principalmente homens nessa situação que apresentam contagem de sêmen no limite inferior à normalidade. Entretanto, mesmo com contagem de sêmen normal, o fumo deve ser desencorajado.
Drogas recreativas: a cada ano, novas drogas são introduzidas no “mercado do vício”. Embora nem todas estejam comprovadamente associadas à fertilidade, os prejuízos causados são fortes indícios quando comparados a outras drogas mais antigas. Todas elas agem no sistema nervoso central estimulando, bloqueando e interferindo nos hormônios, principalmente do eixo hipotálamo hipofisário, fundamentais para o bom funcionamento do sistema reprodutor. Por isso, podemos nos arriscar a afirmar que perturbam a fertilidade tanto do homem quanto da mulher.
Álcool: em doses diminutas, o álcool possui discreta ou nenhuma ação sobre as funções reprodutiva e sexual. O consumo crônico e prolongado, no entanto, prejudica ambas as funções, podendo atingir mais de 80% de comprometimento nos dependentes. Uma meta-análise indicou que as mulheres que bebem três ou mais drinques por dia têm risco 60% maior de apresentar infertilidade quando comparadas àquelas que não bebem. Não houve distinção, nesses estudos, entre o tipo de bebida, podendo ser vinho, cerveja e/ou coquetéis.
Cafeína: a queda da fertilidade feminina está associada à alta dose de cafeína (> 500 mg/dia, equivalente a 5 xícaras por dia). Durante a gravidez, consumir mais de 300 mg/dia de cafeína aumenta o risco de aborto. O consumo moderado (1 a 2 xícaras por dia) não demonstra efeitos adversos na fertilidade ou na gravidez.
Casais homoafetivos femininos
Em qualquer casal homoafetivo, não é possível gerar uma criança com material genético de duas mulheres ou dois homens. Nos casais femininos, sempre é necessário utlizar sêmen doado, podendo haver duas possibilidades: inseminação artificial ou fertilização in vitro.
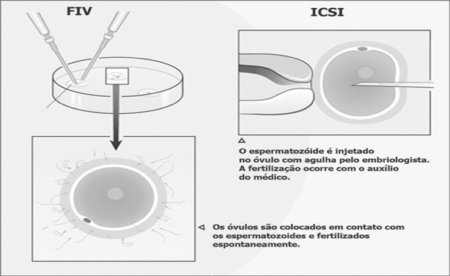
Qual a diferença entre Inseminação Artificial e Fertilização in vitro (FIV)
A inseminação artificial é um método acompanhado por um médico e consiste no processo de colocar o sêmen direto na cavidade intrauterina, perto das trompas, portanto a fertilização ocorre no interior do organismo materno, como em uma gravidez espontânea, ao passo que a FIV é totalmente diferente, pois a fertilização e o desenvolvimento embrionário inicial ocorrem no laboratório de fertilização. Na inseminação, sempre uma das mulheres irá gestar com seus próprios óvulos. Já a FIV chama-se fertilização in vitro porque a fecundação é feita em laboratório (veja detalhes mais à frente), ou seja, diferentemente do que ocorre no método natural, a formação do embrião (junção do gameta feminino, o óvulo, com o gameta masculino, o espermatozoide) acontece fora do útero da mulher. Aqui teremos duas possibilidades: na primeira, uma das mulheres vai gestar com os seus próprios óvulos, na segunda é a gestação compartilhada. Neste caso, as duas mulheres passam por exames que avaliam a capacidade reprodutiva, anatomia uterina, análise de fatores como idade e doenças como diabetes, hipertensão etc. Dessa forma, é possível que uma mulher viva a gestação do filho biológico de sua parceira. Esse método é garantido como direito pelo Conselho Federal de Medicina, desde a Resolução CFM nº 2.121/2015, e reafirmado na Resolução CFM nº 2.168/2017.
Pontos importantes a serem levados em consideração são a idade e a saúde da mulher que vai doar/fornecer o óvulo. Sabe-se que a idade do óvulo é um fator fundamental para as chances de sucesso, independente de qual técnica de reprodução assistida foi a indicada, assim como na incidência de complicações materno-fetais.
Consulta e exames importantes preparatórios
Todas as mulheres que se submeterão a um tratamento de reprodução assistida devem procurar um centro especializado em reprodução humana para avaliação. Na consulta serão explicados todo o processo necessário para o tratamento, as opções, assim como chances de sucesso e limitações. Vale lembrar que a idade da mulher e a reserva ovariana são muito importantes para se avaliar a chance de gravidez.
Além de ser explicado todo o processo às parceiras, elas deverão passar por uma avaliação clínica e ginecológica para escolher qual procedimento adotado, assim como quem desempenhará cada papel.

Caso optem por inseminação intrauterina, somente aquela que vai ser submetida ao tratamento deverá passar por avaliação. Caso seja fertilização in vitro, é preciso identificar quem terá os ovários estimulados e quem vai gestar para que os exames sejam direcionados de acordo com o papel que cada uma desempenhará: os exames de função ovariana para a que fornecerá os óvulos e os de avaliação uterina e falhas de implantação para aquela que irá gestar. Caso a mesma mulher for desempenhar os dois papéis, somente ela passará por avaliação, de forma completa.
No caso de quem fornecerá os óvulos, a avaliação clínica é importante para saber se não há riscos para a estimulação ovariana com hormônios (chance de trombose, câncer hormônio dependente) ou de acidentes na hora da coleta (cirurgias pélvicas, tumores pélvicos, endometriose). Isso é importante para se escolher o melhor esquema de estimulação e planejar a coleta de óvulos. Além disso, avaliação ginecológica e ultrassom para avaliar os ovários em relação a tamanho, número de folículos e acessibilidade dos mesmos.
Para a que vai gestar, devemos avaliar doenças clínicas que podem afetar a gravidez, além de um exame ginecológico e ultrassom para avaliar a anatomia do útero que deve ser perfeita para receber os embriões.
Além disso, alguns exames devem ser solicitados. Em caso de FIV, são eles:
Para ambas (quem vai fornecer os óvulos e quem vai receber os embriões):
- Exames gerais: Tipagem sanguínea, hemograma completo, coagulograma e vitamina D.
- Citologia oncótica (Papanicolau)
- Exame de secreção vaginal: bacteroscopia e cultura, culturas para micoplasma / ureaplasma, Neisseria gonorrhoeae e pesquisa de clamídia por PCR.
- Sorologias: hepatite B, hepatite C, sífilis, HIV 1 e 2, HTLV 1 e 2 e Zika Vírus- IgM.
- Hormônios: TSH, T4 livre e prolactina.
- Ultrassom transvaginal
- Outros exames, como ultrassom de mamas e mamografia podem ser necessários de acordo com o caso.
Para quem vai fornecer os óvulos:
- Cariótipo com Banda G (avalia os cromossomos da paciente),
- A avaliação da Reserva Ovariana é fundamental e é avaliada pela medida no sangue, entre o 3º e 5º dia do ciclo menstrual, de alguns hormônios: FSH, LH e estradiol, e o principal deles, o hormônio antimulleriano (AMH ou HAM), além da contagem dos folículos antrais.
- Uma avaliação clínica mais completa pode ser necessária se paciente tiver fatores de risco para receber hormônios.
Para quem vai receber os embriões e gestar:
- Exames clínicos gerais: além dos básicos já citados, colesterol e frações, triglicérides, glicemia de jejum. Dependendo da idade e antecedentes, avaliação clínica mais completa com ECG, ecocardio, etc.
- Sorologias: além das já citadas, rubéola, toxoplasmose, citomegalovírus e, atualmente, sarampo
- Outros exames podem ser solicitados de forma individualizada: trombofilias, anticorpos, ressonância nuclear magnética de pelve ou ultrassom transvaginal com preparo intestinal para pesquisa de endometriose/adenomiose, vídeo-histeroscopia e biópsia do endométrio.
Exames Necessários para as pacientes submetidas à Fertilização in vitro (FIV)
Para as pacientes que serão submetidas a Inseminação Intrauterina, por ser um procedimento mais simples, os exames, em geral, não necessitam ser tão elaborados e devem ser individualizados. Um exame importante que não incluímos na FIV, mas que é importante no caso da inseminação, é uma avaliação das trompas com HISTEROSSALPINGOGRAFIA.
Bancos de sêmen
Os bancos de sêmen fornecem, pelos seus sites, um catálogo que descreve detalhes particulares dos doadores anônimos, como cor dos olhos, cabelos, estatura, profissão, hobbies etc. São poucos os bancos de sêmen no Brasil e, por isso, nem sempre é fácil achar uma amostra de doador compatível com as características do futuro pai. Muitas vezes não se encontra, nas amostras disponíveis, características físicas que coincidam com a aparência.
Neste caso, o IPGO orienta os pacientes na busca de amostras em bancos de sêmen internacionais, que oferecem amostras com as mais diversas características e, certamente, pelo menos uma delas deverá estar de acordo com o perfil do solicitante.
Bancos de Sêmen no Brasil
Pro-seed – São Paulo (www.pro-seed.com.br)
Este é praticamente o único banco de sêmen no Brasil com o maior número de amostras disponíveis. Os demais são muito pequenos e oferecem um número restrito de amostras. O banco de sêmen fornece às clínicas de reprodução humana um catálogo numerado. Cada número corresponde a um doador que vem seguido das características físicas e pessoais: etnia, tipo de sangue, tipo físico, estatura, cor dos olhos, cabelo, pele, ascendência, qualificações profissionais e hobby. Os doadores são selecionados segundo os critérios: idade superior a 21 anos e inferior a 40 anos, integridade física e mental comprovada, fertilidade reconhecida, ser anônimo e sem benefício financeiro. A amostra escolhida deverá estar em harmonia com as características físicas e intelectuais desejadas pelo casal.
Os doadores realizam os seguintes exames laboratoriais: Hepatites B e C, HTLV 1 e 2, HIV I e II, Sífilis, Cariótipo simples e cultura seminal (pesquisa de bactéria e fungos no sêmen). Os exames são realizados no dia da coleta e repetidos após seis meses. Depois desse período, as amostras são liberadas.
O cadastro dos doadores está disponível para as clínicas de reprodução humana, sem os nomes dos doadores, somente numerados para identificação e apresentado aos pacientes interessados da seguinte maneira:
Banco de Sêmen Internacional
Seattle Sperm Bank (www.seattlespermbank.com)
FairFax Cryobank – São Paulo (http://www.fairfaxcryobank.com.br/)
O Fairfax Cryobank é representado no Brasil por Crio Brasil Serviços, distribuidor exclusivo dos produtos.
Os bancos de sêmen internacionais têm a vantagem de fornecer mais características do doador e, em alguns casos, disponibilizar inclusive fotos. Tem a desvantagem do custo mais elevado e a demora de cerca de 40 dias para chegar a amostra.
Individualizar os tratamentos para cada casal é fundamental!
Para se definir o melhor protocolo para a estimulação ovariana é importante compreender o significado de “individualizar”. Individualizar significa ajustar algo para que melhor se adéque aos requisitos de alguém; personalizar. Assim, o protocolo de estimulação ovariana deve ser individualizado para cada paciente de acordo com o histórico e a situação em que se encontra. Para que qualquer organismo atinja um ótimo estado de maturação (amadurecimento), deve-se primeiro passar por pleno crescimento e desenvolvimento. Uma boa analogia é o fruto colhido de uma árvore antes de ter se desenvolvido totalmente. Ele ainda pode amadurecer na prateleira e até parecer tão atraente como aquele que teve um desenvolvimento adequado. Entretanto, não terá a mesma qualidade. Os mesmos princípios se aplicam para o desenvolvimento e maturação dos óvulos da mulher. Um desenvolvimento adequado, bem como o sincronismo preciso no início de maturação dos óvulos com os hormônios apropriados, é essencial para se conseguir um óvulo ideal, uma boa fertilização, um ótimo embrião e, finalmente, a gravidez. Na verdade, nos casos em que a maturação dos óvulos não é devidamente sincronizada, há um aumento do risco de aneuploidia (anormalidades cromossômicas estruturais e numéricas), levando ao comprometimento do desempenho reprodutivo.
O potencial dos óvulos de uma mulher sofrerem maturação ordenada, fertilização bem sucedida e posterior progressão para “embriões de boa qualidade”, capazes de produzir um bebê saudável, é, em grande parte, determinado geneticamente. No entanto, a expressão do potencial reprodutivo é influenciada por numerosas variáveis extrínsecas no ovário e endométrio durante a fase pré-ovulatória do ciclo, principalmente nos casos de mulheres más respondedoras ou das mais maduras (mais velhas), cujos ovários acompanham o envelhecimento, independentemente da aparência jovial de cada uma. Nesses casos, os protocolos de estimulação precisam ser personalizados para atender às necessidades individuais. A utilização de protocolos especiais como Duostim, utilização do hormônio de crescimento (GH), G-CSF ou outras estratégias para más respondedoras, deve ser avaliada individualmente. Tudo o que podemos fazer é evitar comprometer o ambiente de ovário durante a estimulação ovariana e, assim, evitar mais prejuízo à qualidade do óvulo.
Por outro lado, este conceito também é importante para se programar a transferência do embrião. Uma avaliação individualizada dos fatores relacionados a falhas de implantação deve ser feito e, se necessários, tratados. O ambiente uterino deve ser o mais favorável possível e, com uma avaliação criteriosa podemos maximizar as chances de implantação e gravidez.
Inseminação Intrauterina (IIU)
Nos tratamentos de inseminação intrauterina (média complexidade), a fertilização ocorre no próprio organismo e não necessita de uma estrutura de laboratório complexa nem ambiente cirúrgico para ser realizada. Além disso, utilizam protocolos simples e de baixo risco para estimulação ovariana, sendo mais fáceis de ser realizados pelo ginecologista geral. Já na alta complexidade, a fertilização ocorre no laboratório, por isso chamamos fertilização in vitro (FIV), necessitando de um equipamento laboratorial sofisticado, além de envolver protocolos mais complexos de estimulação ovariana.
Para definirmos o melhor tratamento é importante primeiramente decidirem quem vai fornecer os óvulos e quem vai gestar. Na inseminação, a mesma mulher obrigatoriamente desempenhará as duas funções. Além disso, é necessária uma avaliação completa da mulher para saber se devemos começar por algo mais simples ou se seria indicado ir direto para o de alta complexidade. Isso se justifica, pois qualquer tratamento, por mais simples que seja, envolve desgaste emocional e frustração se o resultado for negativo. Assim, é necessária uma pesquisa mínima da fertilidade antes da indicação de um determinado tratamento para que não se insista em uma opção com baixa chance de sucesso.
A inseminação intrauterina (IIU) pode ser realizada em ciclos espontâneos, entretanto, vários autores já demonstraram maiores índices de sucesso quando os ciclos são estimulados.
Passo a passo da inseminação intrauterina (IIU)
1. Estimulação ovariana
A estimulação ovariana é uma etapa importante para o sucesso do tratamento de IIU. Tem o objetivo de estimular mais de um oócito, dois ou três no máximo, para que se aumente a taxa de um resultado positivo
Muitos estudos têm demonstrado os benefícios da estimulação ovariana quando comparados aos ciclos espontâneos. A taxa de gravidez sem estimulação ovariana é muita baixa, cerca de 4%. Comparando-se as taxas de gravidez entre grupos de pacientes que tiveram os ovários estimulados com outras que não tiveram, foram encontradas taxas de gestações até cinco vezes maiores no grupo que recebeu o estímulo.
Para a estimulação ovariana, é necessário compreendermos alguns conceitos sobre o ciclo menstrual normal da mulher. FSH e LH são hormônios chamados gonadotrofinas, sendo produzidos pela glândula hipófise e agindo nos folículos ovarianos (pequenos cistos que contém um óvulo cada). O FSH, entre outras coisas, faz os folículos crescerem e produzirem estradiol (hormônio importante para estimular o endométrio). Quando os folículos atingem o tamanho acima de 17 mm, ocorre o pico do hormônio LH, que desencadeia a ovulação 36h após e induz a maturidade do óvulo.
Além disso, é importante que o ginecologista não só tenha conhecimento dos medicamentos utilizados na rotina deste procedimento, como também realize exames de ultrassom para o acompanhamento do desenvolvimento folicular. Se o profissional não tiver este recurso, deverá ter parceria com uma clínica de ultrassom experiente que possa avaliar o ciclo ovulatório desde o início da menstruação.
O primeiro exame deverá ocorrer no segundo ou terceiro dia da menstruação para que se confirme a inexistência de folículos remanescentes do ciclo anterior e, depois deve ser repetido, de acordo com o desenvolvimento folicular, até que se obtenha pelo menos um folículo com o diâmetro médio de 18 mm e o endométrio com espessura superior a 7 mm. Um laboratório de análises clínicas que entregue em poucas horas o resultado de dosagens hormonais de estradiol e progesterona pode ser útil nas situações em que houver dúvidas quanto a real fase do ciclo ovulatório ou se a ovulação ocorreu antes do período previsto. Quando isso ocorrer, deve ser ponderado o cancelamento do procedimento. A estimulação ovariana pode utilizar diferentes medicamentos, orais ou injetáveis, isolados ou em associação. Os medicamentos injetáveis contém o hormônio FSH, enquanto os orais induzem o corpo a aumentar a produção deste hormônio. O FSH é o hormônio responsável pelo crescimento folicular.
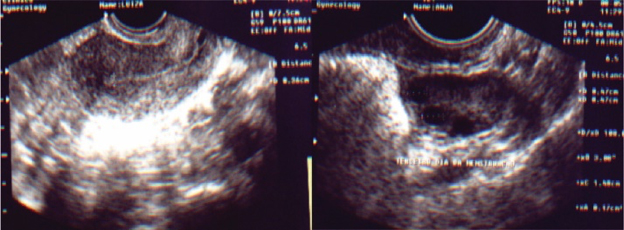
2. Monitorização do crescimento folicular com ultrassonografia transvaginal
O ultrassom transvaginal é realizado a cada dois ou três dias, durante o período de estimulação, para acompanhar o crescimento e desenvolvimento dos folículos.
ULTRASSOM NO 2º – 3º DIA DO CICLO MENSTRUAL PARA INICIAR ESTIMULAÇÃO OVARIANA
ULTRASSOM DE 8º DIA DO CICLO MENSTRUAL COM ESTIMULAÇÃO OVARIANA
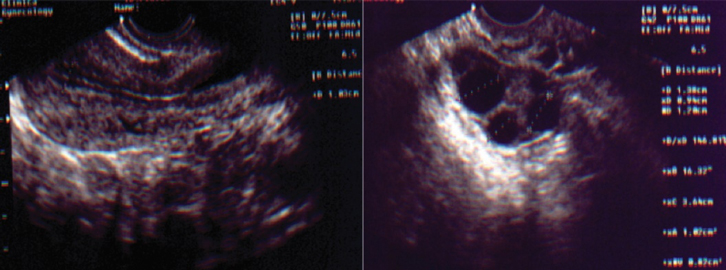
ULTRASSOM DE 10º DIA DO CICLO MENSTRUAL COM ESTIMULAÇÃO OVARIANA
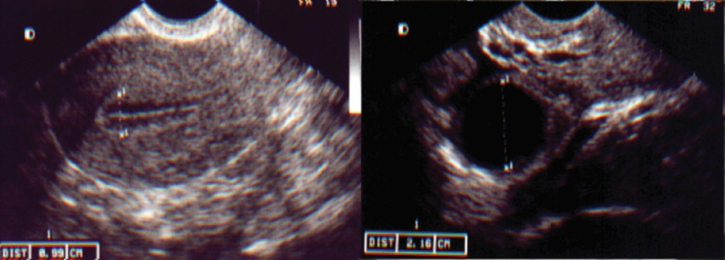
Importante: caso haja crescimento de mais de 3 folículos, o ciclo deve ser cancelado e a paciente orientada a não ter relação desprotegida pelo risco de gravidez múltipla. Outra opção é converter o ciclo para FIV.
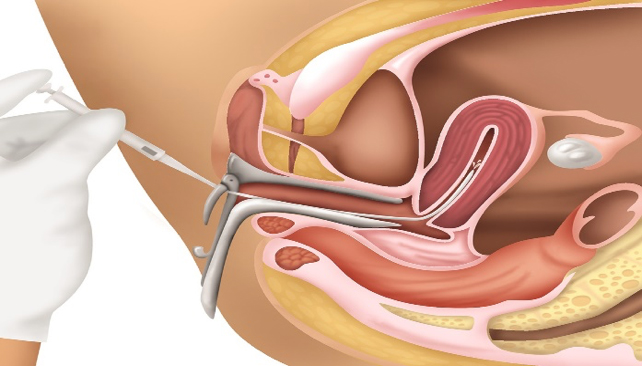
3. O momento da inseminação intrauterina
Quando pelo menos um folículo atinge 18 mm, a ovulação deve ser desencadeada utilizando um hormônio chamado hCG, também injetável, que tem ação semelhante ao LH. A amostra do banco de sêmen já deve estar disponível na clínica de reprodução assistida.
A inseminação intrauterina, em geral, ocorre 36 horas após o hCG, que é quando a ovulação costuma ocorrer. Alguns autores mostraram bons resultados com a inseminação dupla, com 12 e 36 horas após a aplicação do hCG, mas isto não é feito de rotina.
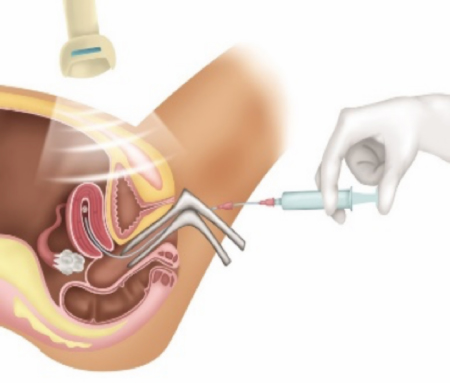
A inseminação intrauterina é um procedimento relativamente simples. É realizada em ambiente ambulatorial sem anestesia, é indolor e não dura mais que alguns minutos. Com a paciente em posição ginecológica, coloca-se o espéculo, semelhante ao exame ginecológico de rotina. É feita uma limpeza vaginal com água destilada ou soro fisiológico, pois os agentes antissépticos são lesivos aos espermatozoides. O esperma é, então, colocado dentro do útero, através de um cateter flexível que transpassa a vagina e o canal cervical. Para evitar que o cateter bata no fundo, pode-se realizar a inseminação guiada por ultrassom abdominal.
Após o procedimento, a paciente permanece em repouso por 30 minutos e, tendo alta, volta à vida normal.
4. Suporte de fase lútea
Para suporte de fase lútea, pode-se usar a progesterona. No mercado existem diferentes formas de apresentação da progesterona (oral, vaginal, injetável), não havendo diferenças significativas entre elas. Normalmente, utilizamos 200 mg de progesterona micronizada (Utrogestan® ) via vaginal.
Orienta-se o teste de gravidez 14 dias após a inseminação intrauterina.
5. Taxas de sucesso
Quanto à taxa de sucesso dos tratamentos de baixa complexidade, ela está muito relacionada às condições reprodutivas da mulher (idade, útero e outros fatores), mas é inferior à das técnicas de alta complexidade. Na inseminação intrauterina em pacientes abaixo de 30 anos, a taxa de gravidez é de 20 % a 22%, mas, acima de 37 anos, cai para menos de 10%.
6. Complicações
Complicações são raras neste tipo de procedimento. Mas, dentre as possibilidades, existe um risco muito baixo de infecção (0,2%), reação alérgica, síndrome da hiperestimulação ovariana (1% a 2%) e gestação múltipla (16%) quando a estimulação ovariana não for bem controlada.
Fertilização in vitro (FIV)
Entre os processos de reprodução humana para casais homoafetivos femininos, a FIV é o que oferece os melhores resultados na concepção do bebê.
Lembramos que se chama fertilização in vitro porque a fecundação é feita em laboratório, ou seja, diferentemente do que ocorre no método natural, a formação do embrião (junção do gameta feminino, o óvulo, com o gameta masculino, o espermatozoide) acontece fora do útero da mulher.
Lembramos mais uma vez que uma das possibilidades pode ser a gestação compartilhada, quando um embrião gerado por meio da técnica de reprodução humana assistida NÃO é transferido para o útero da mãe biológica, mas para o de sua companheira. Dessa forma, é possível que uma mulher viva a gestação do filho biológico de sua parceira.
O processo pode ser dividido em 6 fases:
- 1ª Fase – Estimulação ovariana.
- 2ª Fase – Bloqueio dos hormônios.
- 3ª Fase – Aspiração e recuperação dos óvulos.
- 4ª Fase – Fertilização dos óvulos pelo espermatozoide.
- 5ª Fase – Transferência do(s) embrião(ões) para o útero.
- 6ª Fase – Suporte hormonal.
1ª Fase – Estímulação ovariana
A primeira fase é a estimulação ovariana propriamente dita, quando medicamentos, em geral injetáveis, são administrados para fazer com que vários folículos cresçam nos ovários. Os medicamentos utilizados para indução são chamados gonadotrofinas, contém o hormônio FSH e são encontrados em diversos tipos, dosagens e nomes comerciais. As dosagens diárias recomendadas são reguladas de acordo com a necessidade verificada pelos exames realizados sistematicamente durante essa fase (hormônios e ultrassom). A estimulação ovariana deverá ser acompanhada pela ultrassonografia para avaliar o crescimento e o desenvolvimento dos folículos ovarianos (dentro dos quais estão os óvulos) até que atinjam um diâmetro médio aproximado de 18mm. A espessura do endométrio (tecido que reveste o útero internamente e onde o embrião se implantará) também é avaliada e deverá ser superior a 7mm. Normalmente, são realizados dois a quatro exames de ultrassom transvaginal durante o ciclo, marcados em intervalos médios de dois dias, iniciando no quinto dia após o início da estimulação, até que alcance o ponto pré-ovulatório. Sempre que as datas de exames caírem no domingo ou feriado, não se preocupe, pois, esses exames poderão ser antecipados ou adiados sem interferir no sucesso final do procedimento. Caso seja necessário, os exames serão realizados também nestes dias.
Quando os folículos atingem um diâmetro médio de 18 mm é administrado um medicamento específico: hCG (Ovidrel® ou Choriomon® ), se os embriões forem ser transferidos no mesmo ciclo para o útero da paciente que colherá os óvulos ou Gonapeptyl® ou Lupron® , se os embriões NÃO forem transferidos no mesmo ciclo ou forem transferidos à parceira. Estes medicamentos visam a maturação final dos óvulos. As doses e os horários das medicações têm influência direta no horário da captação dos óvulos. Realizamos a aspiração dos óvulos entre 34 e 36 horas (conforme protocolo escolhido) após a aplicação. Os efeitos colaterais (raros) mais comuns desses medicamentos são: instabilidade emocional, dores de cabeça, perda de apetite, dor abdominal e dor no local das injeções. Neste último caso, a massagem e o calor local (compressas) podem aliviar esses sintomas.
Para que se alcance o objetivo almejado é fundamental a disciplina na medicação e no controle na estimulação ovariana e, para isso, devem ser seguidas as seguintes recomendações:
- Utilize somente os medicamentos recomendados.
- O dia do ciclo é sempre contado a partir do primeiro dia da menstruação.
- Os medicamentos deverão ser tomados e aplicados sempre no mesmo horário.
- A quantidade de medicação utilizada até a coleta dos óvulos vai depender da evolução do crescimento dos folículos. É recomendável sempre medicação extra de reserva.
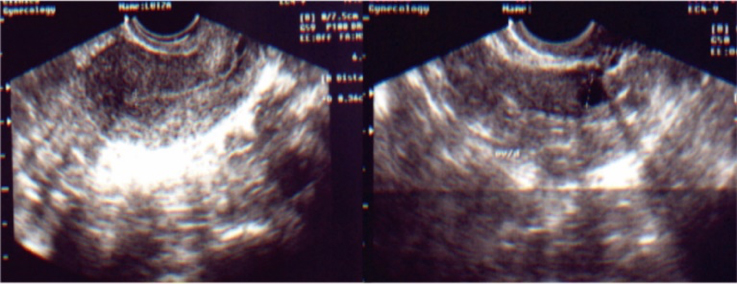
ULTRASSOM NO 3º DIA DO CICLO
CONTROLE ULTRASSONOGRÁFICO NO 5º DIA DA ESTIMULAÇÃO OVARIANA
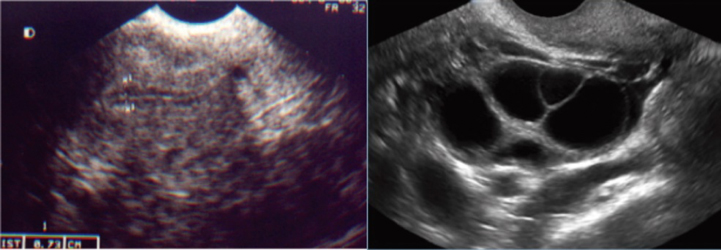
CONTROLE ULTRASSONOGRÁFICO NO 11º DIA DA ESTIMULAÇÃO OVARIANA
2ª Fase – Bloqueio dos hormônios
Consiste no bloqueio da produção pelo organismo dos hormônios que agem nos ovários com medicação adequada. Com esta conduta temos o controle da função ovariana “em nossas mãos” não havendo praticamente perigo de ocorrer ovulação fora do previsto. Isto é, sem esses medicamentos, o mecanismo de controle da ovulação estaria também sob a influência dos hormônios do próprio organismo e a paciente poderia ovular antes da hora programada de colher os óvulos.
O bloqueio pode ser TARDIO (esquema curto ou PROTOCOLO CURTO, realizado durante a estimulação ovariana) ou PRÉVIO (esquema longo ou PROTOCOLO LONGO, iniciado antes da estimulação ovariana). A decisão pelo bloqueio prévio ou tardio vai depender de cada caso.
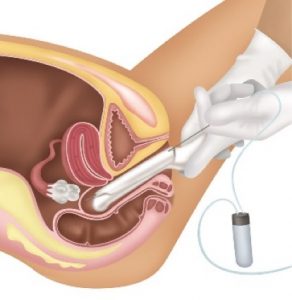
3ª Fase – Aspiração e recuperação dos óvulos
A paciente deverá comparecer ao laboratório especializado aproximadamente 35 horas após a administração do último medicamento (hCG ou Gonapeptyl). Neste momento, o médico estará presente para realizar o procedimento. Em jejum, em horário pré-estabelecido e em uma sala adequada, será dada uma medicação (sedação profunda com Propofol) para relaxar e dormir alguns minutos. Com auxílio do ultrassom, uma agulha especial e um aparato para sucção, os óvulos são colhidos e encaminhados para análise. Este processo é indolor e dura alguns minutos. Após cerca de 60 minutos em repouso em um quarto, a paciente será liberada, podendo executar atividades leves no mesmo dia, mas que não exijam destreza ou concentração (24 horas).
COLETA DE ÓVULOS
Este é o momento da decisão se irá congelar óvulos (vitrificação) ou fertilizá-los
4ª Fase – Fertilização dos óvulos
Os óvulos após a aspiração são separados, cultivados e classificados quanto à sua maturidade para que sejam fertilizados.
a) Amostra Seminal – Banco de Sêmen: a amostra proveniente do banco de sêmen deverá estar disponível para a fertilização no centro de reprodução humana. Ocorrerá pela técnica de ICSI , obrigatoriamente.
b) ICSI (Intracitoplasmatic Sperm Injection ou Injeção Intracitoplasmática de Espermatozoide): Os óvulos serão fertilizados por meio da micromanipulação dos gametas injetando-se um espermatozoide em cada óvulo – Injeção Intracitoplasmática de Espermatozoide. É uma técnica realizada por um profissional especializado que, por meio de uma pipeta microscópica, injeta um único espermatozoide dentro do óvulo.
No dia seguinte à ICSI, são verificados quantos óvulos conseguirem ser fertilizados, formando embriões, que terão seu crescimento acompanhado até o terceiro ou quinto dia de desenvolvimento. Normalmente, esperamos a fase de blastocisto (quinto dia), pois selecionamos os que têm mais chances de implantação, mas dependendo do caso, principalmente se poucos embriões em desenvolvimento, optamos por transferir no terceiro dia. Após o terceiro ou quinto dia, os embriões são então transferidos ao útero ou vitrificados.
5ª Fase – Transferência do(s) embrião(ões) para o útero
a) A escolha de quem receberá os embriões: já deverá estar definida. Se aquela que irá gestar for a companheira que não passou pela estimulação ovariana, o seu útero já deverá estar convenientemente preparado para receber o(s) embrião(ões). Caso contrário, os embriões deverão ser congelados (vitrificados) para serem transferidos posteriormente. Se quem for gestar for a mesma companheira que teve os ovários estimulados, os embriões poderão ser transferidos no mesmo ciclo, desde que as condições sejam favoráveis, caso contrário serão congelados (vitrificados) e transferidos em data oportuna.
b) Preparo do endométrio para receber os embriões: Quando uma das mulheres irá receber os embriões gerados com óvulos da parceira, é necessário fazer um preparo do endométrio (tecido que reveste internamente o útero) antes da transferência. Este preparo pode ser simultâneo à estimulação ovariana da parceira, com transferência de embriões frescos. Neste caso, devemos sincronizar os ciclos das duas mulheres com anticoncepcional, outros hormônios ou bloqueio hormonal.
Para o preparo endometrial, geralmente utilizamos estradiol exógeno e acompanhamos o endométrio por ultrassom. Como dito, isso pode ser precedido de um bloqueio hormonal, que pode ser feito com 1/2 ou 1 ampola de agonista do GnRH de depósito, na fase lútea (21° dia) do ciclo anterior.
Quando a paciente menstrua, no segundo ou terceiro dia, inicia-se estradiol via oral e/ou transdérmica. Em caso de bloqueio hormonal, pode-se aguardar mais dias até a parceira menstruar. Há 3 opções de estradiol: 6 mg via oral, 3 adesivos de 100 mcg trocados a cada 3 dias ou estradiol gel (6 pumps por dia). No IPGO, costumamos dar 4 mg via oral e um adesivo. Esta medicação será mantida por pelo menos dez dias e o endométrio acompanhado por ultrassom. No dia da coleta dos óvulos da parceira, se o endométrio estiver adequado (> 7 mm e de aspecto trilaminar), inicia-se a progesterona. Uma das seguintes opções será a utilizada:
- Progesterona injetável (Progesterone®): 50 a 100 mg/dia – intramuscular;
- Progesterona micronizada (Utrogestan®): 600 a 1200 mg/dia – via vaginal;
- Progesterona gel (Crinone® 8%): 1 a 2x/dia, via vaginal.
Em algumas situações pode ser adicionado o Duphaston® (didrogesterona 10 mg 12/12h, via oral).
A transferência será realizada 3 ou 5 dias após, dependendo do embrião ser de terceiro dia ou blastocisto.
No caso de transferência de embriões congelados, o processo é semelhante, iniciando a progesterona após pelo menos 10 dias de uso do estradiol se o endométrio estiver com aspecto satisfatório.
Ultrassom no 10o dia após preparo do endométrio
Em ciclos de transferência de embriões ou óvulos congelados, se a mulher tem ciclos regulares há ainda a opção de não utilizarmos medicação, somente acompanhando um ciclo ovulatório espontâneo, com a presença somente dos hormônios produzidos pelo próprio organismo. Deve ser acompanhado rigorasamente por ultrassom e dosagens hormonais (estradiol, progesterona e LH). Quando o folículo atinge mais de 17 mm, normalmente faz-se uso do hCG, que simula o pico de LH, que desencadeia a ovulação 36 horas depois. Isso pode ser antecipado caso o LH estiver em ascensão. No momento da ovulação, os oócitos são descongelados e fertilizados e a progesterona é introduzida. Caso os embriões já estejam vitrificados, a progesterona também é iniciada no dia da ovulação
c) A transferência do(s) embrião(ões) para o útero: é indolor, realizada sob visão do ultrassom, com cateter flexível e sem necessidade de anestesia, É introduzido um pequeno cateter pela vagina em direção ao colo do útero até atingir a cavidade uterina. O(s) embrião(ões) deve(m) ser colocado(s) de 1,5 cm a 2 cm abaixo do fundo uterino. A passagem do cateter deve ser um movimento delicado, pois as chances de gravidez têm muita ligação com este momento. Trata-se de um procedimento simples, mas que exige tranquilidade, um bom relaxamento da paciente e experiência do profissional. Após essa etapa, a paciente deverá ficar deitada por alguns minutos, retornando, posteriormente, para casa liberada a fazer atividades físicas limitadas, e orientada com as devidas medicações.
TRANSFERÊNCIA DE EMBRIÕES
d) Decisões importantes para o dia “D”
1- avaliação da qualidade dos embriões e escolha do dia da transferência (3º ou 5º dia?): no dia seguinte à fertilização, que ocorre horas após a aspiração dos óvulos, os embriões são analisados para verificar qual a porcentagem dos óvulos maduros que foram fertilizados. Na maioria das vezes, mesmo nos casos de ICSI, uma parte desses óvulos não se fertiliza. Já neste momento pode ser feita uma análise inicial microscópica e prognóstica da qualidade desses embriões e quais são os que têm maior chance de sobreviver e alcançar um estágio mais avançado de divisão celular. No terceiro dia, os embriões são mais uma vez estudados para que se faça uma nova classificação dos melhores. A classificação é baseada na “morfologia”. no dia seguinte à fertilização, que ocorre horas após a aspiração dos óvulos, os embriões são analisados para verificar qual a porcentagem dos óvulos maduros que foram fertilizados. Na maioria das vezes, mesmo nos casos de ICSI, uma parte desses óvulos não se fertiliza. Já neste momento pode ser feita uma análise inicial microscópica e prognóstica da qualidade desses embriões e quais são os que têm maior chance de sobreviver e alcançar um estágio mais avançado de divisão celular. No terceiro dia, os embriões são mais uma vez estudados para que se faça uma nova classificação dos melhores. A classificação é baseada na “morfologia”.
Na morfologia do embrião de terceiro dia (D3), dois itens são analisados: o número de células (deverá ser de 6 a 8) e o índice de fragmentação. Quanto menor o grau de fragmentação e número adequado de células, teoricamente, melhor será este embrião e maior será a chance de implantação. Neste dia serão conhecidos os de melhor qualidade e, assim, o médico especialista, o embriologista e o casal decidirão juntos quantos deles serão transferidos, número este que pode variar de um a quatro, e que dependerá das regras da ética, da idade da mulher e da qualidade dos embriões.
Comentário importantíssimo: ao classificarmos um embrião de melhor ou pior, não estamos concluindo que as crianças nascidas deles terão saúde diferente umas das outras. Significa simplesmente que, ao implantar os embriões que passaram pelo período de divisão celular inicial com facilidade, a chance de gerar uma gravidez deve ser estatisticamente maior. O embrião morfologicamente “mais feio” (menos células e mais fragmentado) poderá ter uma chance menor de implantação, mas gerar uma criança 100% saudável. Se no terceiro dia após a fertilização tivermos um número excessivo de embriões (superior a três), uma boa conduta é aguardarmos que esses embriões atinjam a fase de blastocistos (D5) para que os melhores passem por mais essa prova de seleção. Assim, no quinto ou sexto dia, os embriões que atingirem essa fase serão os que terão maior chance de implantação. E, mais uma vez, a decisão do dia da transferência será feita após a coleta dos óvulos e no decorrer do desenvolvimento dos embriões no laboratório. Dependerá de algumas variáveis importantes, por exemplo, idade da paciente e número de tentativas anteriores entre outras possibilidades.
Blastocistos: geralmente a melhor opção. Normalmente, por vias naturais, o embrião chega à cavidade uterina com cinco ou seis dias de vida, em um estágio chamado blastocisto. Assim, parece claro que, quando transferimos para a mulher embriões neste estágio (ou seja, cinco ou seis dias após a coleta dos óvulos, a chance de gravidez deve ser maior). Além do mais, como existe uma perda considerável no número de embriões durante esses cinco dias de desenvolvimento, ao se trasnferir um blastocisto, temos a garantia que ele já atingiu esta fase de desenvolvimento mais avançada em relação ao embrião de terceiro dia. Quando serão vitrificados, podemos ainda esperar até sete dias para ver se chegam à fase de blastocisto. Entretanto, nem sempre conseguimos que o embrião chegue a este estágio no laboratório e sabemos que muitos embriões serão perdidos.
Avaliação morfológica do embrião até o 5º dia de desenvolvimento
2- Quantos embriões devem ser transferidos?
O Conselho Federal de Medicina (CFM), desde a resolução CFM nº 1.957/2010 (Normas Éticas para a Utilização das Técnicas de Reprodução Assistida), definiu:
“O número máximo de embriões a serem transferidos para o útero não pode ser superior a quatro e são feitas as seguintes determinações:
- Mulheres com até 35 anos: até dois embriões;
- Mulheres entre 36 e 39 anos: até três embriões;
- Mulheres com 40 anos ou mais: até quatro embriões.”
Importante: para decidir o número de embriões a transferir, deve-se levar em conta a idade da mulher que forneceu os óvulos e não de quem receberá os embriões!!!
Essa norma é importante para diminuir o número de gestações múltiplas, fixando um número máximo de embriões de acordo com a idade. Como quanto maior a idade da mulher, menor a chance de implantação, podemos colocar mais embriões naquelas com idades mais avançadas. Entretanto, não se leva em conta a qualidade do embrião e se ele está em D3 ou blastocisto. Como blastocistos apresentam maior taxa de implantação que em D3, tendemos a colocar um menor número de embriões nesta fase. Hoje em dia, com a alta tecnologia empregada nos tratamentos de fertilização, a recomendação é transferir um, no máximo dois blastocistos, mas a decisão deverá ser individualizada para cada caso.
Outras preocupações que serão discutidas mais à frente: biópsia embrionária e vitrificação dos embriões.
6ª Fase – Suporte hormonal
Após a coleta dos óvulos, se a mesma paciente for transferir os embriões neste ciclo, iniciamos o suporte de fase lútea com progesterona e estradiol, se necessário. As opções são semelhantes na descrita no preparo endometrial, mas em geral em doses menores.
Quando a paciente tiver poucos óvulos, o suporte da fase lútea poderá ser feito com três doses de hCG 1.500U SC a cada três dias. Não se deve utilizar hCG para suporte na fase lútea se o número de óvulos for maior pelo risco de Síndrome de Hiperestimulação Ovariana.
Após a transferência, independente de ciclo fresco ou de congelado, realizamos um controle rigoroso das condições hormonais a fim de mantê-los em níveis satisfatórios para um adequado desenvolvimento embrionário intrauterino. As doses recomendadas desses hormônios são ajustadas de acordo com a necessidade da paciente e variam.
Durante a fase lútea, podem ser realizados exames de sangue que comprovam o equilíbrio hormonal (estradiol > 200 pg/mL e progesterona > 20 ng/mL). Caso haja necessidade, as doses da progesterona poderão ser modificadas e/ou introduzido reposição de estradiol, caso já não esteja sendo feita.
O dosagem de beta-hCG é realizado 10 a 12 dias após a transferência dos embriões e, se confirmar gravidez, o suporte hormonal deverá ser mantido até o terceiro mês de gestação.
Diagnóstico da gestação: após cerca de 10 dias contados a partir da transferência dos embriões para o útero, a paciente deverá realizar um exame de sangue (dosagem de beta-hCG) para confirmar a gravidez. Se positivo, repetimos o teste uma semana depois para saber se está subindo adequadamente e, após 2 semanas do primeiro teste, realizamos uma ultrassonografia para confirmarmos se a gravidez está tópica (dentro do útero), quantos embriões implantaram e se tem batimentos cardíacos (gravidez clínica). Daí em diante, repetimos o ultrassom a cada duas semanas até completar 12 semanas, quando então a paciente deve seguir seu pré-natal igual a uma gestação espontânea. Dezenas de semanas depois, o casal comemora o crescimento da família e o fato de que duas pessoas do mesmo sexo podem, sim, gerar um filho juntas.
Taxas de sucesso com a FIV
O sucesso da FIV vai depender de vários fatores:
- idade da mulher;
- qualidade dos óvulos e espermatozoides;
- qualidade dos embriões;
- qualidade endometrial;
- presença de outros fatores: mioma, adenomiose, endometriose, endometrite, etc
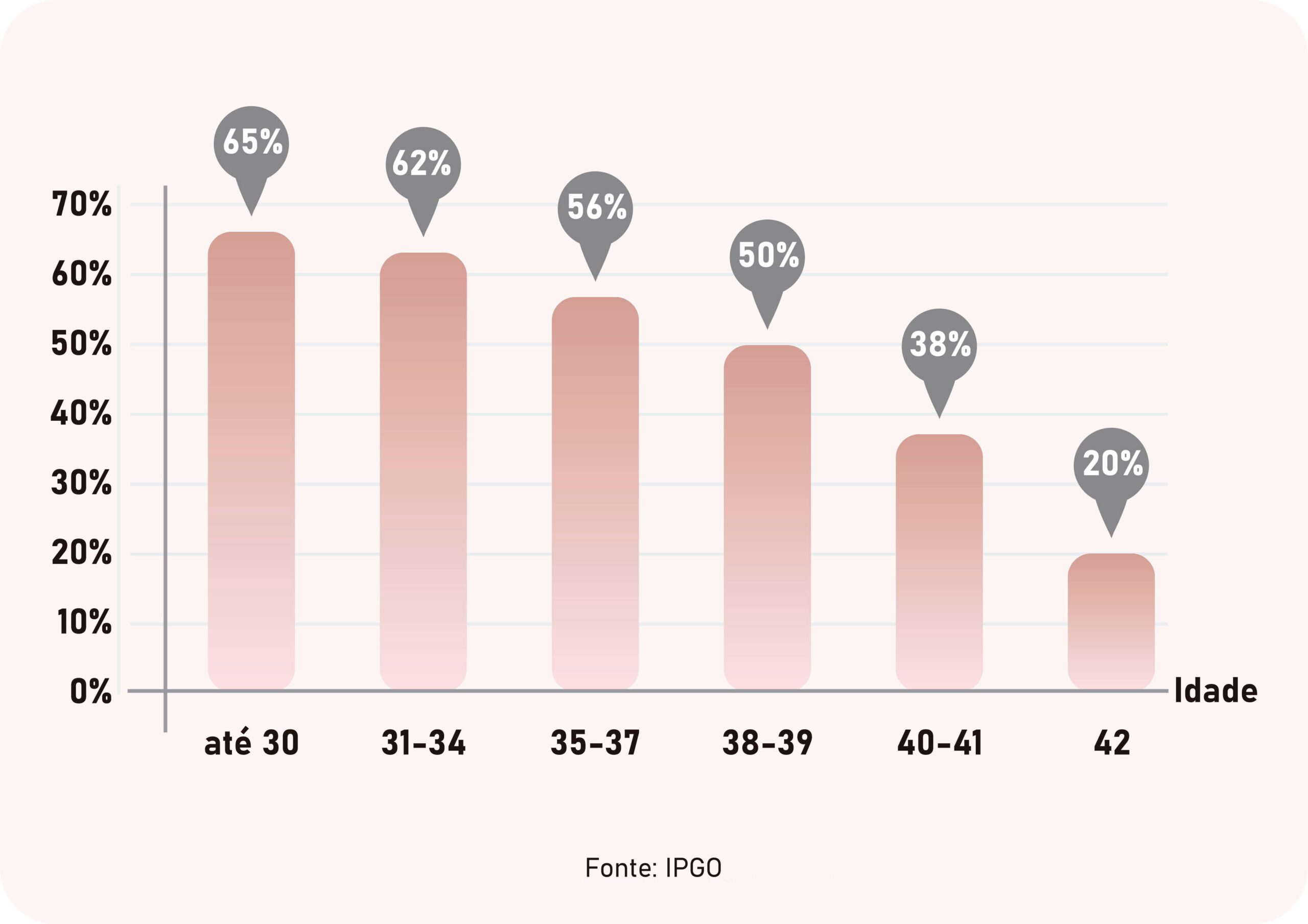
Entretanto, mesmo quando todos os parâmetros são favoráveis, ainda há chance de insucesso. A idade da mulher é o maior preditor de sucesso da FIV, caindo progressivamente com o avançar da idade. Enquanto mulheres abaixo dos 35 anos têm taxa de gravidez de mais de 60% em ciclos de FIV, essa taxa cai pra menos de 20% nas maiores de 40 anos.
TAXA DE GRAVIDEZ POR TRANSFERÊNCIA EMBRIONÁRIA DE ACORDO COM A IDADE MATERNA
Os dados apresentados acima são as taxas de gravidez por transferência, ou seja, as taxas de sucesso quando se tem pelo menos um embrião para transferência. Entretanto existem casos em que não há óvulos ou eles não conseguem ser fertilizados ou formam-se embriões mas estes param de crescer antes que possam ser transferidos. As chances de não ter embriões também aumenta progressivamente com a idade.
Importante ressaltar que quando falamos da idade mulher interferindo nas chances de sucesso, estamos falando da idade do óvulo. A idade de quem receberá os embriões não interfere nas chances de sucesso.
Complicações da FIV
As complicações da FIV são incomuns e em geral não são graves, mas em uma pequena parcela de casos, podem se complicar e levar até a óbito. Essas complicações podem ser divididas em 3 grupos:
Complicações agudas decorrentes da estimulação ovariana
O ovário pode responder demais e levar à Síndrome de Hiperestimulação Ovariana (SHO). Casos leves têm frequência de até 20%, moderados de 3-6% e, em sua forma mais severa, ocorre entre 0,5 a 2% dos ciclos de estimulação ovariana. Atualmente, a SHO tem diminuído de frequência através do uso de novos protocolos.
Complicações decorrentes da coleta de óvulos
- Lesão da artéria ilíaca: muito raro, pode levar à laparotomia de urgência, com grande chance de complicações sérias;
- Sangramento ovariano após punção: também infrequente (0,5% dos casos), mas pode necessitar internação para observação e até abordagem cirúrgica para cauterização;
- Infecção pós-punção: descrito em cerca de 0,3% dos casos, necessitando em casos mais graves de tratamento antibiótico e até cirúrgico
Complicações obstétricas
- Gravidez múltipla: a taxa de gemelaridade chega até 20% das gravidezes de FIV;
- Prematuridade e baixo peso ao nascer: bebês de FIV/ICSI tem até 2 x mais risco de restrição de crescimento, baixo peso ao nascer e parto prematuro.
Casais homoafetivos masculinos
Para os casais homoafetivos masculinos, o sonho da paternidade é um pouco mais complicado, mas sim, possível. É mais difícil primeiramente porque sempre deve ser por fertilização in vitro (FIV) utilizando óvulos doados. Além disso, a posterior gestação necessitará ser em útero de substituição.
O primeiro passo é que o casal selecione uma doadora de óvulos anônima. Nesse caso, a doação de óvulo segue as normas normais estabelecidas pela Resolução do CFM, ou seja: a doação nunca terá caráter lucrativo ou comercial e os doadores não devem conhecer a identidade dos receptores e vice-versa.
No caso da doação temporária de útero, o CFM estabelece que “as doadoras temporárias do útero devem pertencer à família de um dos parceiros num parentesco consanguíneo até o quarto grau (primeiro grau – mãe/ filha; segundo grau – irmã/ avó; terceiro grau – tia/sobrinha; quarto grau – prima), que ceda o seu útero para a gestação dos embriões. Em todos os casos respeitada a idade limite de até 50 anos. Também não pode haver caráter lucrativo nem comercial.
A última etapa consiste na escolha de quem coletará os espermatozoides.
Assim, resumidamente, é realizado o procedimento de fertilização in vitro, no qual o óvulo doado anonimamente é fertilizado em laboratório, com os gametas masculinos coletados de um dos parceiros e, depois do desenvolvimento inicial, os embriões são implantados no útero de substituição e, dessa forma, a gestão acontece. É possível que parte dos óvulos seja fertilizada com sêmen de um dos homens do casal e a outra parte dos óvulos com o sêmen do parceiro, formando embriões de ambos e, então, transferindo um embrião de cada ao útero.
A doadora de óvulos e a mulher que vai ceder o útero não podem ser a mesma pessoa. A doadora deve ser anônima, enquanto o útero deve ser de alguma parente de até quarto grau.
Consulta e exames importantes preparatórios
Todos os casais homoafetivos masculinos que desejam um tratamento de reprodução assistida devem procurar um centro especializado em reprodução assistida para avaliação. Nesta consulta será explicado todo o processo necessário para o tratamento, assim como as chances de sucesso e limitações.
Além de explicar todo o processo, o doador do sêmen deverá passar por uma avaliação da fertilidade através do exame de espermograma. É importante também que mulher que irá gestar para o casal também passe em consulta e por uma avaliação médica e ginecológica.
Espermograma: avaliação mínima do homem
O espermograma é o exame inicial, o mais importante e o principal parâmetro para avaliar a fertilidade masculina, embora não seja o único, nem definitivo, pois, em condições ideais, os resultados podem ser variáveis, ora melhor, ora pior. Por isso, nem sempre um único exame garante a conclusão do resultado, sendo necessária, em alguns casos, a repetição por mais uma ou duas vezes, em intervalos de pelo menos 15 dias. O laboratório escolhido para este exame deve ser de excelência e seguir todas as recomendações internacionais de análise do sêmen. Caso contrário, o exame poderá ser incompleto e inconclusivo, e repercutirá negativamente na avaliação do homem. O sêmen é obtido por masturbação e o homem precisa estar com no mínino dois e no máximo cinco dias de abstinência sexual. Períodos inferiores a um dia ou superior a cinco não são recomendados.
Segue a lista de exames solicitados além do espermograma:
- Hemograma completo e tipagem sanguínea;
- Sorologias: hepatite B, hepatite C, toxoplasmose, citomegalovírus, sífilis, HIV 1 e 2, HTLV 1 e 2, Zika Vírus – IgM e, atualmente, sarampo;
- Outros exames podem ser solicitados em situações especiais e de forma individualizada: ultrassom de bolsa escrotal, cariótipo com Banda G (avalia os cromossomos do paciente), perfil metabólico (colesterol, triglicérides e outros), hormônios (FSH, LH, testosterona total e livre, estradiol, TSH, T4 livre e prolactina), entre outros.
Doadoras de óvulos
A doação de óvulos é realizada no Brasil pelo IPGO há mais de 15 anos. É ética e legal, contanto que não haja fins comerciais e seja anônima. Portanto, a doadora não saberá a identidade do casal receptor e vice-versa – é o que determina a lei e a ética. Chamamos de doadora a mulher que será estimulada para um ciclo de FIV, do qual resultará a coleta de vários óvulos que serão doados, na sua totalidade (doação exclusiva) ou metade deles (doação compartilhada), para outro casal, sendo os embriões transferidos ao útero de outra mulher (no caso de casais homoafetivos masculinos, para a barriga solidária).
Avaliando e selecionando as pacientes doadoras
No Brasil a ovodoação é obrigatoriamente anônima, ou seja, nem a doadora nem a receptora sabem a identidade de uma ou de outra, diferente dos Estados Unidos, onde o casal pode escolher uma doadora conhecida. É muito comum o casal pedir para que a irmã ou parente de um deles doe o óvulo para ser fertilizado com o sêmen do parceiro, tendo a criança, então, características da família dos dois membros do casal. ISSO NÃO É PERMITIDO NO BRASIL! No Brasil também não é permitida nenhuma transação comercial neste tipo de tratamento. A doação deve ser voluntária e sem fins lucrativos. Segundo a Resolução CFM nº 2.168/2017, é permitida a chamada doação compartilhada, isto é, uma mulher, em tratamento para engravidar, pode doar parte dos seus óvulos, em troca do custeio de parte do tratamento.
Por essa resolução, a idade limite para ser doadora é 35 anos. No IPGO, a candidata a doadora, além de um exame clínico e laboratorial rigoroso, deve preencher um questionário detalhado sobre sua vida pessoal e médica incluindo detalhes sobre antecedentes e características familiares. Detalhes físicos como peso, estatura, tipo e cor dos cabelos, cor dos olhos e da pele são incluídos neste questionário, acompanhados de uma foto de quando era criança para que o casal tenha uma ideia da fisionomia de quem lhe doará os óvulos.
Solicitamos também que escrevam um pequeno texto que reflita os seus sentimentos e traços da sua personalidade que darão maior ênfase às suas características íntimas. Hábitos como tabagismo, alcoolismo e uso de drogas devem ser questionados. As doadoras não são buscadas ao acaso, na maioria das vezes, elas estão fazendo também um tratamento para engravidar (doação compartilhada) em decorrência de problemas de fertilidade do marido (poucos espermatozoides ou ausência deles), fatores tubários ou esterilidade sem causa aparente, sendo, independente da razão sempre submetidas a exames para a pesquisa da fertilidade, principalmente da reserva ovariana. Todas as sorologias como sífilis, HIV, hepatite B e C, HTLV 1 e 2, pesquisa de secreção vaginal e Papanicolau devem ter sido realizadas há menos de 6 meses, além de tipagem sanguínea, cariótipo para descartar translocações balanceadas e avaliação rigorosa da reserva ovariana. Além disso, exame de Zika Vírus – IgM deve ser colhido no prazo de menos de um mês antes da coleta.
Dessa forma, para ser doadora, a mulher deve ter as seguintes características:
- Idade entre 18 e 35 anos;
- Bom nível intelectual;
- Histórico negativo de doenças genéticas transmissíveis;
- Teste negativo para doenças infecciosas sexualmente transmissíveis;
- Boa reserva ovariana
Como o casal escolhe a doadora?
Quando se utiliza óvulos doados, há, primeiramente, duas possibilidades de escolha:
- óvulos vitrificados: a doadora já foi submetida ao processo de estimulação ovariana e coleta de óvulos que foram, então, congelados. Tem a vantagem de saber já quantos óvulos estão disponíveis.
- óvulos frescos: neste caso, as doadoras estão aguardando para iniciar o tratamento que deverá ser realizado simultâneo ao preparo da mulher que ira gestar. Tem a vantagem dos óvulos serem frescos, mas a desvantagem de não sabermos exatamente quantos óvulos a doadora terá.
Em termos de chances de sucesso, atualmente, as taxas estão praticamente iguais comparando óvulos frescos e congelados.
O casal terá acesso ao questionário com todas as características físicas da doadora e uma foto dela quando criança.
As doadoras devem ter entre 18 e 35 anos de idade. Quanto mais velha a doadora menor a chance de gravidez da receptora devido à diminuição natural da chance de engravidar em função do aumento da idade materna.
O IPGO trabalha com ovodoação de maneira intensa e não tem, sequer, uma lista de espera para que os casais interessados consigam a doadora compatível com o que desejam. O IPGO tem doadoras compatíveis para todos os tipos de sangue e praticamente todos os tipos físicos, além de um programa intenso para incentivo a doação de óvulos. Mas pode haver algum tempo de espera para encontrar uma doadora compatível visto que algumas etnias são mais raras dependendo da região do país como, por exemplo, a negra e oriental.
Quem são as doadoras?
- Pacientes do programa de fertilização in vitro ou inseminação artificial com altas respostas ao estímulo ovariano, às vezes, desejam de forma voluntária e anônima doar parte dos óvulos obtidos ou embriões excedentes;
- Doação compartilhada: É a situação mais comum. Neste caso, a receptora recebe os óvulos doados de uma paciente submetida à FIV que doa parte de seus óvulos em troca do custeio de parte do seu tratamento. Desta forma, o casal e a doadora estão se ajudando mutuamente.
- Óvulos e embriões congelados provenientes de mulheres submetidas à tratamentos de FIV que engravidaram e tiveram seu(s) filho(s). De alguma forma, o sucesso do tratamento já realizado indica uma boa qualidade destes óvulos. Estas pacientes, quando não desejam ter mais filhos, muitas vezes doam os óvulos ou embriões excedentes. Vale ressaltar que a doação de óvulos é muito mais fácil de ser aceita pela paciente em relação à doação de embriões.
- Doação por generosidade pura: Algumas mulheres de maneira altruística ou já beneficiadas por tratamentos anteriores de FIV, não desejando mais ter filhos e movidas por um sentimento de gratidão, se oferecem para doar seus óvulos sem qualquer benefício.
- Cada clinica deve manter um registro de todas as doadoras e receptoras bem como dos resultados de cada tratamento, de preferência até o nascimento dos bebês. Além de serem confidenciais, a confiabilidade dos arquivos médicos deve ser respeitada como qualquer outro. A liberação de informações só poderá ser feita mediante autorização expressa do paciente.
Útero de substituição (barriga solidária)
Como dito, segundo o CFM, a mulher que será a barriga solidária deverá ser parente de até quarto grau de um dos membros casal (mãe, filha, irmã, avó, tia, sobrinha ou prima). Em todos os casos respeitada a idade limite de até 50 anos. Também não pode haver caráter lucrativo nem comercial.
Há situações em que o casal não possui uma pessoa com ligações consanguíneas para ceder seu útero para gestação. Isso ocorrendo, o caso é enviado ao Conselho Federal de Medicina para uma avaliação da possibilidade de realização do tratamento. Em outros países há mais possibilidades, pois se pode pagar a uma mulher pelo “aluguel” do seu útero ou comprar óvulos. Porém, essas opções continuam proibidas no Brasil.
A mulher que irá gestar deve passar em consulta onde serão explicados os procedimentos necessários, implicações e riscos. Além disso, deve passar por uma avalição clínica e ginecológica, além de uma avaliação psicológica.
Exames necessários:
- Citologia oncótica (Papanicolau)
- Exame de secreção vaginal: bacteroscopia e cultura, culturas para micoplasma / ureaplasma, Neisseria gonorrhoeae e pesquisa de clamídia por PCR.
- Sorologias: hepatite B, hepatite C, sífilis, HIV 1 e 2 e HTLV 1 e 2, rubéola, toxoplasmose, citomegalovírus, Zika vírus – IgM e, atualmente, sarampo
- Hormônios: TSH, T4 livre e prolactina.
- Ultrassom transvaginal
- exames clínicos gerais: Tipagem sanguínea, hemograma completo, coagulograma, vitamina D, colesterol e frações, triglicérides, glicemia de jejum. Dependendo da idade e antecedentes, avaliação clínica mais completa com ECG, ecocardio, etc.
- Outros exames podem ser solicitados de forma individualizada: trombofilias, anticorpos, ressonância nuclear magnética de pelve ou ultrassom transvaginal com preparo intestinal para pesquisa de endometriose/adenomiose, vídeo-histeroscopia e biópsia do endométrio, mamografia e /ou ultrassom de mamas.
- Avaliação psicológica
Nós, do IPGO, encaminhamos o consentimento informado a ser preenchido por todos os envolvidos, relatório médico e psicológico atestando adequação clínica e emocional da doadora temporária do útero e recomendação da participação de outros profissionais, como, por exemplo, psicóloga, assistente social e advogado, até processos burocráticos para autorização do Conselho Regional de Medicina, quando necessário.
Como é feita a FIV em casais homoafetivos masculinos?
1- Sincronizando a doadora e útero de substituição
Se formos utilizar óvulos frescos, é necessário sincronizar o ciclo da doadora com a dona do útero. Existem vários protocolos que podemos utilizar para sincronizar as duas como, por exemplo, os análogos do GnRh, o uso de pílulas anticoncepcionais ou o uso concomitante de análogos e antagonistas de GnRh. O importante é fazer com que as duas possam iniciar juntas o tratamento. A doadora iniciará com injeções para estimular a ovulação enquanto a receptora iniciará com medicações via oral para preparar o útero para receber o embrião.
No caso de óvulos congelados, o preparo do útero pode se iniciar no início do ciclo que desejarem.
2- Tratamento da doadora
O ciclo de doação de óvulos é realizado pela técnica de Fertilização in vitro já descritos anteriormente neste e-book (vide Fertilização in vitro (FIV)). A doadora é submetida a estimulação ovariana usual para um ciclo de FIV. Se forem utilizar óvulos frescos, no dia da coleta, o homem que irá fornecer o sêmen deve colher uma amostra por masturbação no mesmo laboratório que os óvulos foram coletados e os óvulos maduros serão submetidos ao processo de fertilização (ICSI).
Quando o processo for realizado pela doação compartilhada, metade dos óvulos serão fertilizados com os espermatozoides do marido da doadora e a outra metade com os espermatozoides do casal receptor. Se houver número impar de óvulos, a doadora fica com um óvulos a mais.
3- Tratamento da barriga solidária
O preparo do endométrio é idêntico ao descrito para casais homoafetivos femininos ( vide Preparo do endométrio para receber os embriões).
Inicia-se o preparo com estradiol e, no dia da coleta dos óvulos da doadora, a receptora iniciará o uso da progesterona a noite, desde que seu endométrio esteja adequado (pelo menos maior que 7 mm, de aspecto trilaminar). Se não estiver adequado, vale a pena congelar os embriões e aguardar que esteja favorável.
Se os óvulos já estiverem congelados, o preparo do endométrio pode ser feito com ciclo natural ou com estradiol. Neste caso, no dia da ovulação (se ciclo natural) ou quando endométrio estiver adequado (após pelo menos 10 dias de estradiol), os óvulos são descongelados e fertilizados com o sêmen coletado de um dos membros do casal. Neste dia, a barriga solidária inicia uso de progesterona e os embriões são transferidos ao seu útero de 3 a 5 dias após.
Se os óvulos já estiverem congelados, o preparo do endométrio pode ser feito com ciclo natural ou com estradiol. Neste caso, no dia da ovulação (se ciclo natural) ou quando endométrio estiver adequado (após pelo menos 10 dias de estradiol), os óvulos são descongelados e fertilizados com o sêmen coletado de um dos membros do casal. Neste dia, a barriga solidária inicia uso de progesterona e os embriões são transferidos ao seu útero de 3 a 5 dias após.
O procedimento da transferência e suporte hormonal também é o mesmo já descrito neste ebook ( A transferência do(s) embrião(ões) para o útero e 6ª Fase – Suporte hormonal).
Em relação ao número de embriões transferidos, considerando que as doadoras de óvulos tem menos de 35 anos, pode-se transferir no máximo 2 embriões!!!!
O teste de gravidez é realizado de 10 a 12 dias após a transferência embrionária, o caso de beta-hCG positivo, a reposição hormonal (estradiol e progesterona) deverão ser mantidas até 12 semanas.
4- Coleta de sêmen em situações especiais
Mesmo que o homem tenha uma alteração seminal importante, a maioria dos casos pode ser resolvida com a FIV associada à ICSI. Com ela, são necessária quantidades mínimas de espermatozoides. Entretanto, nos casos de azoospermia, ou seja, ausência de espermatozoides no ejaculado, podem ser necessárias técnicas mais avançadas para recuperação dos espermatozoides. Nestes casos, os espermatozoides são recuperados diretamente do testículo (ou do epidídimo) e, através de ICSI, os óvulos são fertilizados. As principais técnicas são:
PESA (Aspiração Percutânea de Espermatozoides do Epidídimo): aspira-se uma pequena quantidade de sêmen do epidídimo, um estrutura que fica atrás do testículo e armazena os espermatozoides.
TESA (Aspiração de Espermatozoides do Testículo): é uma técnica similar, na qual os espermatozoides são retirados por uma minúscula biópsia de tecido testicular.
MicroTESE (microdissecção testicular): é uma microcirurgia que possibilita a retirada dos espermatozoides diretamente dos ductos seminíferos, que é o local onde eles estão em maior concentração.
Biópsia embrionária estudo genético (PGT-A, PGT-M e PGT-SR)
Pacientes submetidas à FIV tem a opção de realizar uma biópsia embrionária antes da transferência para excluir algumas doenças de origem genética.
O que é biópsia embrionária (PGT)?
Biopsia embrionária (Trofectoderma): é um procedimento de retirada de células do embrião (trofectoderma: células que vão originar as estruturas da placenta) para análise genética ou cromossômica. É muito importante que a biópsia seja realizada de maneira correta para que não comprometa o desenvolvimento do embrião no futuro. Essas células, então, poderão ser submetidas às seguintes análises:
PGS (Pré-implantation Genetic Screening) (em português, Triagem Genético PréImplantacional): atualmente denominado PGT-A (Preimplantation Genetic TestingAneuplody) é um exame realizado no embrião antes da implantação no útero, com o objetivo de diagnosticar a existência de alguma doença cromossômica. Essa avaliação estuda os 24 cromossomos do corpo humano (22 pares de cromossomos autossomos denominados com números de 1 a 22 e mais dois sexuais X e Y). Essas técnicas são capazes de identificar todas as anomalias cromossômicas chamadas aneuploidias, que são alterações de perdas ou ganhos no número de cromossomos, causados por erros na divisão celular. Os embriões gerados com cromossomos a mais ou a menos não conseguem se desenvolver normalmente, e são a principal causa de falhas reprodutivas. Entre as aneuploidias mais conhecidas estão as síndromes de Down, Patau, Edwards, Klinenfeter e Turner. As técnicas detectam alterações envolvendo todos os 24 cromossomos e são realizadas em uma fase adiantada de evolução embrionária, o blastocisto, geralmente no quinto dia após a fecundação (120 horas), o que permite avaliar um número maior de células (de 6 a 10) e, consequentemente, obter um resultado mais preciso. A retirada das células embrionárias ocorre após a realização de uma pequena abertura na região externa do blastocisto, chamada de trofectoderma. Algumas células que se exteriorizam Biópsia embrionária estudo genético (PGT-A, PGT-M e PGT-SR) por essa abertura são delicadamente aspiradas e encaminhadas ao laboratório de genética. Os embriões saudáveis são transferidos para o útero. Essa avaliação pode aumentar a chance de sucesso do tratamento. Para facilitar o entendimento, padronizou-se nomear o exame PGT-A (teste genético pré-implantacional para aneuploidia).
PGT-M ou PGD: preimplantation genetic diagnosis (ou diagnóstico genético pré-implantacional). Nele, a biópsia avalia doenças genéticas causadas por genes específicos. Hoje é chamado de PGT-M – preimplantation genetic testing for monogenic/single gene diseases (ou teste genético pré-implantacional para desordens monogênicas – gene único).
Time-lapse Um avanço tecnológico que pode melhorar os resultados
Time-Lapse (EmbryoScope® Plus) é uma incubadora (local é onde os embriões se desenvolvem no período em que estão no laboratório, antes de serem transferidos para o útero), que difere das outras por possuir uma câmera de vídeo acoplada ao sistema, que permite fazer vídeos do desenvolvimento dos embriões e melhorar o acompanhamento da fertilização até a transferência para o útero da mulher. Isto tem um efeito muito positivo na escolha do melhor blastocisto e, provavelmente, nos melhores resultados. As pacientes poderão até receber um vídeo sobre o desenvolvimento de seus embriões. A reprodução assistida está avançando muito, especialmente no campo tecnológico, já que as clínicas não param de incorporar novos elementos a seus laboratórios para alcançar o objetivo final perseguido: um bebê saudável em casa. Uns dos avanços mais marcantes nos últimos anos a este respeito são as incubadoras com tecnologia Time-Lapse, cuja câmera permite ver a evolução dos embriões sem ter que removê-los da incubadora para o check-up.
As vantagens dessas incubadoras sobre as convencionais são notáveis, já que seu sofisticado sistema de captura de imagens permite registrar mudanças no desenvolvimento embrionário as quais, com as incubadoras convencionais, podem passar despercebidas. A incubadora Time-Lapse possui vários compartimentos separados fisicamente onde os embriões são introduzidos, cada um com uma câmera que apreende imagens a cada 10 minutos. A incubadora possui um software que converte todas essas imagens em um vídeo, por meio do qual as pacientes podem ver os primeiros dias de desenvolvimento dos embriões concentrados em poucos minutos. Graças a este sistema, os embriologistas podem ter informações sobre os embriões que estão em cultivo no laboratório, o que lhes permite melhor seleção daqueles com maiores possibilidades de implantação.
Desta forma, a cultura até o estágio de blastocisto dos embriões ocorre sob condições estáveis de temperatura e umidade, CO2 e baixa concentração de oxigênio, como aconteceria em condições normais no corpo de uma mulher. Em geral, qualquer paciente em tratamento de fertilização in vitro poderia usar este tipo Time-lapse Um avanço tecnológico que pode melhorar os resultados de incubadora, mas ela é especialmente indicada para casais que passaram por processos anteriores fracassados ou por casais que desejam apenas transferir um único embrião.
Porque os tratamentos de FIV podem falhar
Os motivos que podem levar ao insucesso dos tratamentos de FIV devem ser investigados, de preferência antes mesmo do início do tratamento e devem ser individualizadas para cada caso. As razões, de um modo geral, são uterinas, endometriais, trombofilias e imunológicas, entre outras que, por serem muitas, estão descritas no site do IPGO e no e-book “Como aumentar as chances de sucesso nos tratamentos de fertilização?”, que pode ser baixado neste link: https://ipgo.com.br/e-books/.
Este texto foi extraído do e-book “OS TRATAMENTOS DE FERTILIZAÇÃO EM CASAIS HOMOAFETIVOS”.
Faça o download gratuitamente do e-book completo clicando no botão abaixo: