Abortos de repetição
A definição de aborto é a perda fetal antes de 22 semanas de gestação ou a perda de um feto com peso inferior a 500 g. O aborto espontâneo é uma fatalidade comum que acomete de 15% a 25% das mulheres que engravidam. É considerado uma das maiores frustrações da vida reprodutiva de um casal. Mesmo sendo um fato bastante comum nas gestações iniciais, deve merecer um tratamento médico específico e, muitas vezes, um acompanhamento psicológico.
Abortamento de repetição (AR) é classicamente definido como a ocorrência de três abortos consecutivos, e sua prevalência está em torno de 1%-5%. Entretanto, muitos pesquisadores atualmente têm mudado essa definição para duas ou mais perdas sequenciais. Assim, ainda que do ponto de vista acadêmico, a pesquisa mais detalhada para os abortos repetidos deve ser feita depois de três perdas fetais, ela pode ser iniciada após o segundo ou, em casos especiais, após o primeiro aborto. Os AR representam um trauma na vida do casal e, por isso, devem ser vistos com seriedade, caso contrário, a alegria e expectativa positiva pelo filho que virá, sentida nos primeiros dias do atraso menstrual, poderão frustrar e causar uma decepção imensurável. Portanto, todas as alterações que justifiquem as causas de abortos, mesmo as pouco prováveis, devem ser investigadas.
As causas de abortamento são variadas, podendo inserir-se nas estatísticas normal de perda, natural do ser humano e comum a todas as mulheres, principalmente devido à idade. Mas, ainda assim, mesmo aquelas que já tiveram filhos, mas perderam um bebê sem causa justificada, podem ter problemas específicos que devem ser investigados.
ESSE É UM CONTEÚDO EXTENSO PARA QUE VOCÊ TENHA TODOS OS DETALHES QUE FAZEM A DIFERENÇA!
Índice
ToggleFatores de Risco para abortos
E xistem alguns fatores que aumentam o risco de aborto e devem ser levados em conta na investigação.
Entre eles:
Idade da mulher
para formação do óvulo, as células sofrem um processo de meiose, ou seja, passam de uma célula de 46 cromossomos para uma célula de 23 cromossomos (que receberão 23 cromossomos do espermatozoide para formar um embrião com 46 cromossomos). Como os óvulos não se renovam, quanto maior a idade da mulher, mais velho é o óvulo que está sofrendo a meiose, sendo mais sujeito a erros que levam à formação de óocitos aneuploides (com alterações cromossômicas). Como consequência, ao serem fertilizados, gerarão embriões aneuploides, que frequentemente evoluem para aborto. Portanto, em mulheres com idade avançada, é esperado que uma parcela de gestações acabe em aborto, sem outra causa associada (Quadro 1).
Quadro 1. Idade materna x risco de aborto
Pode-se observar que, até os 34 anos, há pouca variação no risco de aborto, aumentando progressivamente após essa idade, coincidindo com a queda natural da fertilidade da mulher.
Idade paterna
a idade paterna não tem uma influência tão importante como a materna na ocorrência de aborto, mas também pode aumentar o risco. Enquanto a idade materna maior que 35 anos já é um fator de risco isolado, independentemente da idade paterna, a idade paterna maior que 40 anos pode aumentar o risco em mulheres já acima dos 30 anos (em três vezes mais), e ainda mais se acima dos 35 (em mais de seis vezes), em comparação a casais em que os dois têm menos de 30 anos.
Antecedente de aborto
como abortos são frequentes, já ter tido um anteriormente muda muito pouco o risco de um novo. Mas a partir de dois, esse risco já se mostra aumentado, independentemente da idade. Estudos demonstraram que mulheres entre 20-29 anos, sem gravidezes prévias, tiveram 8% de risco de um aborto espontâneo. As com um aborto prévio, tiveram 12% de risco. Com dois abortos, o risco subiu para 22,7%, e com três abortos prévios, para 44,6%. Por isso, apesar de academicamente serem necessários três abortos para se definir o quadro como aborto de repetição, muitos serviços já iniciam a investigação a partir do segundo.
Fatores externos
alguns hábitos podem interferir na chance de aborto, como o álcool (mais de cinco doses por semana), cafeína (> 300 mg/dia, equivalente a três xícaras de café), cigarro (principalmente se mais de 20 cigarros/dia) e drogas. Em relação ao peso, mulheres obesas (IMC > 30) ou com baixo peso (IMC < 18,5) também apresentam risco aumentado. A mulher deve ser orientada a corrigir esses fatores antes da gestação, independentemente do antecedente de aborto. Suplementação de ácido fólico também deve ser sempre recomendada.
Causas de abortos de Repetição
E studos sempre mostraram que, em cerca de 50%-75% dos AR, não se identificava a causa, sendo consenso que em mais da metade dos casais, a causa dos AR permanecia indeterminada. Pesquisas mais recentes, no entanto, com análise genética dos produtos de aborto, mostraram que, em pelo menos 40% deles, havia alterações genéticas no embrião, reduzindo o número de AR de causa indeterminada para cerca de 25% (Figura 1).
As principais causas identificáveis são:
- Alterações cromossômicas e genéticas
- Alterações anatômicas
- Trombofilias
- Alterações endocrinometabólicas
- Infecções
- Fator masculino
- Causas imunológicas
- Intolerância ao glúten
- Abortos recorrentes sem explicação
- Aborto na FIV
Figura 1: Causas de abortos de repetição

Alterações cromossômicas e genéticas
Cerca de 60%-70% dos abortos espontâneos isolados são cromossomicamente alterados, e aumentam quanto maior a idade da mulher. Em AR, a prevalência de alterações genéticas no embrião é menor (até 45%).
As alterações genéticas mais comuns nos produtos de aborto são duplicações ou perda de algum cromossomo ou de parte dele. Um exame cariótipo do produto de aborto pode definir se essa foi realmente a causa, mas, apesar de serem muito frequentes nas perdas gestacionais iniciais, na maioria dos casos, essas alterações ocorrem ao acaso. Investigação dos pais com cariótipo com banda G também deve ser feita em casais com AR, mas somente 2% a 10% deles apresentarão alguma alteração. As alterações mais comuns nos pais são as translocações recíprocas (quando ocorre uma troca de material entre cromossomos não-homólogos), translocações robertsonianas (quando dois cromossomos acrocêntricos se fundem próximos da região do centrômero, com perda de seus braços curtos) e inversões (quando em um mesmo cromossomo ocorrem duas quebras, sendo que logo em seguida os fragmentos são restaurados, porém, em posição inversa, ou seja, há uma modificação na ordem dos nucleotídeos). Os pais são fenotipicamente normais, mas na meiose há risco aumentado de formar gametas com alterações não balanceadas (perda ou acréscimo de material genético).
Casais com AR e cariótipo alterado têm risco de mais de 70% de novo aborto por aneuploidia e 1% de chance de filho vivo com alteração cromossômica. Por isso, nesses casos, deve ser oferecido o diagnóstico genético pré-implantacional (PGS), realizado num ciclo de fertilização in vitro. Um estudo demonstrou que essa conduta não mudou o número de partos de nascidos vivos em relação a uma nova tentativa de gravidez sem intervenção (35% e 42%, respectivamente), mas diminuiu muito a chance de aborto (9% contra 28%).
Alterações anatômicas
As principais alterações anatômicas relacionadas a AR são as malformações mullerianas (septo uterino, útero bicorno, unicorno e didelfo), miomas, pólipos e sinéquias uterinas. Para diagnóstico, recomenda-se ultrassom transvaginal e histeroscopia. Entretanto, muitas vezes é necessário complementar com ressonância nuclear magnética (RNM) de pelve, ultrassom 3D ou laparoscopia associada a histeroscopia para diferenciar septo de útero bicorno.
Malformação mulleriana (Malformações do útero)
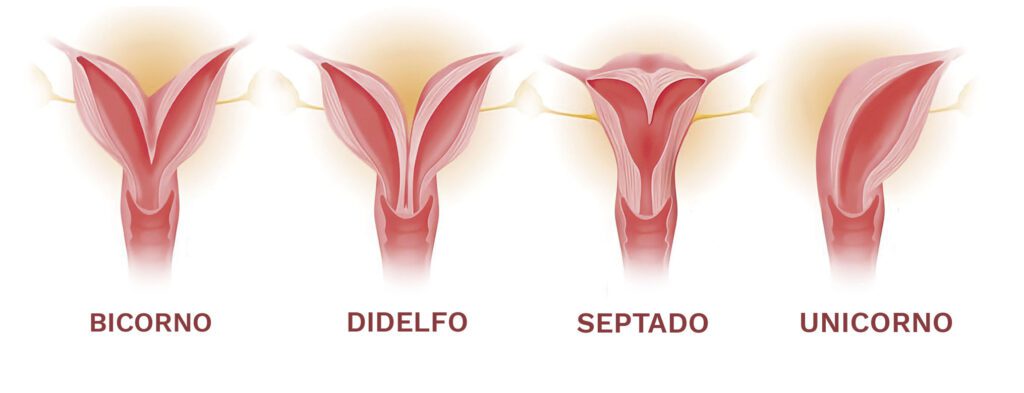
Apresenta prevalência muito variável na literatura médica, mas, enquanto na população geral está em torno de 3-5%, em pacientes com AR são encontradas em 7%-13%, sendo as mais frequentes útero bicorno e septo uterino. Pacientes com essas malformações têm risco aumentado para novo aborto. Uma revisão da literatura mostrou que a incidência de abortos foi de 44% para mulheres com septo uterino e cerca de 36% para útero unicorno, bicorno e didelfo (Figura 2).
Feito o diagnóstico de septo uterino, é recomendada a ressecção histeroscópica, que diminui a chance de novo aborto para em torno de 16% (compatível com a perda normal esperada para qualquer casal). Outras malformações envolvem cirurgias mais complexas e de resultados controversos, sendo necessário avaliar cada caso individualmente.
Figura 2: Malformações Uterinas
Miomas
A frequência de miomas em pacientes com AR está em torno de 5%-8%, mas nem sempre está relacionada com a causa do aborto. Esse tema é controverso na literatura, mas é consenso que miomas submucosos ou que distorcem a cavidade podem aumentar o risco de abortos. Nesse caso, a miomectomia pode melhorar as taxas de nascidos-vivos.
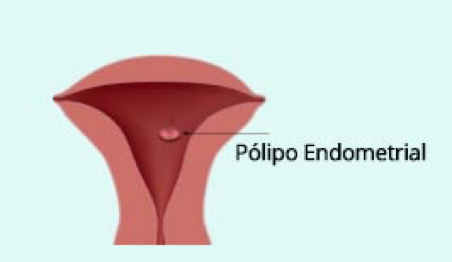
Pólipos endometriais
Não são frequentes em AR, mas podem estar associados a um maior risco de aborto e devem ser retirados, principalmente se maiores de 1 cm.
Sinéquias
Aderências intrauterinas decorrentes de cirurgias uterinas ou endometrite podem estar relacionadas à infertilidade e AR. Na presença dela, recomenda-se ressecção histeroscópica.

Os problemas imunológicos têm sido responsabilizados por alguns casos de insucesso na fertilização in vitro e por abortos de repetição. Alguns autores acreditam que muitos casos de falha são, na verdade, abortos muito precoces que, após um período curto de implantação embrionária, não chegam a ser detectados nos testes de gravidez, não evoluem e são eliminados. Existem controvérsias a respeito desse tema.
Trombofilias
São doenças pouco frequentes e que provocam alterações de coagulação do sangue. Estas alterações não são detectadas em exames de sangue comuns e, quando existem, aumentam a chance de formar coágulos sanguíneos e causar tromboses mínimas capazes de impedir a implantação do embrião ou provocar abortos. Os exames para esta pesquisa são feitos por coleta de sangue em laboratórios especializados e sempre com indicação médica. Entre elas estão:
Síndrome do Anticorpo Antifosfolípede (SAAF)
É caracterizada pela associação de anticorpos antifosfolípedes com complicações obstétricas ou trombose. É a principal causa tratável de AR, presente em até 15% das pacientes, contra 2% de frequência em mulheres em geral. O mecanismo patológico que leva ao aborto se deve à inibição da função e diferenciação trofoblástica, à ativação da via do complemento na interface maternofetal levando a processo inflamatório e, tardiamente, à trombose dos vasos placentários.
*Embora em termos acadêmicos se definir como SAAF seja recomendável ter pelo menos um critério clínico e um laboratorial, o IPGO não recomenda que todas as etapas descritas a seguir sejam cumpridas para que se inicie a pesquisa:
Critérios clínicos:
- Trombose vascular (um ou mais episódios): arterial, venoso ou pequenos vasos;
- Complicações obstétricas:
• morte inexplicada de feto normal após dez semanas de gestação;
• parto prematuro antes de 34 semanas devido a pré-eclâmpsia, eclâmpsia ou insuficiência placentária;
• três ou mais abortos espontâneos consecutivos inexplicáveis antes de dez semanas de gestação.
Critérios laboratoriais:
- anticorpo anticardiolipina (aCL) (IgM e/ou IgG): presente no sangue em níveis moderados ou altos por teste ELISA padronizado*;
- anticoagulante lúpico (AL): detectado no plasma de acordo com as recomendações da Sociedade Internacional de Trombose e Hemostasia*;
- anti-β2glicoproteína I (β2GPI) IgG ou IgM: presente no plasma por teste ELISA padronizado*..
*em pelo menos duas medidas com intervalo de pelo menos 12 semanas.
- livedo reticularis;
- trombocitopenia;
- nefropatia;
- alterações neurológicas;
- IgA aCL e IgA β2GPI;
- anticorpo antifosfatidilserina;
- anticorpo antifosfatidiletolamina
Pacientes com AR e SAAF sempre necessitam de tratamento, uma vez que, quando presente e não tratada na gestação, leva a uma taxa inferior a 10% de nascidos vivos. O tratamento se faz com AAS 100 mg/dia e heparina subcutânea em dose profilática. Pode ser utilizada heparina não fracionada (HNF) 5.000 UI a cada 12 horas ou dose única diária de heparina de baixo peso molecular (HBPM): enoxaparina 40 mg ou dalteparina 5.000 UI. A heparina não só tem o efeito antitrombótico de vasos placentários, como atua na função trofoblástica e via do complemento, também envolvidas na fisiopatologia da doença. Um efeito colateral da terapia com heparina é a plaquetopenia e, portando, a quantidade de plaquetas deve ser monitorada com hemograma. Não há diferença de eficácia clínica entre a HNF e a HBPM, mas a HBPM tem a vantagem de ser dose única diária e provocar, menos frequentemente, plaquetopenia em comparação à HNF. Uso de corticoide não mostra benefício.
Discute-se os casos em que a paciente apresenta alguns critérios para SAAF, mas estes não completam o diagnóstico. Não é consenso, mas na presença de algum dos achados clínico-laboratoriais, mesmo que não completos, o tratamento pode ser instituído, frente à grande morbidade da doença. Nesses casos, pode-se ainda falar a favor do tratamento a presença dos outros achados clínicos e laboratoriais que não são critérios.
Outras trombofilias
Existem outras trombofilias inatas que poderiam estar associadas a AR, embora estejam mais relacionadas com perdas fetais tardias, por trombose dos vasos placentários. São elas:
- fator V de Leiden – mutação G1691A;
- mutação G20210A do gene da protrombina;
- deficiência de Proteína S;
- deficiência de Proteína C;
- antitrombina III;
- mutação C677T e A1298C da Metilenotetrahidrofolato redutase (MTHFR);
- homocisteína;
- antifosfatidilserina;
- Polimorfismo 4G/5G
A relação dessas trombofilias com aborto de repetição ainda é um assunto controverso, assim como a necessidade de heparina nesses casos. Apesar de não ser consenso, existe uma tendência a se tratar pacientes com AR na presença de alguma dessas trombofilias.
Alterações endócrino-metabólicas
Algumas alterações endócrinas podem estar relacionadas a risco aumentado de abortos.
São elas:
Diabetes mellitus (DM)
A prevalência de DM em mulheres com AR é igual à da população geral. Entretanto, mulheres diabéticas com aumento de hemoglobina glicosilada no primeiro trimestre têm maior chance de aborto e malformação fetal. Diabéticas controladas têm risco igual ao da população geral.
Síndrome dos Ovários Policísticos (SOP)
Pacientes com SOP têm risco aumentado para aborto, provavelmente devido à resistência à insulina e à hiperinsulinemia. O uso de sensibilizadores da insulina, como metformina, para diminuir a taxa de aborto tem sido sugerido, entretanto os dados da literatura ainda são controversos.
Hipotireoidismo
Apesar de pacientes com AR não apresentarem maior frequência de hipotireoidismo que mulheres sem história de perda, sabe-se que hipotireoidismo 7. Alterações endócrino-metabólicas descompensado aumenta o risco de aborto. Assim, em pacientes com AR, deve-se sempre pedir TSH, T4 livre e anticorpos antitireoidianos (antitireoglobulina e antiperoxidase).
Como durante a gravidez há uma sobrecarga da glândula tireoide, recomenda-se manter TSH abaixo de 2,5 mlU/l em mulheres com hipotireoidismo em tratamento. O hipotireoidismo subclínico, quando associado a auto anticorpos, deve sempre ser tratado. Não há consenso quanto aos casos de ausência de auto anticorpos, mas a tendência é recomendar o tratamento também.
A presença de auto anticorpos para tireoide tem maior prevalência em mulheres com AR (20%-25%) em comparação às gestantes normais (15%-20%), mas, se o tratamento com levotiroxina apresenta benefício, ainda é algo controverso. Recomenda-se tratar esses casos quando o TSH está acima de 2,5 mlU/l.
Hiperprolactinemia
Pode estar associada a AR por alterar o eixo hipotálamo-hipófise-ovário, resultando em alteração na foliculogênese, maturação oocitária e insuficiência lútea. Dosagem de prolactina e normalização dos níveis quando elevados com agonistas dopaminérgicos podem melhorar os resultados em uma nova gestação.
Insuficiência lútea
Apesar da insuficiência lútea não ser frequente, e estudos demonstrarem que a suplementação de progesterona não diminui o risco de abortos espontâneos isolados, há evidência de benefício em pacientes com AR e deve ser utilizada no primeiro trimestre. Normalmente, é feita com progesterona micronizada 200 mg via vaginal de uma a três vezes ao dia.
Infecções
Qualquer infecção que leve à bacteremia ou viremia pode causar aborto de primeiro trimestre, mas, normalmente, não estão envolvidas em AR. Toxoplasmose, rubéola, citomegalovírus (CMV) e sífilis também podem estar associadas a abortos, mas não com AR. DSTs também podem estar associadas a aborto e devem ser investigadas. Recomenda-se ainda bacterioscopia e cultura de secreção vaginal, além de pesquisa específica de Mycoplasma hominis, Ureaplasma urealiticum, Chlamydia trachomatis e Neisseria gonorrhoeae.
Entretanto, mesmo não havendo infecção vaginal detectada, pode haver uma inflamação do endométrio. Endometrite crônica está presente em 9%-12% das mulheres com AR, mas não está estabelecido se realmente está envolvida na causa. É geralmente assintomática ou com sintomas discretos, como o corrimento vaginal, dores pélvicas discretas ou sangramento vaginal irregular. Acredita-se que essa infecção pode produzir toxinas que causam danos ao embrião e ao processo de implantação. É diagnosticada por biópsia de endométrio com anatomopatológico compatível com infecção (o que nem sempre está presente) ou presença de plasmócito no estroma endometrial (CD138 e EMA) detectado por imuno-histoquímica. Quando presente, deve ser tratada com antibiótico.
Outro exame que pode avaliar a presença de endometrite crônica é o Teste ALICE. Por meio dele, identifica-se a presença das oito principais bactérias patogênicas associadas à Endometrite Crônica, auxiliando o manejo clínico com a indicação do tratamento probiótico ou antibiótico adequado.
Se por um lado há bactérias que causam mal ao sistema reprodutor feminino, existe um grupo de bactérias que podem ser benéficas. Hoje sabemos que as bactérias normalmente encontradas no endométrio fazem parte de uma 8. Infecções flora normal (ou microbiomaI). Sua presença não causa endometrite, mas protege contra bactérias patogênicas. Entre as bactérias benéficas estão os lactobacilos (Lactobacillus acidophilus, L. bulgaricus, L. reuteri, L. Gasseri, L. Iners, L. Crispatus, L. Jenseni, L. plantarum, L. casei, B. bifidus) S. salivarius, S. thermophilus e Saccharomyces boulardii.
Apesar de não haver estudos relacionando o microbioma uterino com abortos de repetição, sua avaliação pode ter benefício em casos de abortos inexplicados e pode ser realizada por meio do Teste EMMA (análise metagenômica do microbioma endometrial). Esse exame identifica a porcentagem de Lactobacilos e outras bactérias. Se o endométrio não é dominante em Lactobacilos, o tratamento com probióticos pode ser benéfico.
Causas masculinas
Os parâmetros usuais do espermograma não parecem ter relação com AR, entretanto, estudos sugerem que o aumento da fragmentação do DNA do espermatozoide aumenta a taxa de aborto e pode estar associado a AR. As causas mais comuns de fragmentação alterada são fumo, idade avançada, drogas e varicocele. A erradicação dessas causas pode melhorar esse problema, mas, se isso não for suficiente, o tratamento com antioxidantes pode ajudar (vitamina C 500 mg/dia, vitamina E 400UI/dia e ácido fólico 5 mg/dia). Em alguns casos, podem ser prescritos anti-inflamatórios e antibióticos, mas sem evidência científica de real benefício.
Causas imunológicas
Os problemas imunológicos têm sido responsabilizados por alguns casos de insucesso na fertilização in vitro e por abortos de repetição. Alguns autores acreditam que muitos casos de falha são, na verdade, abortos muito precoces que, após um período curto de implantação embrionária, não chegam a ser detectados nos testes de gravidez, não evoluem e são eliminados. Existem controvérsias a respeito desse tema, mas os resultados positivos têm nos encorajado a prosseguir com esse tratamento, indicado em situações especiais.
A implantação do embrião ao útero é um processo muito complexo que envolve interações do embrião com o endométrio. O papel do sistema imune na implantação e desenvolvimento embrionário é essencial ao processo. Do ponto de vista imunológico, a gestação somente é possível porque uma intrincada rede imunorregulatória é disparada com o objetivo único de desenvolver um estado de tolerância materno-fetal e permitir a implantação, o desenvolvimento fetal e a formação da placenta.
Dada a sua importância, problemas imunológicos têm sido responsabilizados por alguns casos de AR. A literatura médica nesse assunto é controversa, mas existem alguns exames que podem ser realizados e tratamentos que podem ser propostos.
O produto gestacional contém metade do seu material genético de origem paterna, sendo, portanto, estranho ao sistema imune da mãe. Mas, de alguma forma, esse embrião é reconhecido pelo sistema imune materno, sem que seja disparada uma resposta imune de rejeição como ocorre nos transplantes. Ainda não se sabe totalmente como isso ocorre, mas sabe-se que várias células do sistema imune, incluindo linfócitos T e células Natural Killer (NK), participam deste processo.
Linfócitos T Auxiliares (T helper)
Linfócitos são um dos vários tipos de glóbulo branco (célula sanguínea de defesa). Linfócitos T são aqueles cuja ação é realizada pela liberação de citocinas (substâncias que regulam as células do sistema imune).
Entre os diferentes tipos de linfócitos, estão os T auxiliares, um subgrupo de linfócitos muito importante à implantação. Os linfócitos T auxiliares podem ser de 3 tipos principais: Th1, Th2 e Th17.
Linfócitos Th1 liberam as seguintes citocinas: interferon gama (IFNb), fator de necrose tumoral (TNFα) e interleucinas: IL-1, 2, 12, 15 e 18. Estas citocinas são pró- -inflamatórias, além de estimularem a ação citotóxica das células NK.
Já linfócitos Th2 liberam citocinas IL-4, IL-5, IL-6 e IL-10, que têm ação anti-inflamatória, além de inibir a ação citotóxica das células NK. No início da gravidez, ocorre um aumento da taxa de linfócitos Th2 em relação aos linfócitos Th1, ou seja, uma dominância da via Th2, fato importante para a implantação. Por outro lado, muitos estudos já demonstraram relação entre predomínio da via Th1 (logo, aumento na atividade inflamatória e citotóxica) e falhas de implantação e aborto de repetição.
Entretanto, apesar desta relação ser clara, existem algumas controvérsias. Primeiro, não se sabe ao certo se esta alteração na taxa Th1/Th2 é um defeito primário que leva à perda gestacional ou consequência de uma gestação que não está evoluindo por outra causa, por exemplo aneuploidia (alteração cromossômica), uma vez que gestações anembrionadas (em que o embrião não desenvolve) por aneuploidia também demonstram perda da dominância Th2/ Th1. Além disso, questiona-se se, antes da concepção, há diferenças no sistema imune entre mulheres que, na gravidez, terão resposta com dominância Th2 (favorável) e aquelas com dominância Th1 (adversa). Na verdade, predomínio Th1 fora do período gestacional é normal.
Entretanto, apesar da falta de compreensão completa e questionamentos sobre o quão relevantes são os exames disponíveis para se avaliar defeitos imunológicos em AR, alguns tratamentos imunes têm sido propostos, entre eles, corticoides, imunoglobulina, intralipídio e heparina (explicados abaixo). Acredita-se que esses tratamentos podem estimular a via Th2, favorável à implantação.
Há ainda uma outra via de resposta imune mediada por linfócitos T auxiliares: Th17, com liberação das citocinas IL-17, IL-22 e IL 26, que também aumentam o processo inflamatório e podem estar relacionados com piores resultados gestacionais.
Linfócitos T Reguladores (Treg)
Linfócitos T reguladores são um tipo de linfócitos T com função imunorreguladora, ou seja, apresentam como característica básica a capacidade de produção de citocinas imunossupressoras, como IL-4, IL-10 e TGF-β. Atuam em uma complexa rede de mecanismos reguladores destinados a assegurar a modulação das respostas imunológicas frente aos diversos antígenos provenientes de agentes infecciosos, tumores, aloantígenos, autoantígenos e alérgenos.
Na gestação, essa atividade é especificamente dirigida aos antígenos paternos, regulando toda a intrincada rede de atividade imune relacionada ao reconhecimento do embrião, implantação, formação da placenta e desenvolvimento fetal. Apesar dos mecanismos específicos de sua ação imunomodulatória na gestação ainda estarem sendo estudados, foi demonstrado que a proporção de células Treg no endométrio e no sangue periférico aumenta na fase de gestação precoce. Além disso, a ausência de células Treg leva à linha, alguns estudos já demonstraram associação de falhas de implantação, aborto de repetição e problemas de placentação (pré-eclâmpsia e parto prematuro) com uma menor atividade da Treg.
Células NK
As células NK são um tipo de linfócitos caracterizadas pelo receptor de superfície CD56, que pode ser reconhecido por imuno-histoquímica. Apresentam uma ação citotóxica, ou seja, levam à destruição celular, mecanismo importante para a defesa. As células NK reconhecem células com alteração como células tumorais e infectadas por vírus e as destroem. Considerando-se que a presença de células NK no útero, inclusive na interface materno-fetal, já foi demostrada e que as células NK são capazes de reconhecer o embrião, levantou-se a hipótese de que sua ação exagerada poderia levar à destruição das células dos embriões. Muitos estudos demostraram associação de uma atividade aumentada de células NK no endométrio com falhas de implantação, abortos e problemas tardios na gravidez, como restrição de crescimento fetal e pré-eclâmpsia (aumento de pressão arterial na gestação). Assim, muitos tratamentos foram propostos visando diminuir a atividade das células NK.
Dosagem sanguínea não reflete a expressão endometrial e não tem valor. A dosagem no endométrio pode ser feita colhendo-se material por biópsia realizada no período após a ovulação e encaminhada para análise por imuno-histoquímica. Entretanto, não há consenso na literatura sobre o que é considerado um número normal de células NK no endométrio. Há autores que consideram valores acima de 10% como aumentados, outros, valores acima de 5%. Quando a atividade citotóxica está aumentada, alguns tratamentos podem ser propostos, incluindo corticoides, intralipídeo, imunoglobulina e G-CSF.
Autoanticorpos
Autoanticorpos são anticorpos produzidos pelo nosso sistema imune contra células do próprio organismo, podendo causar doenças como Doença de Hashimoto (hipotireoidismo por anticorpos contra a tireoide) e lúpus. Muitos autores associam a presença de autoanticorpos com infertilidade, falência ovariana, endometriose, falhas de implantação e abortos. Alguns estudos já demonstraram piores resultados em ciclos de fertilização in vitro (FIV) em pacientes com autoanticorpos (FAN e anticorpos antitireoides), mas não se sabe ao certo qual mecanismo poderia interferir nos resultados. Assim, tratamento com corticoides tem sido proposto para melhorar os resultados, embora esta conduta possa ser questionada.
OBS: existe um autoanticorpo específico (anticardiolipina) relacionado à síndrome do anticorpo antifosfolípede, patologia comprovadamente associada a aborto de repetição e eventos trombo embólicos na gestação, já abordado no tópico trombofilias.
Tratamentos Imunológicos
Apesar de não ser consenso, e alvos de muita crítica, muitos tratamentos imunológicos vêm sendo propostos para aumentar as taxas de implantação e diminuir o risco de aborto. Os estudos são limitados, mas demonstram algum benefício. Assim, apesar de não ser indicado como rotina nos tratamentos de reprodução assistida, podem ser uma opção em casos de falhas de implantação, aborto recorrente.
São eles:
AAS (Aspirina)
É um anti-inflamatório com a função de inibir a agregação plaquetária, tendo, assim, um efeito antitrombótico. Sua ação em reprodução é diminuir o processo inflamatório na cavidade uterina, podendo ter benefício em casos de aborto de repetição. Como é barato e de fácil uso, vem sendo utilizado em grande escala em reprodução, mas ainda há controvérsias de sua real indicação.
Heparina
Como dito anteriormente, a heparina vem sendo usada em pacientes com aborto de repetição e trombofilias. Entretanto, mesmo na ausência de trombofilias, alguns autores recomendam seu uso em casos de aborto de repetição e falhas de implantação. A razão seria porque, além do efeito antitrombótico, a heparina aumenta alguns fatores de crescimento como IGF (insulin-like growth factor) I e II, que aumentam a invasão trofoblástica (penetração do embrião no endométrio).
Além disso, induz a produção de enzimas importantes para esta invasão. Apesar de haver beneficio teórico do seu uso, em geral, é recomendado somente em casos em que haja alguma trombofilia detectada.
Corticoides
Corticoides são drogas imunossupressoras, ou seja, que diminuem a resposta inflamatória do sistema imune e a atividade das células NK, podendo diminuir a chance de aborto. Uma opção muito comum é a prednisona, por ser via oral e de baixo custo. Vem sendo muito utilizada em casos de abortos prévios e aumento de atividade das células NK, embora seu benefício seja algo ainda controverso.
Imunoglobulina
É uma medicação intravenosa já usada há muito tempo para tratar doenças autoimunes e condições inflamatórias não relacionadas à gravidez. Vem sendo proposto que a imunoglobulina pode reduzir a citotoxicidade das células NK, aumentar as células T reguladoras (Treg) e induzir a resposta Th2, condições que diminuiriam o risco de aborto e mostrariam melhora nas taxas de implantação, gravidez e nascidos-vivos. Entretanto, há poucos estudos bem desenhados que realmente confirmam seu benefício em AR, sendo também ainda alvo de polêmica. Soma-se ainda o fato de ter um custo muito elevado. Alguns autores recomendam o uso somente se houver aumento de atividade de células NK, mas também não há consenso.
Intralipid® / Lipofundin® (Intralipídeo)
Lipofundin® é uma emulsão de lipídeos usada normalmente para nutrição parenteral de pacientes. Seu uso em reprodução se deve ao fato de se acreditar que tem ação semelhante à imunoglobulina, diminuindo a citotoxicidade de células NK e suprimindo as citocinas pró-inflamatórias (via TH1), podendo ser útil em casos de falhas de implantação e abortos, principalmente se associado ao aumento da citotoxicidade das células NK. Não se sabe por qual mecanismo exato o Intralipid® modula o sistema imune, mas acredita-se que os ácidos graxos da emulsão ligam- -se a receptores das células NK, diminuindo sua citotoxicidade. É administrado por via intravenosa durante um período de 3-4 horas, semelhante à imunoglobulina, repetindo-se a cada 2-3 semanas no primeiro trimestre da gestação. Tem a vantagem de ter um custo muito mais baixo do que a imunoglobulina, sendo um tratamento muito mais acessível.
Poucos dados da literatura confirmam a eficácia desta terapia, mas um estudo randomizado com 296 mulheres inférteis, ou com aborto de repetição e aumento de células NK, demonstrou melhora discreta na taxa de nascidos-vivos. Em outro estudo, com 162 mulheres com falhas prévias de implantação e 38 com abortos recorrentes com elevação de células NK, o tratamento com intralipídeo teve uma taxa de gravidez de 52%, e somente 9% de aborto. Comparando o intralipídeo à imunoglobulina, os estudos demonstram não ter diferença de eficácia. Apesar da limitação dos estudos, mesmo sendo controverso, é uma opção de tratamento que pode ter benefício.
G-CSF
(Granulocyte-colony stimulating factor ou Fator estimulante de colônia de granulócitos)
G-CSF é um fator de crescimento que tem efeito específico na ativação de vias intracelulares associadas à proliferação celular, diferenciação e estimulação de granulócitos (um tipo de glóbulo branco no organismo). É um medicamento muito utilizado em oncologia quando há queda dos glóbulos brancos após a quimioterapia. Entretanto, foi demonstrado que muitos outros tecidos do organismo, incluindo os do sistema reprodutor, têm receptores e também produzem G-CSF. Além disso, há nos tecidos fetais receptores para esses fatores de crescimento e a concentração sanguínea aumenta durante a ovulação, além de ter alta concentração no interior dos folículos e nos tecidos fetais. Em animais, foi demonstrado que, se essas citocinas estiverem ausentes, não ocorrerá implantação. Estudos ainda mostram efeito do G-CSF na ativação da via Th2, ativação de células Treg, modulação da citotoxicidade das células NK no útero e estímulo da angiogênese (proliferação vascular) no endométrio, processo importante para a implantação e formação da placenta. Concluiu-se, então, a importância destes fatores em todas as etapas reprodutivas, levantando a hipótese de ter efeitos que podem contribuir para a implantação e evitar abortos de repetição de causa imunológica. Para uso em reprodução, normalmente utiliza-se aplicações subcutâneas repetidas.
Há poucos estudos publicados com seu uso, mas há alguma evidência de benefício. Um estudo (Scarpellini e Sbracia, 2013) avaliou seu uso em mulheres com abortos repetidos. Eles compararam 35 mulheres tratadas com G-CSF com um grupo de 33 mulheres que receberam, no lugar do G-CSF, um placebo. No grupo que recebeu a medicação, 29 deram à luz um bebê saudável, e seis abortaram novamente (82% de bebês nascidos). Entre as que receberem o placebo, 16 deram à luz, e as outras 17 abortaram (48,5% de bebês nascidos).
Anti-TNF (Adalimumab)
Adalimumab (Humira®) é um medicamento utilizado em algumas doenças inflamatórias como artrite reumatóide, cuja ação é bloquear o TNF-alfa, citocina relacionada à resposta imune Th1. Como a via está associada a falhas de implantação e aborto de repetição, foi proposto que este medicamento poderia ter benefício neste grupo de pacientes. Na literatura médica, ainda não há estudos consistentes (ensaios clínicos randomizados) que confirmam seu benefício, mas alguns dados vêm sendo publicados. Segundo pequenos estudos de Winger et al, em pacientes com aumento da relação Th1/Th2 ou aumento da atividade citotóxica NK, tratamento com Adalimumab aumentou a taxa de nascidos-vivos. Entretanto, é um estudo pequeno, com falhas metodológicas, sendo ainda prematuro afirmar um real benefício com esta medicação.
Tacrolimus
É um medicamento imunossupressor que inibe a resposta citotóxica dos linfócitos, a expressão de receptores IL-2 e a produção de IL-2 e Interferon gama, citocinas ligadas à via Th1. Dessa forma, assim como o medicamento anterior, foi sugerido que pudesse ter benefício em falhas de implantação/abortos recorrentes de causa imunológica. Um estudo avaliou pacientes com falhas de implantação prévias e aumento da relação Th1/Th2, mostrando que o uso do medicamento dois dias antes da transferência embrionária aumentou a taxa de gravidez clínica e a de nascidos-vivos de zero para 64% e 60%, respectivamente. Entretanto, apesar de benefício teórico, necessita-se mais estudo para avaliar seu benefício em AR.
Sirolimo (Rapamune®)
É um medicamento imunossupressor utilizado em transplantes para evitar rejeição. Seu mecanismo de ação é inibir a ativação e a proliferação de linfócitos T que ocorrem em resposta ao estímulo de antígenos e de citocinas. Nas células, o sirolimo liga-se à imunofilina, proteína de Ligação FK 12 (FKBP-12), para formar um complexo que se liga à enzima mTOR (Mammalian Target of Rapamycin), inibindo sua atividade. Essa inibição suprime a proliferação de células T induzida por citocina. Além do uso para evitar rejeição em transplantes, novos usos do Rapamune® vêm sendo propostos, incluindo seu uso em casos de falhas de implantação e aborto recorrente. Um estudo prospectivo randomizado avaliou 76 mulheres com falhas prévias, com aumento de Th17 (linfócitos T relacionados com maior resposta inflamatória) e diminuição de linfócitos T reguladores (Treg), relacionados com uma implantação normal. Quarenta e três usaram a medicação, enquanto 33 não utilizaram. Os resultados mostraram uma maior taxa de gravidez clínica no grupo tratado (55,81%), em relação a quem não utilizou a medicação (20,93%). Além disso, a taxa de gravidez que evoluiu além de 12 semanas (período de maior incidência de abortos) também foi maior no grupo tratado (44.18% vs 16.26%). Não se sabe ao certo qual o mecanismo de ação para estes resultados. Além disso, novos estudos são necessários para confirmar a eficácia desse tratamento, mas é uma nova opção que surge com resultado promissor.
Inflamações crônicas “silenciosas”
As Inflamações Crônicas Subclínicas, que aqui chamamos de “Inflamações Silenciosas” por serem imperceptíveis e não causarem sintomas, podem interferir na fertilidade, dificultando o sucesso da gravidez espontânea, e também nos tratamentos de fertilização (falhas de implantação).
A inflamação é um mecanismo de defesa natural do corpo. Faz parte do sistema imunológico e pode ser desencadeada por muitos fatores. É um processo complexo pelo qual os glóbulos brancos do corpo são liberados no sangue ou tecidos afetados para combater a infecção. A inflamação é a maneira de o corpo marcar uma região para receber atenção do sistema imunológico.
Óvulos e espermatozoides saudáveis e hormônios equilibrados são necessários para uma gravidez bem-sucedida, mas igualmente importante é a condição e a receptividade do útero. Um óvulo fertilizado deve inserir-se na parede do útero para implantação, mas a inflamação uterina crônica é uma causa conhecida de falha na implantação e perda gestacional precoce.
Essas inflamações são causadas por razões variadas: estresse físico, emocional e mental; dieta inadequada; toxinas ambientais; problemas simples de saúde, como alergias e obesidade; problemas ginecológicos, como ovários policísticos, endometriose, falência ovariana ou simples processos naturais, como a própria ovulação ou mudança cíclica do ovário.
Exames específicos para identificação precoce da Inflamação Crônica Subclínica são as citocinas: Interleucina 10 (IL-10); Interleucina 6 (IL-6); Lipoproteína A; Óxido Nítrico; Fator de Necrose Tumoral (TNF alfa) e a Fosfolipase A2 (PLAC2) .
O tratamento baseia-se em dieta apropriada que deverá ser indicada por nutricionista ou nutrólogo, suplementos vitamínicos manipulados de forma individualizada que minimizem o processo inflamatório, além da redução do estresse e atividades físicas regulares.
Condições reprodutivas associadas à Inflamação Crônica incluem: Endometriose; Síndrome do Ovário Policístico (SOP); Doença Inflamatória Pélvica; Miomas Uterinos e Cistos Ovarianos; Adenomiose e Síndrome de Asherman; Menopausa Precoce (insuficiência ovariana prematura); má qualidade de espermatozoides; má qualidade dos óvulos.
Intolerância ao glúten
A intolerância ao glúten, chamada doença celíaca, é uma doença inflamatória crônica, caracterizada por intolerância ao glúten contido no trigo e em cereais afins. O glúten representa 80% das proteínas do trigo e é composto pela mistura de gliadina e glutenina. A doença celíaca é causada por uma resposta imunológica do organismo, mas, apesar de ser frequentemente chamada de alergia ao glúten, não é um processo alérgico e, sim, autoimune, que compromete a mucosa intestinal dificultando a absorção de nutrientes..
Os sintomas característicos são diarreia, vômito, perda de peso, dor abdominal, aumento de gases, “estufamento” e perda de apetite. Entretanto, nem sempre apresenta este quadro clínico tão bem definido. Muitas vezes, o único sinal da doença, que é muitas vezes negligenciado, é a presença de abortos repetidos e infertilidade, uma vez que muitas pesquisas apontam uma ligação entre sensibilidade ao glúten e desordens reprodutivas na mulher. Os mecanismos não são totalmente claros, mas o que se sabe hoje é que a doença celíaca provoca má absorção de nutrientes importantes para o sistema reprodutor, como ferro, ácido fólico, vitamina K, B12, B6 e outras vitaminas lipossolúveis, que poderiam ser também responsáveis até por malformações congênitas.
Além do risco de infertilidade, tem sido demonstrado que, em mulheres com doença celíaca não tratada, a taxa de aborto espontâneo é maior que a encontrada na população geral. Nestes casos, o risco relativo de aborto múltiplo e recém-nascidos de baixo peso é 8-9 vezes maior do que o da população geral.
Para diagnóstico, alguns exames podem ser realizados:
Anticorpos a serem pesquisados
- anti-TTG (Anticorpo antitransglutaminase)
- anti-EMA (Anticorpo antiendomísio)
- Anticorpo antigliadina
- IgA (se estiver baixo poderá confundir um falso negativo).
Teste genético
HlA-DQ2 e/ou DQ8. A grande maioria dos pacientes celíacos e 30% da população geral apresentam HLA-DQ2 e/ou DQ8. Assim, a presença de um desses dois alelos tem boa sensibilidade, mas baixa especificidade.
Tratamento
O tratamento baseia-se exclusivamente na dieta alimentar. Deve-se excluir do cardápio produtos industrializados com a presença de glúten, como pães, bolos, bolachas, macarrão, coxinhas, quibes, pizzas, cervejas, uísque, vodca etc., quando estes alimentos possuírem o glúten em sua composição ou processo de fabricação. Um desafio para aqueles que adoram este tipo de comida! Devido a exclusão total de alguns alimentos ricos em carboidratos e fibras, esta dieta é composta, em sua maior parte, de gorduras (margarina, manteigas, óleos etc.) e proteínas (carne em geral) e, em menor parte, de carboidratos (massas sem glúten, açúcares, etc.). Todo celíaco que não transgride a doença tende a ter um aumento do peso corporal e, desta forma, deve ter uma dieta equilibrada. Para tanto, deve diminuir a ingestão de proteínas, moderar o consumo de gorduras, e aumentar o consumo de frutas, sucos naturais, verduras e legumes, tornando a alimentação mais adequada e saudável. O malte, muito questionado, é um produto da fermentação da cevada, portanto, apresenta também uma fração de glúten. Os produtos que contenham malte, xarope de malte ou extrato de malte não devem ser consumidos pelos celíacos. O glúten não desaparece quando os alimentos são assados ou cozidos e, por isto, a dieta deve ser seguida à risca.
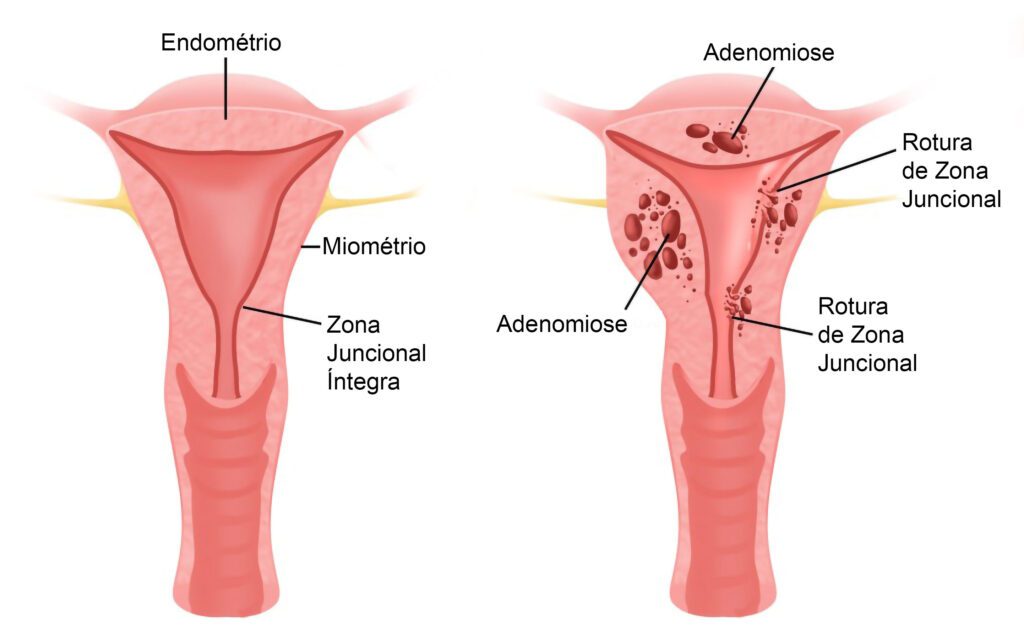
Adenomiose
A adenomiose é uma patologia uterina relacionada com a Endometriose, caracterizada pela presença de glândulas e estroma endometrial no miométrio (camada muscular do útero), podendo levar a hipertrofia das fibras musculares, com aumento do volume uterino.
A Adenomiose pode ser focal ou difusa, e, quando difusa, pode tornar o útero mais volumoso e pesado. A doença é comumente encontrada em multíparas entre 35 e 50 anos, mas estudos recentes mostram sua associação com infertilidade, falhas de implantação e abortos recorrentes.
Clinicamente, a Adenomiose causa menorragia (aumento do fluxo menstrual), dismenorreia (cólicas) e dor pélvica crônica. Sua causa ainda é desconhecida.
A Ressonância Magnética da pelve é o exame padrão ouro para o diagnóstico, com 90 de taxa de especificidade e sensibilidade, mas uma Ultrassonografia Endovaginal boa resolução realizada por profissionais especializados nesta área, também pode ser utilizada para diagnóstico. Mulheres que apresentam a zona juncional entre o endométrio e miométrio acima de 8mm são diagnosticadas com a doença.
O mecanismo exato da associação de Adenomiose e infertilidade ainda não está claro. Estudos mostram sua associação com as falhas de implantação e aumento no risco de abortos em mulheres submetidas a tratamento de Fertilização in Vitro. Estudos multicêntricos apontam para um mecanismo autoimune no processo, devido ao aumento de macrófagos (CD163) e células NK (CD 56) no endométrio de mulheres com Adenomiose.
Pacientes com Adenomiose se beneficiam com “Ultra Down Regulation” por 2-6 meses, isto é, a mulher recebe os medicamentos agonistas de depósito ( Lectrum, Lupron Depot ou Zoladex) antes do início do preparo do útero para a transferência dos embriões. O tempo de tratamento vai depender do grau de comprometimento do útero.
Atualmente, o IPGO recomenda o exame de Ultrassom com preparo intestinal para que se avalie também a Endometriose que, frequentemente, está associada à Adenomiose. A partir desse exame, a Adenomiose é considerada grave quando compromete mais do que 50% do miométrio.
Abortos recorrentes sem explicação
E m até 50% dos casos, nada se encontra na investigação de AR. Assim, tratamento empírico com corticoide, AAS e heparina não demonstrou benefício. A mulher deve ser orientada a mudar o estilo de vida: parar de fumar, diminuir o consumo de álcool e cafeína, praticar exercícios moderados e controlar o peso. Suplementação de ácido fólico e progesterona também deve ser indicada, e muitas vezes é necessário suporte psicológico para que o casal, abalado pelas perdas prévias, não desista de tentar uma nova gravidez. É importante informar ao casal que a chance de ter uma gestação normal na próxima vez, sem nenhuma intervenção, é de 50%-75%, dependendo da idade da mulher e do número de abortos prévios, e que, portanto, vale a pena continuar tentando!
Aborto na FIV
Muitas mulheres apresentam alterações que estão associadas a aborto de repetição, mas não o sabem, pois não conseguiram engravidar espontaneamente. Após tratamentos de reprodução assistida, algumas conseguem engravidar, mas cerca de 15% a 20% das pacientes que conseguem a gravidez, acabam evoluindo para o aborto. Isso é muito frustrante, visto o quão desgastante é o tratamento de fertilização in vitro. Devido a isso, muito se discute se devemos investigar como rotina as causas de aborto em pacientes que fazem tratamentos de reprodução assistida. Não há consenso, mas o IPGO costuma investigar as principais causas em toda paciente submetida a tratamento de fertilização in vitro e, se há alguma alteração, orientamos tratamento.
No caso de abortos após a FIV, exames mais específicos podem ser orientados com a pesquisa do KIR.
Nova abordagem imunológica na FIV: o papel do KIR x HLA-C
Como dito anteriormente, sabemos que uma atividade citotóxica exagerada das células NK poderia estar relacionada a perdas gestacionais, diminuir esta ação pode ser eficaz. Entretanto, novos estudos vêm demonstrando que a ação da célula NK uterina é mais complexa, uma vez que existem dois tipos de células NK com atividades distintas. Já foi dito que as células NK são caracterizadas pela presença do receptor CD56, entretanto podem ser CD56dimCD16+ ou CD56brightCD16-. O primeiro tipo tem ação citotóxica, enquanto o segundo tipo não. Na verdade, 15. Aborto na FIV estas últimas liberam citocinas que são imunomoduladoras e que contribuem para a implantação (citocina é qualquer substância liberada por células do sistema imunológico que controla as reações imunológicas do organismo).
Na gestação normal, as células trofoblásticas produzem citocinas da via Th2, que induzem a diferenciação das células NK em células não citotóxicas. Já as citocinas Th1 são ditas indutoras de abortamento, devido à capacidade de induzir na interface materno-fetal a diferenciação fenotípica das células NK em células com atividade citotóxica. Diferentemente das células NK citotóxicas, as NK uterinas são muito importantes para o sucesso da implantação.
Células NK não citotóxicas
As células NK uterinas não citotóxicas são, na verdade, essenciais para a implantação. Estudos demonstram que elas liberam citocinas que regulam a invasão do trofoblasto (células embrionárias) no endométrio, auxiliam nas alterações vasculares importantes para formação da placenta, além de estimular a via imune Th2 (antiinflamatória), essencial para a implantação. Sem a ação das células NK uterinas, o processo de implantação e placentação ocorre de forma deficiente, causando diferentes problemas de acordo com a severidade. Sem a invasão do trofoblasto e transformação vasculares locais, o embrião não implanta. Se ocorrer de forma deficiente, pode até haver implantação, mas evoluir para aborto precoce. E, se de forma menos intensa, a gestação pode evoluir, mas com risco aumentado de restrição de crescimento fetal e pré-eclâmpsia (aumento da pressão arterial na gestação).
Dessa forma, as células NK uterinas são importantes para a ocorrência da gestação. No entanto, a sua presença não basta, mas, sim, a interação com as células trofoblásticas. Essa interação ocorre por meio de partículas da superfície das células trofoblásticas chamadas HLA e receptores das células NK chamados KIR (killer immunoglobulin-like receptor).
Receptor KIR
A ação das células NK, tão importantes para uma gestação normal, depende de uma perfeita interação imunológica entre uma molécula da superfície das células do embrião (chamada HLA-C) e os receptores KIR das células NK uterinas.
Todo ser humano dispõe, em suas células, de antígenos (moléculas que interagem com o sistema imune) denominados HLA, que distinguem os antígenos do próprio organismo dos estranhos. Nosso sistema imune reconhece os antígenos diferentes aos das próprias células, levando a uma reação imunológica.
Os antígenos HLA representam a “marca registrada” de cada indivíduo, a “impressão digital” única, que pode ter uma similaridade maior ou menor com duas pessoas. Assim, quanto maior a distância dessa similaridade, maior a chance de rejeição. O antígeno HLA é uma denominação genética que, nos casos de transplantes de órgãos, tem o objetivo de avaliar o doador ideal para determinado paciente. Os antígenos são divididos em tipos: classe I (A, B e C), classe II (DR, DP, DQ) e outras. Os antígenos HLA estão presentes em todas as células do corpo humano e coordenam a resposta imunológica do nosso organismo não só nos transplantes, mas também em diversas doenças e reações a medicamentos, estimulando a formação de células de defesa, os leucócitos e anticorpos.
O antígeno do embrião é o HLA-C. Como o embrião é composto de 50% de material genético paterno e 50% de material genético materno, ele tem molécula HLA-C materna e paterna. As células NK reconhecem o HLA-C estranho ao seu organismo, ou seja, o HLA de origem paterna. Entretanto, quando a célula NK em questão reconhece este HLA diferente, ela não induz à rejeição, como nos transplantes, mas libera citocinas importantes para gestação.
O HLA-C do embrião pode ser de dois tipos: C1 e C2. A molécula C1 interfere pouco na atividade da célula NK, então pouco afeta a gestação. Já a C2 tem uma ação muito maior sobre os receptores KIR, sendo, então, mais importante para a gestação. Entretanto, sua ação vai depender do tipo de receptor KIR. Este é determinado por um grupo de genes (haplotipo) que pode ser definido como grupo A, quando gera receptores somente com atividade de inibição; ou grupo B, quando gera algum receptor com atividade estimulatória. Assim, a mãe pode ser AA, AB ou BB (pois tem um haplotipo herdado do pai e um da mãe).
Novos estudos, realizados na Espanha, pela equipe liderada pela Drª Diana Alecsandru, imunologista da clínica IVI Madri, revelaram, entre outras coisas, que a união dos receptores KIR AA com antígenos HLA-C2 paterno é uma combinação de risco para o ser humano, uma vez que o HLA-C2 tem uma forte ação sobre os receptores KIR AA, que têm função inibitória sobre as células NK protetoras que se tornam inativas. Isso, portanto, dificulta a implantação e formação da placenta de forma adequada, levando às complicações já descritas.
Quando transferimos dois embriões, a situação se agrava, pois há estímulo HLA-C2 paterno de mais de um embrião, bloqueando, no caso de KIR AA, ainda mais essa ação protetora. Para evitar essas complicações, pode-se avaliar o KIR da mulher e o HLA-C paterno, por meio de exames de sangue. No exame do KIR, avalia-se se a mulher é KIR AA, AB ou BB. No caso do HLA, considerando que herdamos um HLA-C do pai e um da mãe, o marido poderá ser C1C1, C1C2 ou C2C2. Se for C1C1, o embrião gerado terá sempre HLA paterno C1. Se C2C2, sempre o embrião terá C2. E se o marido for C1C2, os embriões formados têm 50% de chances de terem HLA paterno C1 e 50% de chances de terem C2.
Quando a mulher é AB ou BB, não há risco. O mesmo ocorre quando o homem é C1C1. Já nos casos da mulher KIR AA e o marido C2C2 há um risco aumentado de complicações, principalmente se transferirmos dois embriões, sendo indicado transferir somente um por vez. No caso de mulher KIR AA com marido C1C2, como há uma chance de 50% de cada embrião ter C2 paterno, aconselha-se também transferir somente um embrião.
Este texto foi extraído do e-book “Abortos podem ser evitados”.
Faça o download gratuitamente do e-book completo clicando no botão abaixo: