Entre os processos de reprodução humana para mulheres mais velhas, a FIV é o que oferece os melhores resultados na concepção do bebê.
Lembramos que se chama fertilização in vitro porque a fecundação é feita em laboratório, ou seja, diferentemente do que ocorre no método natural, a formação do embrião (junção do gameta feminino, o óvulo, com o gameta masculino, o espermatozoide) acontece fora do útero da mulher. O processo pode ser dividido em 6 fases:
- 1ª Fase – Estímulo do crescimento dos folículos.
- 2ª Fase – Bloqueio dos hormônios do organismo (poderá ser antes ou depois do início da estimulação ovariana).
- 3ª Fase – Aspiração e recuperação dos óvulos.
- 4ª Fase – Fertilização dos óvulos pelo espermatozoide.
- 5ª Fase – Transferência do embrião para o útero.
- 6ª Fase – Controle hormonal até o teste de gravidez.
1ª fase Estímulo do crescimento dos folículos
A primeira fase é a estimulação ovariana propriamente dita, quando medicamentos, em geral injetáveis, são administrados para fazer com que vários folículos cresçam nos ovários. Os medicamentos utilizados para indução são chamados gonadotrofinas, contém o hormônio FSH e são encontrados em diversos tipos, dosagens e nomes comerciais. As dosagens diárias recomendadas são reguladas de acordo com a necessidade verificada pelos exames realizados sistematicamente durante essa fase (hormônios e ultrassom). A estimulação ovariana deverá ser acompanhada pela ultrassonografia para avaliar o crescimento e o desenvolvimento dos folículos ovarianos (dentro dos quais estão os óvulos) até que atinjam um diâmetro médio aproximado de 18mm. A espessura do endométrio (tecido que reveste o útero internamente e onde o embrião se implantará) também é avaliada e deverá ser superior a 7mm. Normalmente, são realizados dois a quatro exames de ultrassom transvaginal durante o ciclo, marcados em intervalos médios de dois dias, iniciando no quinto dia após o início da estimulação, até que alcance o ponto pré-ovulatório. Sempre que as datas de exames caírem no domingo ou feriado, não se preocupe, pois, esses exames poderão ser antecipados ou adiados sem interferir no sucesso final do procedimento. Caso seja necessário, os exames serão realizados também nestes dias.
Quando os folículos atingem um diâmetro médio de 18 mm é administrado um medicamento específico: hCG (Ovidrel® ou Choriomon® ), se os embriões forem ser transferidos no mesmo ciclo para o útero da paciente ou Gonapeptyl® ou Lupron® , se os embriões NÃO forem transferidos no mesmo ciclo. Estes medicamentos causam o chamado trigger da ovulação, visando a maturação final dos óvulos. As doses e os horários das medicações têm influência direta no horário da captação dos óvulos. Realizamos a aspiração dos óvulos entre 34 e 36 horas (conforme protocolo escolhido) após a aplicação. Os efeitos colaterais (raros) mais comuns desses medicamentos são: instabilidade emocional, dores de cabeça, perda de apetite, dor abdominal e dor no local das injeções. Neste último caso, a massagem e o calor local (compressas) podem aliviar esses sintomas.
Para que se alcance o objetivo almejado é fundamental a disciplina na medicação e no controle na estimulação ovariana e, para isso, devem ser seguidas as seguintes recomendações:
- Utilize somente os medicamentos recomendados.
- O dia do ciclo é sempre contado a partir do primeiro dia da menstruação.
- Os medicamentos deverão ser tomados e aplicados sempre no mesmo horário.
- A quantidade de medicação utilizada até a coleta dos óvulos vai depender da evolução do crescimento dos folículos. É recomendável sempre medicação extra de reserva.
ULTRASSOM NO 3º DIA DO CICLO
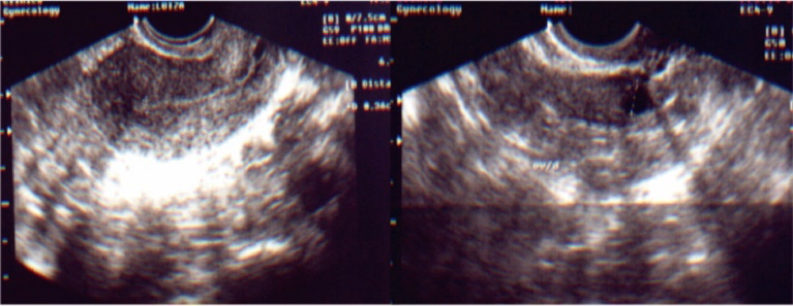
CONTROLE ULTRASSONOGRÁFICO NO 5º DIA DA ESTIMULAÇÃO OVARIANA
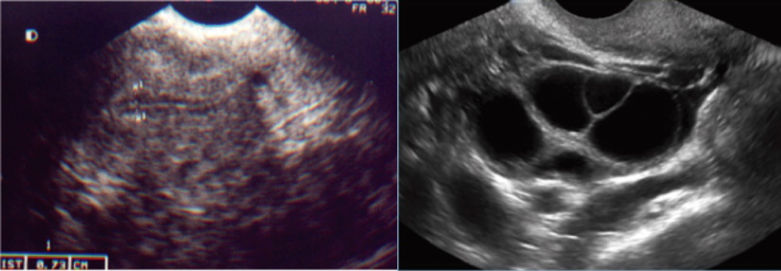
CONTROLE ULTRASSONOGRÁFICO NO 11º DIA DA ESTIMULAÇÃO OVARIANA
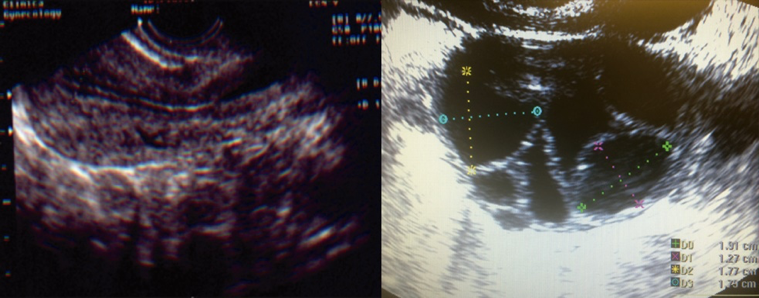
2ª fase Bloqueio dos hormônios
Consiste no bloqueio da produção pelo organismo dos hormônios que agem nos ovários com medicação adequada. Com esta conduta temos o controle da Observa-se endométrio > 7 mm (trilaminar) e presença de folículo ≥ 18 mm função ovariana “em nossas mãos” não havendo praticamente perigo de ocorrer ovulação fora do previsto. Isto é, sem estes medicamentos o mecanismo de controle da ovulação estaria também sob a influência dos hormônios do próprio organismo e você poderia ovular antes da hora programada de colher os óvulos.
O Bloqueio pode ser TARDIO (esquema curto ou protocolo curto, realizado durante a estimulação ovariana) ou PRÉVIO (esquema longo ou protocolo longo, iniciado antes da estimulação ovariana). A decisão pelo bloqueio prévio ou tardio vai depender de cada caso.
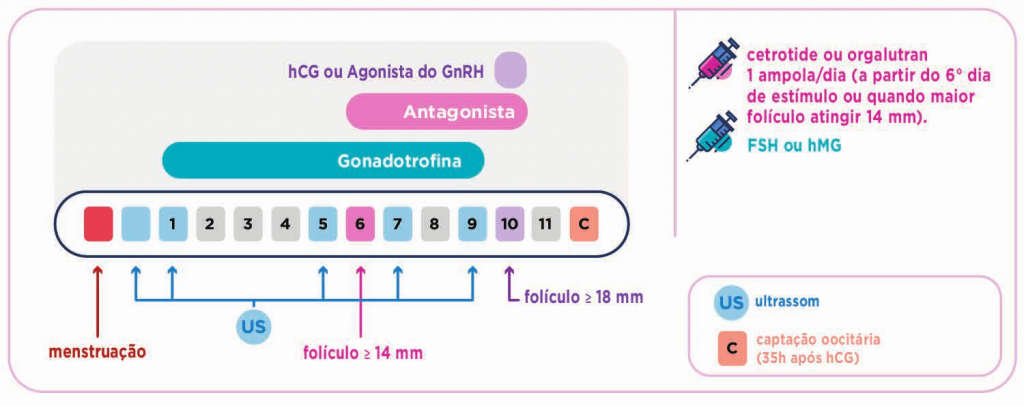
BLOQUEIO TARDIO (protocolo curto): Hoje em dia, o bloqueio tardio, é mais utilizado, pois proporciona um tratamento mais curto, com menos picadas e menor risco de complicações como a Síndrome do Hiperestímulo. É realizado, em geral, a partir do 5º a 8º dia da estimulação ovariana, utilizando a medicação Cetrotide® ou Orgalutran® . Uma vez iniciada, é mantido até o dia do trigger. Existem várias propostas em relação ao momento ideal de iniciar o antagonista, que variam entre o 5º e o 6º dia da indução ou, para alguns, quando os folículos atingirem o diâmetro de 14 mm. Cada clínica tem a sua preferência, o IPGO tem preferido utilizar o protocolo flexível, ou seja, quando a dimensão do maior folículo atinge 14 mm . Uma vez iniciando o antagonista, mantém-se até o dia do trigger.
A maior vantagem deste protocolo está nos casos de pacientes que têm risco de ter Síndrome de Hiperestimulação Ovariana. Nestes casos o hCG que finaliza a maturação folicular é trocado por uma dose única do agonista de GnRH (Gonapeptyl® ou Lupron® ), e com isso evitam-se as complicações desta Síndrome.
PROTOCOLO CURTO COM ANTAGONISTA
BLOQUEIO PRÉVIO (protocolo longo): O Bloqueio é iniciado geralmente no 21º dia do ciclo anterior à estimulação ovariana através de uma medicação injetável (Lupron Kit® , Gonapeptyl daily® ou outros). O Lupron Kit® (o mais usado) vem em um frasco único acompanhado de 14 seringas as quais são usadas para aspiração deste líquido. Você deverá aspirar até a marca 5 ou 10 dependendo do que foi receitado e aplicar na região subcutânea do abdome ou também na face anterior da coxa. As aplicações são diárias e não devem ser interrompidas ou modificadas até segunda ordem. Após 7 a 15 dias de medicação a paciente deverá menstruar. Um ultrassom transvaginal deve ser realizado no 2º ou 3º dia da menstruação, acompanhado muitas vezes de um exame de hormônios (estradiol e progesterona). Caso estes exames confirmem o bloqueio total dos ovários e dos hormônios do seu organismo, a estimulação poderá ser iniciada.
PROTOCOLO LONGO COM AGONISTA

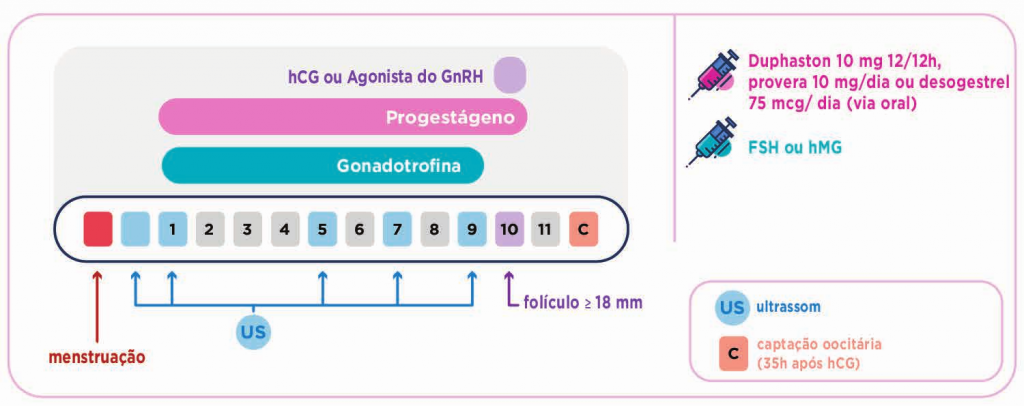
PROTOCOLO CURTO COM PROGESTÁGENOS: É possível realizar o bloqueio dos hormônios com medicação via oral: um progestágeno, hormônio semelhante à progesterona. Neste caso, iniciamos o bloqueio juntamente com o início da estimulação ovariana e mantemos até o dia do hCG ou agonista do GnRH.
PROTOCOLO CURTO COM PROGESTÁGENOS
PROTOCOLO COM FSH DE AÇÃO PROLONGADA: Elonva® (corifolitropina alfa): não há dúvidas de que uma reclamação frequente das mulheres que passam por um ciclo de FIV é o fato de precisarem tomar injeções diárias durante alguns dias. Embora este período normalmente não ultrapasse os dez dias, algumas pacientes chegam a desistir do tratamento por certo tempo e às vezes para sempre, por considerarem esta fase um sofrimento inesquecível.
Elonva® é uma injeção única que vale por sete dias de aplicação de FSH, substituindo as aplicações diárias neste período. É administrada em dose única por injeção subcutânea. As mulheres que pesam 60 kg ou menos devem receber uma dose de 100 microgramas, ao passo que as mulheres que pesam mais de 60 kg devem receber uma dose de 150 microgramas. A própria paciente ou o seu parceiro podem aplicar a injeção no caso de terem recebido as instruções adequadas.
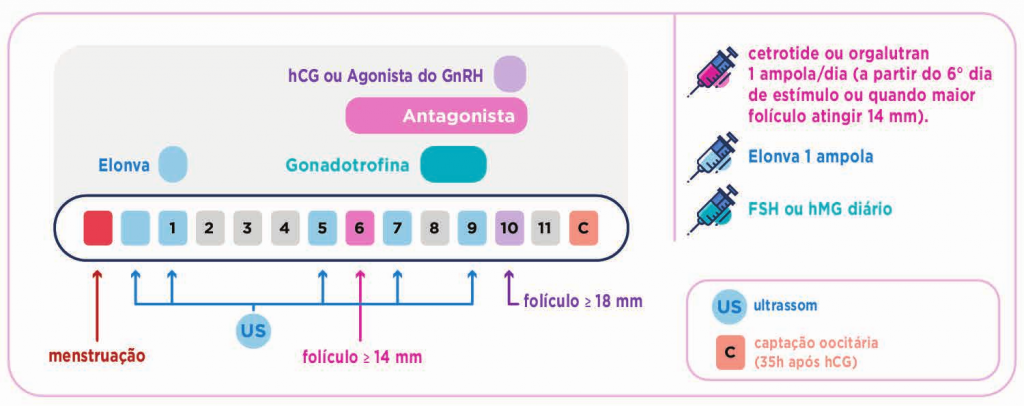
Cinco dias após a injeção do Elonva® , dependendo da resposta dos ovários, inicia-se o tratamento com um antagonista da GnRH, que impede uma liberação prematura dos óvulos pelos ovários. Sete dias após a injeção do Elonva® , no caso de ser necessária uma estimulação ovariana adicional, podem ser administradas injeções diárias de gonadotrofinas (FSH ou FSH+LH), até o momento de se realizar o hCG ou agonista do GnRH. Elonva® (corifolitropina alfa) tem ação semelhante a outros medicamentos que contêm FSH também utilizados para estimular os ovários nos tratamentos de fertilidade, mas tem a diferença de possuir uma ação prolongada no organismo. Em resultado disto, pode ser administrada uma dose única, substituindo desta forma sete injeções diárias necessárias para estes outros.
PROTOCOLO DE ESTIMULAÇÃO OVARIANA COM ELONVA® EM CICLO COM ANTAGONISTA
OBS: uma boa opção é utilizar protocolo de estimulação com Elonva® com progestágenos, reduzindo, assim, ainda mais as picadas. Neste caso, inicia-se o progestágeno via oral no dia de aplicação do Elonva® (MINI-FIV-PLUS)
Qual a melhor gonadotrofina para mulheres mais velhas?
FSH e LH são hormônios chamados gonadotrofinas, sendo produzidos pela glândula hipófise e agindo nos folículos ovarianos (pequenos cistos que contém um óvulo e são revestidos por dois tipo de células: teca e granulosa. O FSH, entre outras coisas, age na granulosa fazendo o folículo crescer e produzir estradiol (hormônio importante para estimular o endométrio). Já o LH age inicialmente na teca produzindo andrógenos (hormônios masculinos), que serão convertidos em estradiol pela granulosa.
Para estimular os folículos a crescer, é necessário o FSH, portanto as medicações de uso na estimulação ovariana sempre contém esse hormônio. Entretanto, podemos encontrar formulações com FSH isolado (Gonal® , Puregon® , Fostimon® ) ou associadas à ação LH (Pergoveris® , Menopur® , Merional® ).
Estudos demonstram associar LH mostra benefício em más respondedoras e pacientes mais velhas. Considerando que mulheres mais velhas tem queda na concentração de andrógenos e estes têm efeito positivo no crescimento folicular, seu uso parece justificado. (vide Uso de testosterona antes do estímulo ovariano).
Além disso, o LH parece ativar nas células da granulosa vias celulares (ERK e AKT) relacionadas a proliferação e crescimento celular e inibição de apoptose (morte celular).
Assim, em pacientes mais velhas, damos preferência a formulações que tenham ação LH associada ao FSH.
3ª fase Aspiração e recuperação dos óvulos
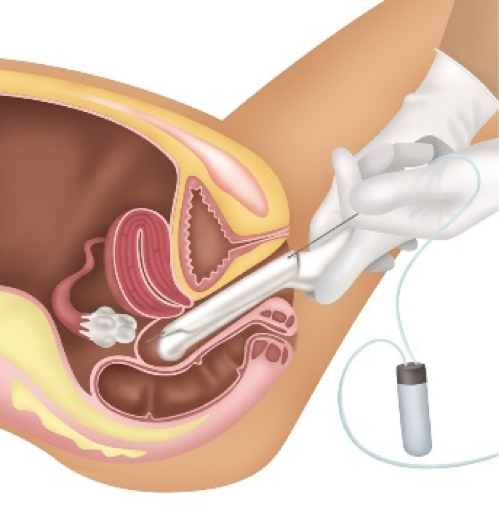
A paciente deverá comparecer ao laboratório especializado aproximadamente 35 horas após a administração do último medicamento (hCG ou Gonapeptyl). Neste momento, o médico estará presente para realizar o procedimento. Em jejum, em horário pré-estabelecido e em uma sala adequada, será dada uma medicação (sedação profunda com Propofol) para relaxar e dormir alguns minutos. Com auxílio do ultrassom, uma agulha especial e um aparato para sucção, os óvulos são colhidos e encaminhados para análise. Este processo é indolor e dura alguns minutos. Após cerca de 60 minutos em repouso em um quarto, a paciente será liberada, podendo executar atividades leves no mesmo dia, mas que não exijam destreza ou concentração (24 horas).
COLETA DE ÓVULOS
 |
Este é o momento da decisão se irá congelar óvulos (vitrificação) ou fertilizá-los.
AMOSTRA SEMINAL: Normalmente o sêmen é colhido por masturbação no dia da aspiração. Após a preparação adequada, a amostra será examinada e encaminhada para o processo de fertilização.
4ª fase Fertilização dos óvulos
Os óvulos após a ASPIRAÇÃO são separados, cultivados e classificados quanto à sua maturidade. Posteriormente, a fertilização poderá ocorrer de duas maneiras:
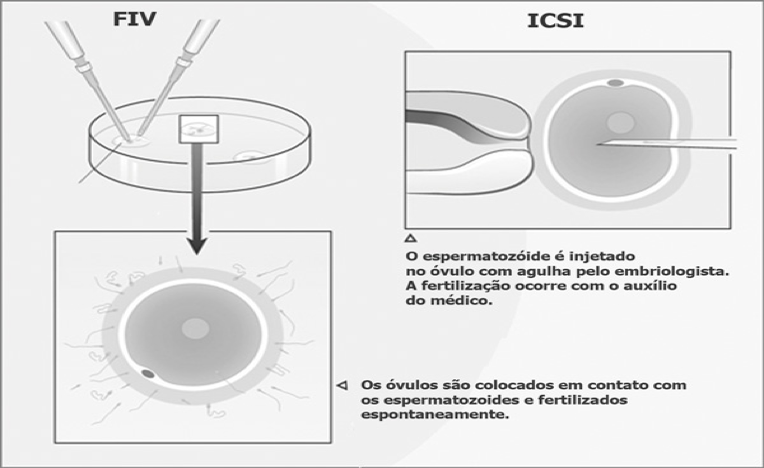
FIV CLÁSSICA: Os óvulos são colocados em uma incubadora no laboratório, junto dos espermatozoides, em condições ambientais semelhantes às encontradas na trompa uterina – local onde normalmente ocorre a fecundação.
ICSI (INTRACITOPLASMATIC SPERM INJECTION OU INJEÇÃO INTRACITOPLASMÁTICA DE ESPERMATOZOIDE): Quando a quantidade de espermatozoides for pequena, os óvulos serão fertilizados através da micromanipulação dos gametas injetando-se um espermatozoide em cada óvulo – Injeção Intracitoplasmática de Espermatozoide. É uma técnica sofisticada realizada por um profissional especializado, que, através de uma pipeta microscópica, injeta um único espermatozoide dentro do óvulo. Foi desenvolvida com o objetivo de tratar a infertilidade dos homens, que produzem pequenas ou nenhuma quantidade de espermatozoide, e das mulheres, que produzem uma quantidade muito pequena de óvulos e não podem correr o risco de não os ter fertilizados. Numa relação sexual normal, o sêmen ejaculado pode conter mais de 200 milhões de espermatozoides viáveis, mas apenas algumas centenas desse número realmente alcançarão o óvulo liberado na trompa de Falópio (tubas uterinas) e só um será capaz de fertilizá-lo. Homens com uma contagem de espermatozoides abaixo de 5 milhões por mililitro sempre foram considerados como de tratamento quase impossível. Com a ICSI, que é uma manobra laboratorial, pode se obter a fertilização com apenas um espermatozoide injetado em cada óvulo. A Injeção Intracitoplasmática de espermatozoide tem sido considerada como uma revolução nos últimos anos, pois oferece um tratamento viável para os mais difíceis casos de infertilidade masculina e feminina. Enquanto no passado não se podia oferecer nada além doação ou inseminação com esperma do doador àqueles casais cuja infertilidade era resultante de ausência ou da baixa quantidade de espermatozoides, agora, a ICSI oferece uma solução a esses casos e a outros que apresentam óvulos de difícil fertilização. Em ambas as técnicas, após 18h da coleta dos óvulos, estes são verificados e, quando confirmada a fertilização, passam a se chamar EMBRIÕES.
 |
 |
Normalmente os espermatozoides são escolhidos de acordo com sua motilidade e sua morfologia (forma). Mas, em alguns casos, os espermatozoides podem passar por uma seleção mais específica para a realização da ICSI: super-ICSI e PICSI.
“SUPER ICSI”, “ICSI DE ALTA MAGNIFICAÇÃO”: O “Super ICSI”, “ICSI de Alta Magnificação”, Morfologically Selected Sperm Injection, High Magnification Morfological Selection ou IMSI utiliza um sistema ótico que apresentam objetivas de maior poder de ampliação eletrônica das imagens, podendo observar os espermatozoides em detalhes, detectar seus defeitos e selecionar os melhores, pois são aumentados em até 12.500 vezes. Identifica em tempo real e com precisão os espermatozoides com maior capacidade de fertilização quando muitos deles tiverem alterações importantes no seu formato (morfologia alterada), vacúolos, alteração de motilidade e no DNA (fragmentações do DNA) – o conjunto destas alterações é dada pela sigla em inglês MSOME (Motile Sperm Organellar Morphology Examination). Estes espermatozoides podem formar embriões de má qualidade e consequente insucesso da FIV. O IMSI ou “Super ICSI” é indicado principalmente para casais cujo homem tem alterações importantes da morfologia dos espermatozoides, insucesso em tratamentos anteriores de FIV, altas taxas de fragmentação do DNA dos espermatozoides e abortos repetidos. Entretanto, a literatura médica ainda é controversa sobre o real benefício desta técnica.
PICSI (SELEÇÃO DE ESPERMATOZOIDES FUNCIONAIS): PICSI (Sperm Selection Device) é um recurso laboratorial utilizado no tratamento de fertilização in vitro, que seleciona os melhores espermatozoides para serem injetados no óvulo de um modo semelhante ao que ocorre naturalmente no organismo. Nela, o sêmen é colocado em uma placa com ácido hialurônico, uma substância parecida com a que é encontrada na camada externa dos óvulos. Essa substância atrai os espermatozoides de melhor qualidade e com menor fragmentação do DNA. É indicado nos casos de Fragmentação do DNA dos espermatozoides acima de 30%.
Em qualquer uma destas técnicas, 18 horas após a coleta dos óvulos é confirmada a fertilização e, assim, passam a se chamar pré-embriões, cujo crescimento é acompanhado até o terceiro ou quinto dia de desenvolvimento, quando então os embriões são transferidos ao útero ou vitrificados. Normalmente, esperamos a fase de blastocisto (quinto dia), pois selecionamos os que têm mais chances de implantação, mas dependendo do caso, principalmente se poucos embriões em desenvolvimento, optamos por transferir no terceiro dia. Na fase de blastocisto (quinto dia) poderá ser realizada a biópsia embrionária para análise genética (Biópsia de embriões – ESTUDO GENÉTICO (PGT-A)
5ª fase Transferência do(s) embrião(ões) para o útero
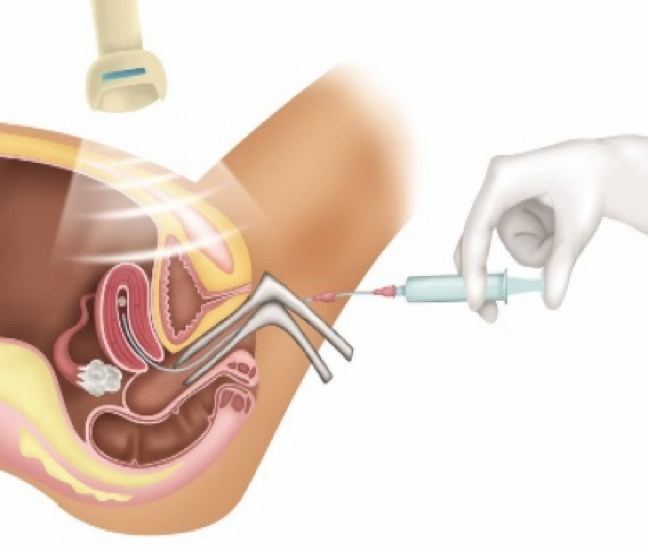
A TRANSFERÊNCIA DO(S) EMBRIÃO(ÕES) PARA O ÚTERO: é indolor, realizada sob visão do ultrassom, com cateter flexível e sem necessidade de anestesia, É introduzido um pequeno cateter pela vagina em direção ao colo do útero até atingir a cavidade uterina. O(s) embrião(ões) deve(m) ser colocado(s) de 1,5 cm a 2 cm abaixo do fundo uterino. A passagem do cateter deve ser um movimento delicado, pois as chances de gravidez têm muita ligação com este momento. Trata-se de um procedimento simples, mas que exige tranquilidade, um bom relaxamento da paciente e experiência do profissional. Após essa etapa, a paciente deverá ficar deitada por alguns minutos, retornando, posteriormente, para casa liberada a fazer atividades físicas limitadas, e orientada com as devidas medicações.
TRANSFERÊNCIA DE EMBRIÕES
 |
Decisões importantes para o dia o dia “D”
1- avaliação da qualidade dos embriões e escolha do dia da transferência (3º ou 5º dia?): no dia seguinte à fertilização, que ocorre horas após a aspiração dos óvulos, os embriões são analisados para verificar qual a porcentagem dos óvulos maduros que foram fertilizados. Na maioria das vezes, mesmo nos casos de ICSI, uma parte desses óvulos não se fertiliza. Já neste momento pode ser feita uma análise inicial microscópica e prognóstica da qualidade desses embriões e quais são os que têm maior chance de sobreviver e alcançar um estágio mais avançado de divisão celular. No terceiro dia, os embriões são mais uma vez estudados para que se faça uma nova classificação dos melhores. A classificação é baseada na “morfologia”.
Na morfologia do embrião de terceiro dia (D3), dois itens são analisados: o número de células (deverá ser de 6 a 8) e o índice de fragmentação. Quanto menor o grau de fragmentação e número adequado de células, teoricamente, melhor será este embrião e maior será a chance de implantação. Neste dia serão conhecidos os de melhor qualidade e, assim, o médico especialista, o embriologista e o casal decidirão juntos quantos deles serão transferidos, número este que pode variar de um a quatro, e que dependerá das regras da ética, da idade da mulher e da qualidade dos embriões.
Comentário importantíssimo: ao classificarmos um embrião de melhor ou pior, não estamos concluindo que as crianças nascidas deles terão saúde diferente umas das outras. Significa simplesmente que, ao implantar os embriões que passaram pelo período de divisão celular inicial com facilidade, a chance de gerar uma gravidez deve ser estatisticamente maior. O embrião morfologicamente “mais feio” (menos células e mais fragmentado) poderá ter uma chance menor de implantação, mas gerar uma criança 100% saudável. Se no terceiro dia após a fertilização tivermos um número excessivo de embriões (superior a três), uma boa conduta é aguardarmos que esses embriões atinjam a fase de blastocistos (D5) para que os melhores passem por mais essa prova de seleção. Assim, no quinto ou sexto dia, os embriões que atingirem essa fase serão os que terão maior chance de implantação. E, mais uma vez, a decisão do dia da transferência será feita após a coleta dos óvulos e no decorrer do desenvolvimento dos embriões no laboratório. Dependerá de algumas variáveis importantes, por exemplo, idade da paciente e número de tentativas anteriores entre outras possibilidades.
Blastocistos: geralmente a melhor opção. Normalmente, por vias naturais, o embrião chega à cavidade uterina com cinco ou seis dias de vida, em um estágio chamado blastocisto. Assim, parece claro que, quando transferimos para a mulher embriões neste estágio (ou seja, cinco ou seis dias após a coleta dos óvulos, a chance de gravidez deve ser maior). Além do mais, como existe uma perda considerável no número de embriões durante esses cinco dias de desenvolvimento, ao se transferir um blastocisto, temos a garantia que ele já atingiu esta fase de desenvolvimento mais avançada em relação ao embrião de terceiro dia. Quando serão vitrificados, podemos ainda esperar até sete dias para ver se chegam à fase de blastocisto. Entretanto, nem sempre conseguimos que o embrião chegue a este estágio no laboratório e sabemos que muitos embriões serão perdidos.
AVALIAÇÃO MORFOLÓGICA DO EMBRIÃO ATÉ O 5º DIA DE DESENVOLVIMENTO

2- Quantos embriões devem ser transferidos?
O Conselho Federal de Medicina (CFM), desde a resolução CFM nº 1.957/2010 (Normas Éticas para a Utilização das Técnicas de Reprodução Assistida), definiu:
“O número máximo de embriões a serem transferidos para o útero não pode ser superior a quatro e são feitas as seguintes determinações:
- Mulheres com até 35 anos: até dois embriões;
- Mulheres entre 36 e 39 anos: até três embriões;
- Mulheres com 40 anos ou mais: até quatro embriões.”
Essa norma é importante para diminuir o número de gestações múltiplas, fixando um número máximo de embriões de acordo com a idade. Como quanto maior a idade da mulher, menor a chance de implantação, podemos colocar mais embriões naquelas com idades mais avançadas. Entretanto, não se leva em conta a qualidade do embrião e se ele está em D3 ou blastocisto. Como blastocistos apresentam maior taxa de implantação que em D3, tendemos a colocar um menor número de embriões nesta fase. Hoje em dia, com a alta tecnologia empregada nos tratamentos de fertilização, a recomendação é transferir um, no máximo dois blastocistos, mas a decisão deverá ser individualizada para cada caso.
Outras preocupações que serão discutidas mais à frente: biópsia embrionária e vitrificação dos embriões.
6ª fase Suporte hormonal
Após a coleta dos óvulos, se a mesma paciente for transferir os embriões neste ciclo, iniciamos o suporte de fase lútea com progesterona e estradiol, se necessário. As opções são semelhantes na descrita no preparo endometrial, mas em geral em doses menores.
Quando a paciente tiver poucos óvulos, o suporte da fase lútea poderá ser feito com três doses de hCG 1.500U SC a cada três dias. Não se deve utilizar hCG para suporte na fase lútea se o número de óvulos for maior pelo risco de Síndrome de Hiperestimulação Ovariana.
Após a transferência, independente de ciclo fresco ou de congelado, realizamos um controle rigoroso das condições hormonais a fim de mantê-los em níveis satisfatórios para um adequado desenvolvimento embrionário intrauterino. As doses recomendadas desses hormônios são ajustadas de acordo com a necessidade da paciente e variam.
Durante a fase lútea, podem ser realizados exames de sangue que comprovam o equilíbrio hormonal (estradiol > 200 pg/mL e progesterona > 20 ng/mL). Caso haja necessidade, as doses da progesterona poderão ser modificadas e/ou introduzido reposição de estradiol, caso já não esteja sendo feita.
O dosagem de beta-hCG é realizado 10 a 12 dias após a transferência dos embriões e, se confirmar gravidez, o suporte hormonal deverá ser mantido até o terceiro mês de gestação.
Diagnóstico da gestação: após cerca de 10 dias contados a partir da transferência dos embriões para o útero, a paciente deverá realizar um exame de sangue (dosagem de beta-hCG) para confirmar a gravidez. Se positivo, repetimos o teste uma semana depois para saber se está subindo adequadamente e após 2 semanas do primeiro teste, realizamos que por ultrassonografia uma semana após o teste inicial para confirmarmos se a gravidez está tópica (dentro do útero), quantos embriões implantaram e se tem batimentos cardíacos (gravidez clínica). Daí em diante, repetimos o ultrassom a cada duas semanas até completar 12 semanas, quando então a paciente deve seguir seu pré-natal como uma gestação espontânea.
Este texto foi extraído do e-book “Mulheres Maduras”.
Faça o download gratuitamente do e-book completo clicando no botão abaixo: