O que são miomas uterinos?
Miomas uterinos, também chamados leiomiomas ou fibromas, são tumores benignos do útero que se desenvolvem a partir do músculo liso uterino (miométrio). Estão presentes em até 30% das mulheres em idade fértil, surgindo com mais frequência entre 35 e 40 anos. Aos 50 anos, chega a acometer 70% das mulheres. São assintomáticos na maioria das pacientes, mas podem levar a manifestações importantes como hemorragia, desconforto abdominal, alterações urinárias, dor e infertilidade. A presença ou não dessas alterações vai depender do tamanho do mioma e da sua localização no útero.
Os miomas uterinos constituem a principal causa de histerectomia (cirurgia para retirada do útero), sendo a miomectomia a segunda cirurgia mais comum. Pelo seu caráter invasivo, estes procedimentos podem acarretar consequências na fertilidade das pacientes e, por isto, é urgente explorar alternativas menos agressivas e radicais que permitam à mulher preservar a sua capacidade reprodutiva.
ESSE É UM CONTEÚDO EXTENSO PARA QUE VOCÊ TENHA TODOS OS DETALHES QUE FAZEM A DIFERENÇA!
Etiologia e Fatores de Risco
Etiologia
Índice
ToggleNão temos uma etiologia definida para os miomas, mas vários estudos identificaram fatores associados ao seu desenvolvimento. Os que seguem são os que exibem uma relação de maior importância com a doença:
- Fatores genéticos: 40% dos miomas apresentam, em suas células, anomalias cromossômicas detectáveis (translocações, deleções e trissomias).
- Fatores hormonais: as evidências sugerem que os estrógenos e a progesterona promovem o seu desenvolvimento, por isso aparecem na idade fértil e regridem na menopausa.
- Fatores de crescimento: substâncias produzidos pelas células musculares lisas e fibroblastos promovem o crescimento dos miomas.
Fatores de Risco
Têm sido apontados vários fatores de risco para o desenvolvimento de miomas uterinos:
- Idade (entre quarta e quinta década de vida)
- Fatores hormonais: menarca (primeira menstruação) precoce e menopausa tardia
- História familiar (1º grau)
- Raça negra
- Obesidade
- Hipertensão
- Dieta: alguns estudos apontam alta ingesta de carne vermelha como fator de risco e dieta rica em vegetais, como fator protetor, mas não é clara esta relação.
- Nuliparidade
Classificação Anatômica
Os miomas podem ser classificados segundo a sua localização anatômica, relativamente às camadas musculares uterinas. Existem três tipos de miomas, de acordo com a localização:
• Intramurais (75%): localizados predominantemente na camada miometrial.
• Subserosos (20%): localizados logo abaixo da serosa (membrana que reveste externamente o
útero).
• Submucosos (5%): localizados abaixo do endométrio (tecido que reveste internamente o
útero), com projeção para a cavidade uterina.
Apesar desta classificação ser amplamente usada, é comum que os miomas tenham mais do que uma localização e, embora na maioria dos casos estes se desenvolvam no corpo uterino, existe a possibilidade destes surgirem no colo do útero e no ligamento largo (ligamento lateral ao útero).
Os miomas podem ser únicos ou múltiplos e ser classificados segundo uma outra localização anatômica mais detalhada. Na literatura, podemos encontrar diferentes tipos de classificação atendendo à localização dos miomas. Quando o intuito é essencialmente terapêutico, a classificação da European Society of Gynecologic Endoscopy (ESGE) e da International Federation of Obstetrics and Gynecology (FIGO) permite estabelecer uma estratégia de abordagem mais bem definida (cirúrgica ou clínica). Esta classificação permite um planejamento objetivo da necessidade ou não de um tratamento cirúrgico da paciente, bem como as possíveis dificuldades na resolução do problema e, principalmente, as implicações no comprometimento da fertilidade.
CLASSIFICAÇÃO DOS MIOMAS (FIGO – PALM – COEIN)
Os miomas são habitualmente assintomáticos (>50% dos casos), pelo que, muitas vezes, são achados ocasionais do exame pélvico ou ecográfico. Quando existem, os sintomas relacionam-se com o tamanho, número e localização dos miomas. Os subserosos tendem a causar compressão e distorção anatômica de órgãos adjacentes, os intramurais causam sangramento e dismenorreia, enquanto os submucosos produzem frequentemente sangramentos irregulares e estão mais associados à disfunção reprodutiva.
Mioma e Fertilidade
A relação entre miomas e infertilidade sempre foi motivo de debate. Acredita-se que miomas podem estar presentes em 5-10% dos casais inférteis, mas somente em 1-2,4% como causa isolada da infertilidade. A principal razão para o mioma prejudicar a fertilidade é quando ele distorce a cavidade endometrial, levando à dificuldade de implantação e maior chance de aborto. Isso ocorre principalmente quando miomas são submucosos, independentemente do tamanho. Neste caso, o mioma pode bloquear o espermatozoide de fertilizar o óvulo, interferir no fluxo sanguíneo endometrial (prejudicando ou causando sangramento) e causar um processo inflamatório local. Com isso, pode haver prejuízo na chance de fertilização dos óvulos, implantação do embrião ao útero e maior a chance de aborto.
Os miomas classificados como submucosos são os que mais afetam a fertilidade. Os outros tipos, localizados em outras áreas do útero nem sempre interferem nesta capacidade reprodutiva, mas dependendo da sua localização no útero podem afetar negativamente a vida reprodutiva da mulher. Deve-se sempre levar em consideração a idade do paciente, a história da infertilidade, abortos espontâneos anteriores e o tamanho do mioma.
Miomas intramurais estão menos associados à infertilidade, mas quando grandes e próximos à cavidade endometrial também podem deformar a arquitetura uterina ou causar alterações circulatórias locais, processo inflamatório e liberação de citocinas, prejudicando a implantação dos embriões. Quando próximos dos óstios tubários, podem também obstruí-los, dificultando uma gravidez espontânea. Miomas intramurais podem ainda levar à disfunção na contratilidade uterina, prejudicando o transporte dos espermatozoides. Miomas subserosos em geral não atrapalham a fertilidade.
Diagnóstico
EXAME FÍSICO
Nem sempre os miomas podem ser detectados por exame físico, entretanto, um exame físico cuidadoso e detalhado pode ser muito útil no diagnóstico desta patologia.
Assim, existem 3 aspetos essenciais:
- Inspeção e palpação do abdome em que os maiores miomas podem facilmente ser detectados;
- Exame com espéculo: permite diagnóstico de miomas cervicais e paridos (miomas submucosos que se exteriorizam pelo colo);
- Toque bimanual: miomas subserosos e intramurais podem ser detectados por um útero aumentado de forma irregular, com massas bem delimitadas de consistência duro-elástico.
Miomas pequenos, em geral, não são percebidos ao exame físico
EXAME POR IMAGEM
Com o desenvolvimento de novas armas terapêuticas menos invasivas e mais adaptadas às necessidades da mulher, observa-se a necessidade de definir com exatidão as características, localização e mapeamento dos miomas. Para atingir este objetivo, é necessário recorrer a exames de imagem, que possam ser mais precisos para distinguir as lesões potencialmente malignas das benignas. Conhecer as alterações anatômicas produzidas por esta patologia é essencial para a conclusão do diagnóstico e a terapêutica futura quando necessária.
ULTRASSONOGRAFIA TRANSVAGINAL
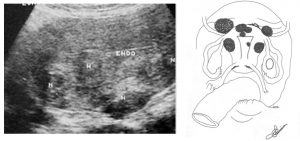
É o exame gold standard (padrão-ouro) para avaliação inicial da paciente com miomas uterinos. É fácil de usar, é segura, tem baixo custo (comparativamente a outros exames de imagem) e está facilmente disponível. Contudo, a sua sensibilidade depende do aparelho de ultrassom e do médico examinador. Ecograficamente, os miomas surgem tipicamente como lesões nodulares sólidas hipoecogênicas com origem na camada miometrial. Na maioria das vezes, ultrassonografia pélvica transvaginal é suficiente na identificação e no diagnóstico diferencial entre miomas uterinos e outras patologias pélvicas. A sensibilidade, especificidade e valor preditivo positivo do uso de sonda abdominal, em associação com a sonda endovaginal no diagnóstico de miomas uterinos chega a 90-98%. A sensibilidade da ultrassonografia aumenta com o uso de sondas com maior frequência e diminui nos casos de úteros muito volumosos, nos que contêm múltiplos nódulos de mioma e também quando os miomas são pequenos ou subserosos. Não é igualmente um método preciso para a distinção entre leiomiomas, leiomiosarcomas e adenomiose.
ULTRASSOM MOSTRANDO ÚTERO COM MIOMAS E UM DESENHO ESQUEMÁTICO
HISTEROSSONOGRAFIA
Histerosonografia (HSoG) é um exame de ultrassom em que é inserido através da vagina um pequeno cateter dentro do útero para ser injetado uma solução fisiológica. Esta técnica aumenta a sensibilidade na detecção de miomas submucosos. A instilação de solução salina intrauterina, na histerossonografia, providencia contraste e uma melhor definição dos miomas submucosos, pólipos, hiperplasia endometrial ou carcinoma.
Enquanto que a sensibilidade e especificidade na detecção de lesões endometriais focais é de 70% e 96%, respectivamente, quando usamos apenas ecografia transvaginal, quando recorremos à HSoG, a sensibilidade aumenta para 90%. Atualmente, aceita-se que a HSoG é uma das técnicas mais sensíveis para avaliar e orientar as cirurgias endoscópicas dos miomas submucosos.
No caso de crescimento rápido dos miomas, a fluxometria poderá auxiliar no diagnóstico diferencial com leiomiosarcoma, embora estudos recentes não sejam unânimes nesta afirmação.
TOMOGRAFIA COMPUTADORIZADA (TC)
Tem um papel muito limitado no diagnóstico de miomas uterinos. Não permite o diagnóstico diferencial com segurança entre miomas uterinos e outras massas uterinas ou cervicais. O achado mais frequente é o aumento do tamanho uterino ou deformidade dos seus contornos. A presença de calcificação é o sinal mais específico, mas é encontrado em menos de 10% dos casos.
RESSONÂNCIA MAGNÉTICA
É o método de imagem mais fidedigno no diagnóstico, mapeamento e caracterização dos miomas uterinos, tendo-se tornado no complemento da ecografia em casos selecionados, ultrapassando as suas limitações.
Trabalhos bem conduzidos afirmam que se trata de um exame menos dependente do operador, logo, mais reprodutível.
Apesar do elevado custo, a ressonância magnética é um exame seguro, com baixa variabilidade entre observadores na interpretação de imagens, que permite uma excelente visualização de praticamente todos os miomas em úteros volumosos. Tem especial utilidade no diagnóstico diferencial com adenomiose e na distinção entre massas benignas e malignas.
RESSONÂNCIA NUCLEAR MAGNÉTICA MOSTRANDO MIOMA VOLUMOSO
Ressonância com cine-mode-display: é uma ressonância nuclear magnética com um software capaz de medir as contrações uterinas e sua direção. Recomendamos realizar durante a fase lútea (em geral entre 19º e 26º dia do ciclo), ou seja, após a ovulação, ou após reposição de progesterona, que simula a fase lútea, que tem o efeito de relaxar a musculatura uterina. Pode ser útil em pacientes em tratamento de reprodução assistida.
VÍDEO-HISTEROSCOPIA DIAGNÓSTICA
A vídeo-histeroscopia consiste na introdução de um tubo fino com fibra óptica através do colo uterino, tendo assim, uma visão do seu interior. Como permite a inspeção da cavidade uterina, é o melhor método diagnóstico para miomas submucosos, sendo possível distingui-los de pólipos. A sua grande vantagem, relativamente aos outros métodos, é a capacidade de determinar a viabilidade para a excisão.
VÍDEO-HISTEROSCOPIA MOSTRANDO MIOMA SUBMUCOSO
HISTEROSSALPINGOGRAFIA (HSG)
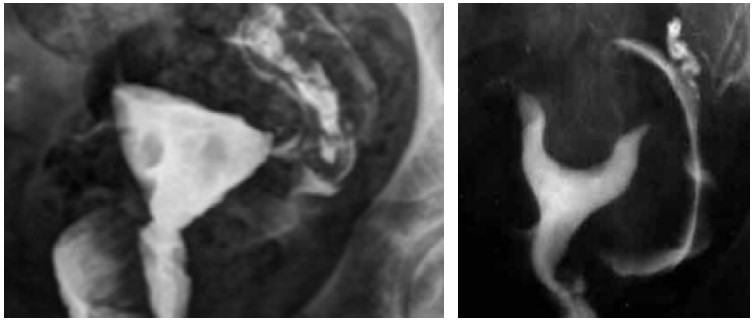
É um raio X após injeção de contraste dentro do útero. Com isso, consegue-se avaliar a integridade da cavidade uterina (sinéquias, miomas, pólipos, malformações uterinas), além da permeabilidade das tubas uterinas. É geralmente realizada quando o mioma está relacionado à infertilidade, por ser um exame muito útil na avaliação das trompas. Para avaliação exclusiva da cavidade uterina, histeroscopia tem melhor sensibilidade e especificidade.
HISTEROSSALPINGOGRAFIAS MOSTRANDO FALHAS DE ENCHIMENTO NA CAVIDADE UTERINA SUGESTIVAS DE MIOMAS SUBMUCOSOS.
Tratamento clínico dos miomas
Tratamento Clínico Convencional
O tratamento clínico convencional consistem em medicações que diminuem sangramentos em geral (anti-inflamatórios e ácido tranexâmico) ou medicamentos hormonais que bloqueiem a menstruação (como anticoncepcionais orais e injetáveis). Neste último grupo, pode-se utilizar anticoncecpionais combinados (com estradiol e progestágenos) ou progestágenos isolados. O principal objetivo do tratamento clínico é o de controlar sintomas (hemorragia e cólicas) e não a redução ou desaparecimento dos nódulos. As pacientes assintomáticas não se beneficiam deste tratamento, uma vez que estamos tratando sintomas. Pacientes com miomas volumosos, sintomas de compressão de órgão vizinhos e aumento de volume abdominal, também não terão benefício. Como são medicações contraceptivas, são pouco indicados em pacientes que desejam engravidar ou serão submetidas a tratamentos de fertilização.
DIU medicado com levonorgestrel (Mirena®)
Uma outra opção de uso de progestágenos é através do Sistema de liberação intrauterina com levonorgestrel (SIU-LNG), um progestetágeno também derivado da 19-norprogesterona. que vem se tornando uma excelente opção para controle de sengramento uterino, além de contracepção. Além de alta taxa de amenorreia (ausência total de menstruação), tem pouca absorção sistêmica, além da facilidade de precisar ser trocado somente após 5 anos. Muitos estudos confirmaram melhora no sangramento e correção de anemia. Em relação ao volume uterino e tamanho dos miomas, existem controvérsias mas não parece haver diminuição significativa. Vale a ressalva que, mulheres com miomas grandes também podem ter uma expulsão espontânea do SIU. O dispositivo, portanto, pode ser mais adequado para uma cavidade uterina não distorcida e um tamanho uterino inferior a 12 semanas.
Danazol
O danazol é um esteróide químico sintético do isoxazol associado à 17-α-etiniltestosterona que cria um ambiente hormonal rico em androgênios (hormônios masculinos) e com pouco estrogênio, resultando na diminuição do tamanho de miomas e atrofia uterina. O mecanismo de ação baseia-se no bloqueio do eixo hipotálamo-hipófise-ovário, inibindo a hipófise a produzir gonadotrofinas, hormônios que, por suavez, estimulariam o ovário a produzir estrogênios. O efeito anti-estrogênico do agente é o provável mecanismo de sua eficácia no manejo dos miomas e pelo seu carácter androgênico, muitos pacientes abandonam a terapêutica devido a efeitos colaterais significativos: acne, hirsutismo, aumento de peso, irritabilidade, dor músculo-esquelética, afrontamentos e atrofia mamária. Estes efeitos influenciam a qualidade de vida das pacientes e podem ser minimizados por uma correta prescrição com doses relativamente baixas. Não há estudos randomizados que abordem os riscos e benefícios no uso de danazol no tratamento de miomas, pelo que, apesar dos benefícios na redução do seu tamanho e sintomatologia, a escolha por parte do médico deve ser cautelosa.
Inibidores da aromatase
A aromatase é uma enzima microssomal que catalisa a conversão de androgênios em estrogênios e cuja expressão se encontra aumentada nos leiomiomas. Assim sendo, o uso dos seus inibidores no tratamento desta patologia permitiria uma rápida redução dos estrogênios, levando a diminuição do tamanho dos miomas e consequente sintomatologia.
Fármacos de 3ª geração como o letrozol (2,5mg) e o anastrazol (1mg) têm sido utilizados, tendo alguns estudos demonstrado que seu uso diário durante 3 ciclos reduziu o tamanho dos miomas e o volume uterino total. Segundo estes autores, a eficácia deste tipo de tratamento é semelhante a análogos de GnRH com a vantagem de ter menos efeitos colaterais. Entretanto, apesar de alguns estudos randomizados sugerirem sua eficácia no tratamento de miomas, uma revisão sistemática da Biblioteca Cochrane, de 2013, não encontrou resultados que fundamentem seu uso para tratamento de miomas.
Agonistas do GnRH (hormônio liberador de gonadotrofina)
Os agonistas da GnRH (GnRH-a) induzem uma diminuição dos níveis de estrogênios e progesterona levando a um estado pseudo-menopáusico, sendo esta a base que fundamenta a diminuição do volume dos miomas. O mecanismo de ação dos análogos da GnRH no tratamento dos miomas uterinos está relacionado com: 1) inibição do eixo hipotálamo-hipófise-ovário, suprimindo a libertação hipofisária das gonadotrofinas e, consequentemente, a produção ovárica de esteroides sexuais (mecanismo indireto); 2) inibição da expressão da enzima aromatase, com diminuição da produção estrogênica in situ (efeito direto).
Sua ação se dá pela ocupação dos recetores hipofisários do GnRH, levando, numa primeira fase, à liberação das reservas hipofisárias de LH e FSH – efeito flare up. Posteriormente, através de um processo de down-regulation dos receptores, leva à supressão da sua produção. Na prática, induzem amenorreia e uma rápida diminuição do volume dos miomas (até 65%), com efeito máximo ao fim de 3 meses de tratamento. As principais desvantagens dos GnRH-a são os efeitos secundários, que impossibilitam o seu uso a longo prazo: sintomas de hipoestrogenismo (ondas de calor, secura vaginal, falta de libido, irritabilidade…), diminuição da densidade óssea e distúrbios no perfil lipídico. Tem-se proposto a combinação de hormônios esteroides (estroprogestativo ou tibolona) para controle de efeitos colaterais, entretanto, o tratamento a longo prazo (superior a 6 meses) não é recomendado. Além disso, apesar de Shaw e colaboradores sugeriram uma redução de 77% do volume uterino após 3 meses de tratamento, a suspensão do tratamento resulta num rápido crescimento dos miomas e útero nos 4 a 6 meses seguintes. Assim, sua principal indicação está no uso pré-operatório. O seu uso durante 3 a 4 meses antes da cirurgia visa estabilizar hemodinamicamente a doente, reduzir o volume uterino e dos miomas, facilitando a intervenção cirúrgica, minimizando as perdas de sangue intraoperatórias e reduzindo os tempos de internação. Além disso, induz ainda um estado de amenorreia, que é particularmente útil na reversão dos casos de anemia ferropriva induzida pela menorragia, minimizando a necessidade de transfusão sanguínea. Um ponto contra o uso GnRH-a pré-operatório para cirurgias conservadoras é que pode levar a dificuldades na definição do plano de clivagem (entre mioma e miométrio) durante a abordagem cirúrgica. Entre as opções terapêuticas estão:
- acetato de gosserrelina: Zoladex® 3,6 mg (mensal) e Zoladex LA® 10,8 mg (trimestral)
- acetato de euprorrelina: Lupron Depot® , Lectrum® ou Lorelim® 3,75 mg (mensal). E Lupron Depot® 11,25 mg (trimestral).
Moduladores Seletivos da Progesterona (SPRMs – selective progesterone receptor modulator)
São substâncias sintéticas derivadas dos esteroides que têm a capacidade de ocupar os receptores da progesterona e passam a ter ação como antagonistas, agonistas-antagonistas ou agonistas desse hormônio, dependendo do tecido-alvo. Essas variedades de ações favorecem a utilização dessas substâncias para o tratamento da miomatose uterina e endometriose, entre outras, tendo também importante aplicação na anticoncepção e na reprodução assistida. O mecanismo de ação dos SPRM não está completamente elucidado, uma vez que intercalam efeitos sinérgicos e antagônicos aos da progesterona. Entretanto, sabe-se que têm efeito antiproliferativo, antiangiogênico, aumentam os índices de apoptose (morte celular) e promovem uma diminuição do aporte sanguíneo das artérias uterinas e dos vasos espiralados do endométrio. Ainda não estão disponíveis no Brasil. Entre os que tem demonstrado resultado está o Elagolix.
Tratamento cirúrgico dos miomas – Indicação
É importante avaliar cuidadosamente os benefícios e os riscos da cirurgia que se propõe a ser feita. Antes de oferecer qualquer procedimento a um paciente é essencial uma avaliação rigorosa da sua história reprodutiva, um estudo completo da infertilidade, abortos recorrentes, exames laboratoriais, reserva ovariana, investigações como ultrassonografia, ressonância, histeroscopia ou histerossalpingografia. Isso vai ajudar a determinar o tamanho, o número e a localização dos miomas para que se possa chegar à melhor opção de “operar ou não operar” e, no caso da intervenção indicada, qual a melhor via cirúrgica e a melhor técnica. As mulheres devem estar plenamente informadas sobre as várias opções de tratamento e os riscos da intervenção escolhida.
Miomas submucosos
Os miomas submucosos estão localizados dentro da cavidade uterina. São os mais sintomáticos, causando aumento de fluxo e irregularidade menstrual, mesmo com volumes pequenos.
O mioma submucoso é, entre os miomas, o principal causador de abortos e infertilidade e devem ser retirados, principalmente aquelas pacientes que serão submetidas a um tratamento de fertilização in vitro (FIV). Talvez possa existir algum debate quanto a um tamanho mínimo permitido sem a necessidade de cirurgia. No nosso entender, qualquer tamanho de mioma submucoso, deve ser removido. Se for uma causa isolada de infertilidade, sua retirada pode levar à gestação espontânea. Nos casos de FIV, se o mioma for submucoso, a miomectomia prévia à transferência dos embriões é benéfica, melhorando as taxas de gravidez e diminuindo taxas de aborto.
Miomas Subserosos
Os miomas subserosos estão localizados na região externa do útero e são considerados assim quando >50% está do lado externo do útero. Podem ser ainda sésseis ou pediculados (quando estão ligados ao útero externamente por um simples ”talo”). São geralmente assintomáticos, mas podem causar dor, desconforto abdominal e sintomas de compressão de outros órgãos, dependendo do tamanho. Normalmente não causam alteração de fluxo menstrual. Se sintomáticas, a cirurgia pode ser uma boa opção.
Miomas subserosos, principalmente os pediculados não trazem prejuízo à gestação e, em geral, não têm indicação de cirurgia no contexto da infertilidade. Não existem estudos que avaliem a gravidez espontânea na presença isolada de miomas subserosos, nem do impacto da cirurgia destes. Não ha evidência que influenciem a gravidez espontânea, exceto em situações de dimensões muito aumentadas, com distorção anatômica significativa.
Miomas Intramurais
Os miomas intramurais estão localizados na espessura da musculatura do útero e <50% do seu volume está externo da serosa. Se pequenos, são geralmente assintomáticos, mas podem causar dor e hemorragia dependendo do tamanho, número e da posição dentro do útero. O grau de interferência destes miomas na fertilidade continua a ser controverso, principalmente na ausência de sintomas; no entanto, a sua associação a complicações obstétricas tem sido constante.
Miomas intramurais são os que oferecem mais divergência nas indicações cirúrgicas. No contexto puramente da infertilidade, a miomectomia é controversa, embora estudos mostrem que pacientes inférteis portadoras de miomas apresentam maior taxa de gravidez após a cirurgia. Entretanto, é importante saber que a cirurgia pode levar a complicações prejudiciais à fertilidade. Uma delas é o risco de evoluir para uma histerectomia no intraoperatório, impossibilitando uma futura gestação a não ser por útero de substituição, método que tem várias limitações no Brasil. Outra complicação menos grave, mas muito frequente, são as aderências, principalmente quando os miomas forem de localização posterior, que leva maior diminuição da fertilidade. A cirurgia pode causar também o enfraquecimento da parede uterina, com risco de ruptura durante o parto e, mais raramente, durante a gestação. Assim, deve-se sempre ponderar se a intervenção é válida.
QUAIS MIOMAS TRATAR NA INFERTILIDADE
Em geral, miomas que distorcem a cavidade devem ser retirados em pacientes inférteis ou com abortos. Outros autores defendem que, dependendo do tamanho também devem ser retirados independente de distorcer a cavidade. Ramzy e Cols, concluíram que miomas com dimensões inferior a 7 cm e não invadindo a cavidade endometrial não aumentam a taxa de abortos e aqueles maiores de 7 cm ou que estejam invadindo ou deformando a cavidade endometrial normalmente tem indicação de ressecção cirúrgica (miomectomia) de preferência por vídeolaparoscopia. Entretanto não existem evidências que comprovem a real necessidade da intervenção cirúrgica, nestes casos mas, na nossa experiência, a indicação cirúrgica é sensata quando miomas intramurais são maiores que 5 cm.
Quando há múltiplos miomas, a intervenção cirúrgica aumenta o risco de perda uterina e, portanto, deve ser bem pensada. Neste caso, em pacientes que serão submetidas a FIV, uso de análogo do GnRH ou acetato de ulipristal de 3 a 6 meses antes da transferência embrionária é uma boa opção. Com isso, pode haver diminuição dos miomas e aumentar a chance de gravidez, evitando os riscos da cirurgia.
Miomas e contrações uterinas
Em casos de fertilização in vitro (FIV), uma exame que pode ajudar a decidir se devemos ou não operar os miomas antes da transferência dos embriões é a Ressonância cine-mode display. Ela mede as contrações uterinas, que podem estar aumentadas em pacientes com miomas. Este fato pode ser um fator que contribui para as menores taxas de gravidez neste grupo, uma vez que alguns estudos já demonstraram que o embrião transferido pode ser expelido pelo útero após a transferência embrionária, o que se atribui às contrações uterinas. Esses estudos levantaram a hipótese de que, algumas vezes, as contrações uterinas poderiam levar os embriões a serem eliminados pelo colo, trompas ou vagina e isso ser a causa das falhas de implantação.
Um estudo com pacientes com miomas submetidas a FIV demonstrou que aquelas que tinham muitas contrações não engravidaram (de 22 pacientes, nenhuma engravidou). Já das 29 que só tinham 1 contração ou menos, 10 engravidaram (34%). Outro estudo, com 220 ciclos de FIV mediu as contrações uterinas antes da transferência embrionária, dividindo as pacientes em 4 grupos de acordo com a frequência de contrações. Demonstraram que quanto menor o número de contrações, maior a taxa de gravidez e implantação. Enquanto o grupos com menos contrações tiveram um taxa de gravidez de 53%, nas com mais contrações, esta taxa foi de 14%. Outro dado importante neste estudo é que as concentrações séricas de progesterona foram inversamente proporcionais ao numero de contrações, mostrando a importância de um nível adequado desde hormônio.
Esses resultados nos levam a pensar que talvez somente aquelas com muitas contrações devam retirar os miomas intramurais, mesmo sem distorção da cavidade. Outra opção é tentar o uso de Atosiban neste grupo de pacientes.
Atosiban é um antagonista da ocitocina, hormônio cuja ação na musculatura lisa uterina é causar contrações uterinas e muito utilizado em hospital para evitar o parto prematuro. Alguns estudos sugerem ainda que no endométrio também há receptores para ocitocina cuja ação leva à produção de prostaglandinas, substâncias que causam reação inflamatória e contrações uterinas. Assim, foi sugerido que utilização do atosiban durante a transferência poderia diminuir o número de contrações e assim, melhorar a chance de implantação. Para avaliar sua eficácia, um grande estudo randomizado com pacientes submetidas a FIV comparou o uso de atosiban durante a transferência embrionária (400 pacientes) com placebo (400 pacientes) e não encontrou diferença entre os grupos nas taxas de gravidez, aborto ou implantação. Portanto, não utilizamos de rotina esta medicação em todas a paciente.
Entretanto, um novo estudo avaliou somente pacientes com falha de implantação. Elas tinham em média 4,8 tentativas prévias de transferência de embriões de boa qualidade, sem sucesso. Neste estudo, avaliou-se o número de contrações uterinas antes e depois do atosiban e demonstrou uma redução acentuada no número de contrações. Viram ainda que aquelas com um grande número de contrações tiveram uma redução maior com o uso do atosiban. Neste estudo, a taxa de gravidez com uso de atosiban foi de 43,7%, um número bom se levarmos em conta que tiveram múltiplas falhas prévias.
Esses estudos sugerem que nem todas as pacientes se beneficiam com o uso do atosiban, mas talvez somente aquelas com contrações aumentadas.
Miomectomia – Miomas Intrauterinos
Quando optamos pela cirurgia, a escolha da melhor técnica de miomectomia vai depender da localização, do tamanho do mioma e da experiência do cirurgião. As abordagens mais usadas no tratamento destes miomas são a laparoscopia e a laparotomia, sendo a última a mais indicada quando existe suspeita de malignidade e quando os miomas são múltiplos (mais que 3) e de grandes dimensões (>7cm). Apesar de exigir maior competência técnica e tempo operatório, a laparoscopia apresenta menor número de complicações (hemorragia, dor pós-operatória) e permite uma mais rápida recuperação. As taxas de gravidez e recorrência aos 5 anos são similares.
Videoeolaparoscopia
É a via preferencial para a remoção dos miomas. O importante nesta via cirúrgica é o adequado fechamento do miométrio. Uma sutura bem feita é essencial para evitar o risco de rotura uterina em uma gravidez futura. A sutura das camadas do útero deve ser precisa para que o órgão se reconstrua adequadamente e com o mínimo de aderências. Portanto, a videolaparoscopia, pressupõe boa experiência em sutura laparoscópica e requer uma experiência muito grande do cirurgião, caso contrário, a via abdominal (laparotômica) pode ser mais indicada. Existem preocupação em acompanhar estas pacientes durante a gestação pelo ao potencial risco de ruptura uterina durante
o terceiro trimestre de gravidez após o procedimento. A miomectomia laparoscópica tem também a vantagem de causar menos aderências, embora estudos não mostrem diferença nas taxas de gravidez pós miomectomia laparoscópica comparada com a laparotomia. A intervenção em casos de miomas maiores pode ser precedida da ligadura das artérias uterinas, o que diminui sangramentos e recidiva sem prejudicar a fertilidade. A cirurgia robótica vem crescendo por apresentar maior facilidade operatória e permitir suturas mais precisas. As técnicas podem ainda ser combinadas: videolaparoscopia + mini-laparotomia. A ruptura uterina durante a gravidez após miomectomia laparoscópica foi atribuída à reconstrução inadequada do miométrio durante a cirurgia. Para aqueles que desejam a concepção, recomenda-se um atraso de 4-6 meses antes de tentar a gravidez após a miomectomia para permitir a cicatrização miometrial.
Miomectomia aberta (LAPAROTOMIA)
A miomectomia por laparotomia deve ser a via de escolha quando houver grandes miomas intramurais ou subserosos (> 7 cm), ou quando houver expectativa de múltiplas aderências. Há casos, ainda, que se tenta realizar por laparoscopia mas tem que se converter para laparotomia. Os cuidados com a hemostasia e com as suturas devem ser os mesmos que na videolaparoscopia, assim, como a recomendação de aguardar 4-6 meses após a cirurgia para engravidar. Quanto ao pós operatório, há mais dor, maior tempo de recuperação e maior risco de infeção com a via lapartoômica. A taxa de recorrência é semelhante à miomectomia laparoscópica.
Miomectomia – Miomas Submucosos
Miomas submucosos devem ser retirados por um cirurgião especializado em videohisteroscopia. A histeroscopia cirúrgica é um procedimento cirúrgico em que o material de ressecção entra pelo colo do útero juntamente com uma câmera e o mioma é retirado sem necessidade de incisão cirúrgica (cicatriz). Com experiência, é um procedimento com relativa facilidade de execução, com baixo risco de complicações e uma morbidade mínima, tornando-se o tratamento de escolha para miomas submucosos. Entretanto, há casos em que a via histeroscópia pode ser de difícil execução, devendo se pesar o custo benefício dessa técnica.
MIOMAS INTRACAVITÁRIOS
A localização dos miomas submucosos e as taxas de gravidez
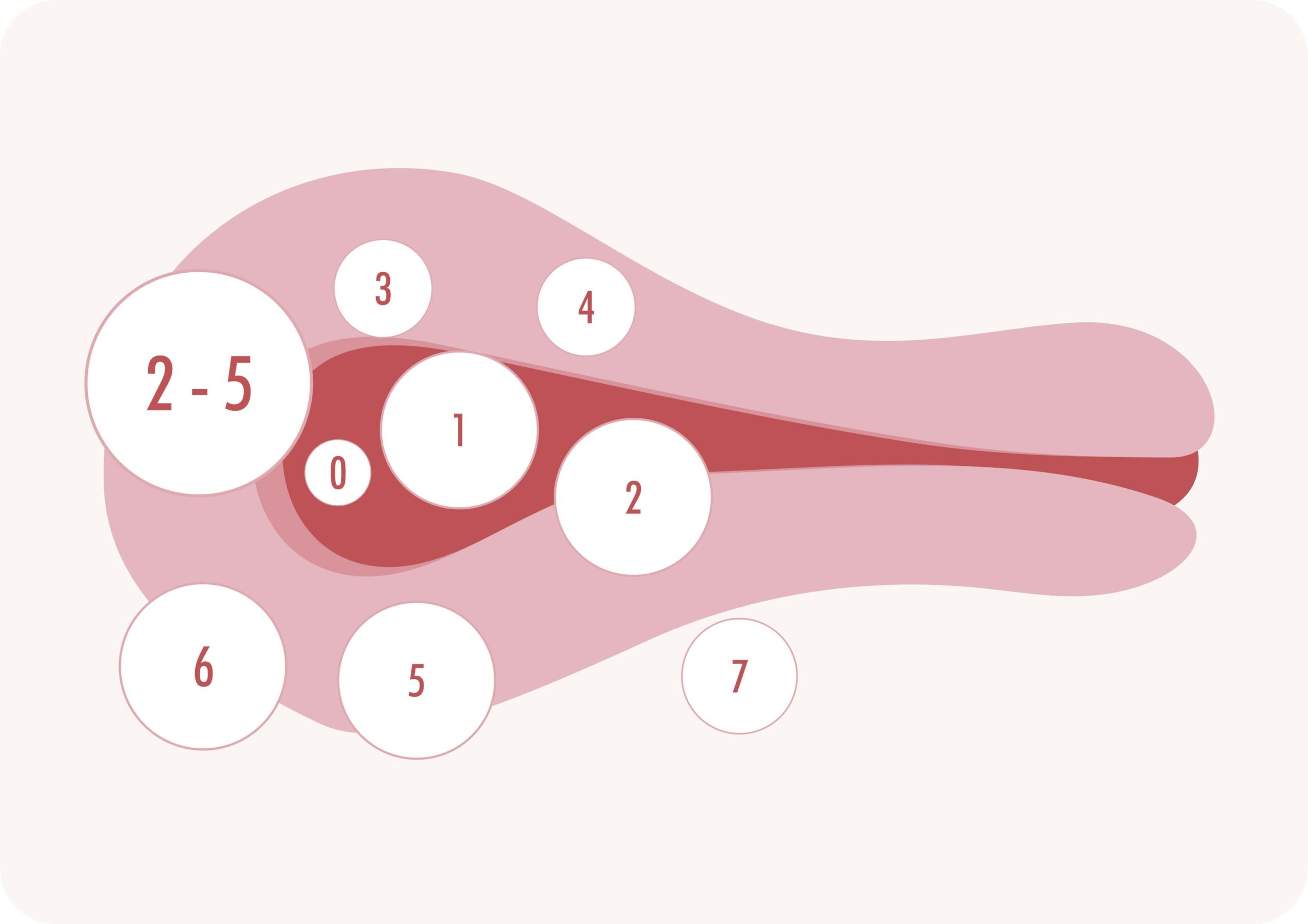
Para uniformizar os diagnósticos, tornando mais fácil a avaliação dos resultados terapêuticos e do prognóstico cirúrgico, foram criadas várias classificações para estes miomas. A classificação mais usada é a da Sociedade Europeia de Endoscopia Ginecológica (ESGE) que denomina os diferentes tipos de miomas submucosos com base na sua localização e divide em três subtipos avaliados por ultrassonografia, ou por histeroscopia. Este sistema de classificação para miomas submucosos visa estabelecer um estadiamento pré-operatório (Tabela 1) e quantifica a profundidade da extensão dos miomas submucosos em relação ao miométrio (Figura 1).
Nesta classificação, o mioma que se encontra totalmente protuso na cavidade uterina recebe o escore 0; o que tem sua maior porção na cavidade uterina e menor porção no miométrio recebe o escore 1 e aquele que tem a sua maior parte no miométrio recebe o escore 2 (Figura 1).
Figura 1
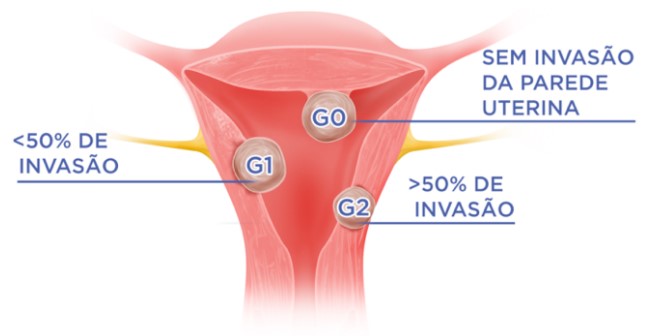
- G 0: mioma na cavidade uterina em toda a sua extensão (pediculado);
- G I: mioma maioritariamente na cavidade uterina, sendo o componente intramural inferior a 50% do seu volume (séssil);
- G II: mais de 50% do volume do mioma é intramural (séssil).
A miomectomia por histeroscopia é o tratamento mais adequado para os miomas submucosos pela menor morbidade cirúrgica e porque preserva o útero e estruturas adjacentes, algo importante em mulheres em idade reprodutiva. Este procedimento é adequado em fibromas tipo 0, I e II (até 4cm), mas deve dar lugar a miomectomia abdominal, quando se prevê grande manipulação uterina (miomas múltiplos, de grandes dimensões, tipo II) em mulheres que queiram engravidar.
Sempre que os miomas forem sintomáticos, mesmo após a menopausa, nas mulheres que desejam engravidar por ovodoação, devem ser sujeitos a intervenção. A excisão completa associa-se aos melhores resultados.
Quanto a miomas assintomáticos, a retirada histeroscópica está indicada quando existe deformação da cavidade uterina nestas mulheres que pretendam engravidar. Qualquer mulher que se submeta a tal cirurgia deve ser informada da possibilidade de existir uma segunda intervenção devido a excisão incompleta ou recorrência dos miomas e/ou sintomatologia (20-25% em 5 anos)
As técnicas (secção, vaporização ou morcelação) usadas devem levar em conta as características de cada paciente. Na preparação pré-cirúrgica, pode ser aconselhada a prescrição de agonistas do GnRH para corrigir anemia subjacente ou outros medicamentos já descritos.
A miomectomia histeroscópica tem mostrado grandes vantagens: procedimento pouco invasivo, realizado em centro cirúrgico ambulatorial, que permite uma rápida recuperação com poucas complicações (<5%) e que rapidamente permite a gravidez.
Considerações importantes sobre a viabilidade da miomectomia histeroscópica
A viabilidade da miomectomia histeroscópica é geralmente determinada pela combinação de diferentes características do mioma: localização, tamanho, margem miometrial livre e profundidade da extensão intramiometrial, sendo este último aspecto geralmente considerado como a característica mais importante na determinação da factibilidade cirúrgica histeroscópica. Um planejamento pré-cirúrgico adequado para a miomectomia é de grande importância, visto que fatores como grau de dificuldade operatória, tempo cirúrgico, balanço hídrico e taxas de complicações estão diretamente relacionadas com essas diferentes características. As taxas de falha e dificuldade operatória para a ressecção histeroscópica parecem estar relacionadas diretamente com esta classificação mais específica. Dessa forma, um adequado mapeamento pré-operatório da extensão do envolvimento miometrial dos nódulos é necessário na seleção apropriada dos casos para a cirurgia endoscópica. A histeroscopia diagnóstica associada à ultrassonografia endovaginal e à ressonância magnética dão uma idéia precisa do comprometimento da cavidade endometrial e do grau de profundidade no miométrio.
Classificação de Lasmar
A classificação proposta por Lasmar conhecida como STEPW (Size, Topography, Extension, Penetration, and lateral Wall) tem como base a análise subjetiva dos parâmetros que tornavam a cirurgia mais difícil. Foram considerados QUATRO critérios:
- Penetração do nódulo no miométrio
- Extensão da base do nódulo em relação à parede do útero
- Tamanho do nódulo em centímetros
- Topografia do mioma e acometimento da parede lateral
Penetração do nódulo no miométrio
Para avaliação da penetração do nódulo no miométrio utiliza-se a mesma sistemática da ESGE) , na qual o mioma que se encontra totalmente protuso na cavidade uterina recebe o escore 0; o que tem sua maior porção na cavidade uterina e menor porção no miométrio recebe o escore 1 e aquele que tem a sua maior parte no miométrio recebe o escore 2 (Figura 2).
Figura 2

Extensão da base do nódulo em relação à parede do útero
A avaliação da extensão da base do nódulo em relação à parede do útero leva em consideração a parede em que está localizado o mioma, separando-a em ístmica, corporal e fúndica. Correlaciona-se a extensão da base do nódulo com a parede acometida e assim temos as seguintes possibilidades: quando o mioma acomete um terço ou menos da parede, recebe o escore 0; quando a base do nódulo ocupa de um terço a dois terços da parede, o escore é 1; e quando ele acomete mais de dois terços da parede, tem
o escore 2 (Figura 3).
Figura 3

Tamanho do nódulo
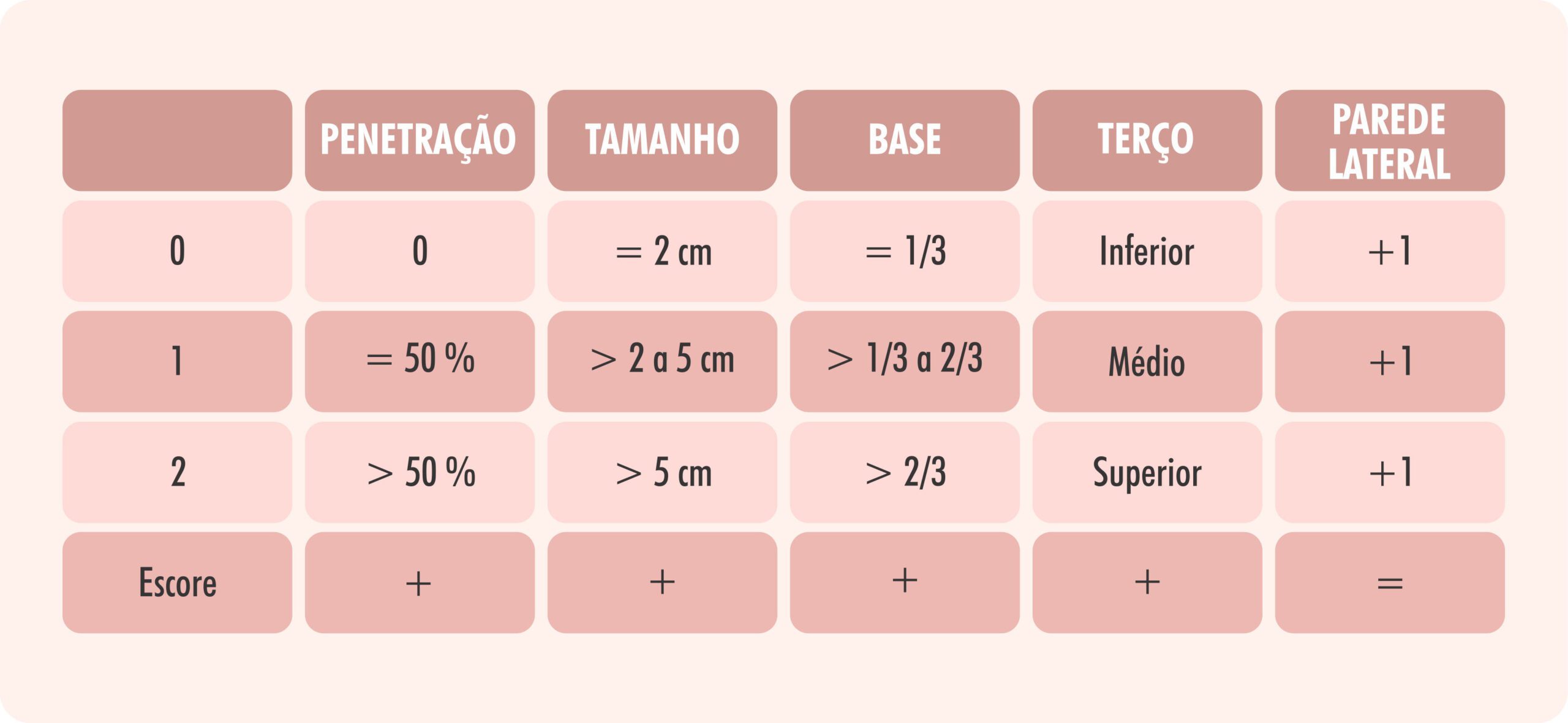
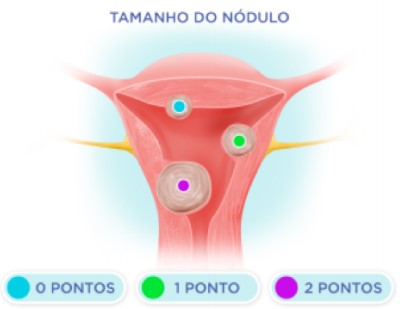
O tamanho considerado é o maior diâmetro encontrado em qualquer um dos exames de imagem: ultra-sonografia, histerossonografia ou ressonância magnética. Quando o nódulo mede 2 cm ou menos, recebe o escore 0; se for maior que 2 cm e menor que 5 cm, recebe o escore 1; e medindo 5 cm ou mais, recebe o escore 2 (Figura 4).
Figura 4
Topografia
A topografia é determinada pelo terço da cavidade uterina em que está situado o mioma, sendo escore 0 no terço inferior, escore 1 no terço médio e escore 2 no terço superior (Figura 5). Quando o mioma está na parede lateral, soma-se mais 1 ponto, independente do terço acometido (por ex., terço médio da parede lateral = 1 + 1).
Figura 5

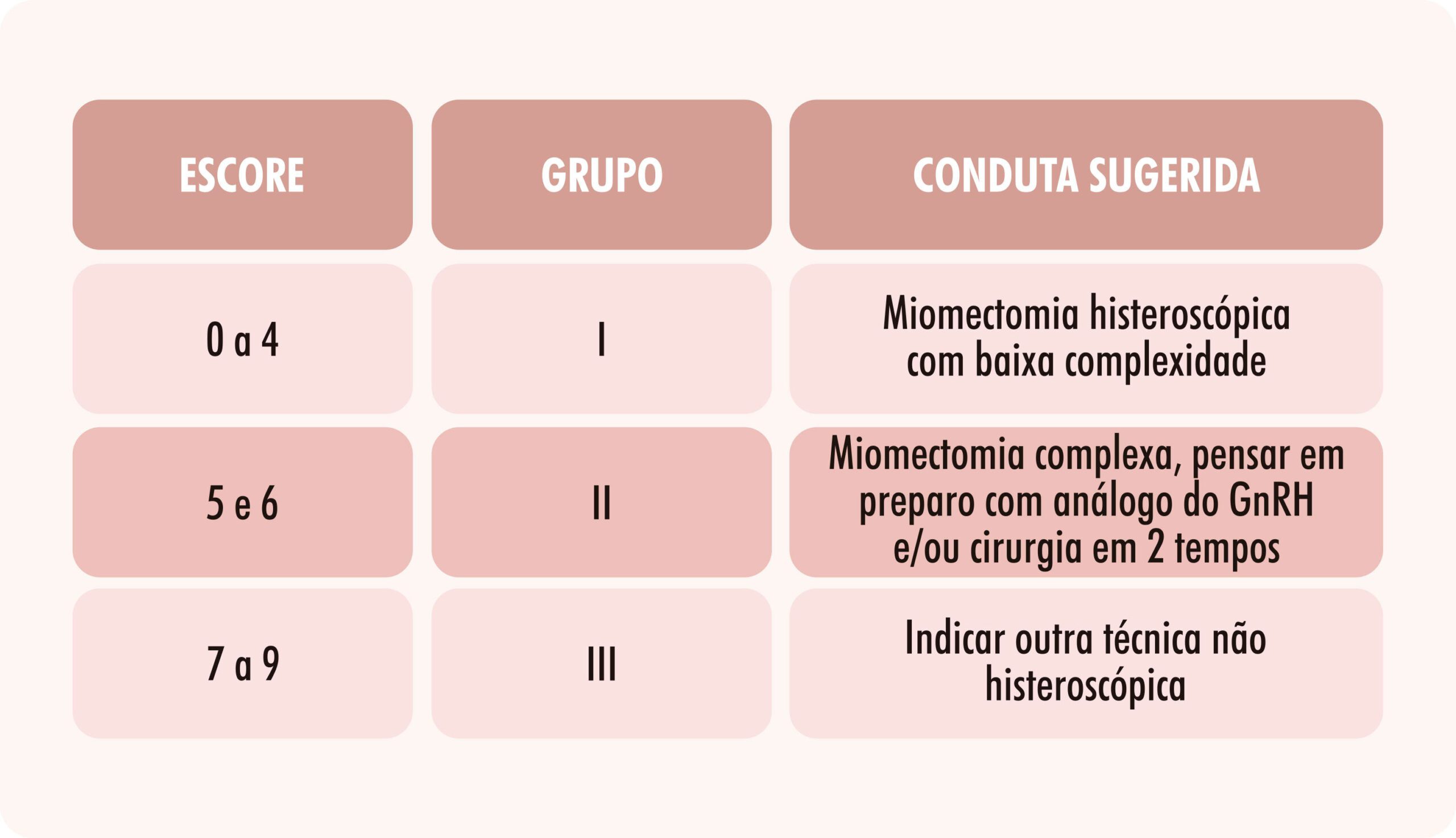
A paciente pode apresentar mais de um mioma submucoso. Cada mioma submucoso tem sua pontuação individual (Tabela 1). Para enquadramento no grupo (I, II ou III) deve ser levado em consideração apenas o mioma que apresente o maior escore (Tabela 2). O escore total máximo é de nove pontos.
Tabela 1: Critérios empregados para a classificação de cada mioma
Tabela 2: Grupo no qual cada paciente se enquadra e conduta sugerida de acordo com o maior escore obtido
Considerações finais
Considerando que o estadiamento dos nódulos determina o nível de dificuldade operatória, Cohen e Valle (2000) consideraram que cirurgiões histeroscopistas com modesta experiência podem operar com certa tranqüilidade os miomas Tipo 0 e Tipo 1, enquanto que os nódulos classificados como Tipo 2, com extensão intramiometrial superior a 50%, deveriam ser operados apenas por cirurgiões com considerável experiência. Portanto, um adequado mapeamento pré-cirúrgico se reveste de considerável importância, prevendo as dificuldades técnicas e possíveis complicações da miomectomia. Com isso, minimiza-se a morbidade do procedimento e evita-se operar miomas que potencialmente não permitiriam uma ressecção completa.
Outros tratamentos para miomas
Embolização da artéria uterina:
Este tratamento limita o crescimento dos miomas pela diminuição do fluxo sanguíneo para os miomas. A embolização da artéria uterina consiste na introdução de um cateter na artéria femoral direita e posterior embolização dos ramos ascendentes da artéria uterina. Este procedimento é indicado nas pacientes com anemia grave que recusam transfusão e quando a cirurgia é contraindicada. Embora seja bastante bem sucedido na redução do tamanho e dor dos miomas, a sua segurança para as mulheres que estão tentando conceber não foi estabelecida. Dor persistente isquêmica, febre pós-embolização, síndrome de pós-embolização grave, piometra, sepse, histerectomia e até mortes foram relatadas após o procedimento. Insuficiência ovariana pode ocorrer em 1% a 2% dos pacientes, embora gestações bem sucedidas também tenham sido relatadas após a embolização. Pelo risco de levar à falência ovariana, é vista com ressalva em pacientes que desejam gestação.
Histerectomia
Histerectomia é a cirurgia de retirada do útero. Pode ser feito por via vaginal, abdominal ou laparoscópica. É o único tratamento definitivo para miomas mas impede uma gravidez futura, já que o útero é removido. É bem indicada em pacientes sintomáticas sem melhora com tratamento clínico, desde que já tenham filhos e não desejem mais engravidar no futuro.
Conclusão
Os estudos que avaliam o efeito dos miomas na fertilidade ainda são conflitantes, tanto nas taxas de implantação, taxas de gravidez e de nascimento. Entretanto, devemos considerar se a paciente esta tentando engravidar naturalmente ou vai realizar FIV. No caso de tentativas naturais deve ser considerado a idade da mulher, o tempo perdido e histórico de abortos. Miomas submucosos e os intramurais maiores de 5 cm que deformam a cavidade endometrial devem ser retirados, mas os riscos de complicações da cirurgia não devem ser desprezados e as pacientes devem ter a ciência que toda intervenção cirúrgica envolve riscos de complicações.
Embora seja questionável se miomas intramurais menores e que não distorcem a cavidade endometrial prejudicam as taxas de gestação, principalmente nos tratamentos de FIV, recomenda-se que, após dois ou três tratamentos de FIV sem sucesso, estes miomas devam ser extraídos. O exame Ressonância Magnética Cine Mode Display também pode ser utilizada para se tomar esta decisão.
Uma opção, nos casos de FIV, é uso de análogo do GnRH ou acetato de ulipristal de 3 a 6 meses antes da transferência embrionária. Com isso, pode haver diminuição dos miomas e aumentar a chance de gravidez, principalmente em mulheres com múltiplos miomas, cuja cirurgia apresenta risco de perda uterina. Em pacientes com miomas e aumento das contrações uterinas, uso de atosiban durante a transferência também pode ser benéfico.