Introdução
O PGT (Teste Genético Pré-Implantacional) pode ser realizado no processo de fertilização in vitro (FIV), com o objetivo de diagnosticar nos embriões a existência de alguma doença genética, antes da implantação no útero da mãe. Assim, casais com chances de gerar filhos com problemas genéticos como Síndrome de Down (trissomia do cromossomo 21), Síndrome de Patau (trissomia do cromossomo 13), Síndrome de Edwards (trissomia do cromossomo 18), Síndrome do Klinefelter (47XXY), distrofia muscular, hemofilia, entre outras anomalias genéticas, podem descobrir se o embrião possui tais doenças por meio deste exame.
Quem se beneficia do PGT na realização da Biópsia Embrionária?
O PGT pode ser utilizado em ciclos de FIV para todos os casais, porém as principais indicações são para casais com mulheres com idade avançada (mais de 40 anos – alguns recomendam após os 37 anos) ou quando um dos parceiros do casal tiver alterações cromossômicas avaliadas pelo exame cariótipo, como as translocações, inversões ou polimorfismos. A importância destas três últimas avaliações vai depender do histórico reprodutivo de cada paciente como, por exemplo, tempo de tentativas de gravidez, abortos e falhas em tratamentos anteriores.
Casais com doenças genéticas na família causadas por genes específicos também têm indicação para realizar o teste.
IDADE MATERNA
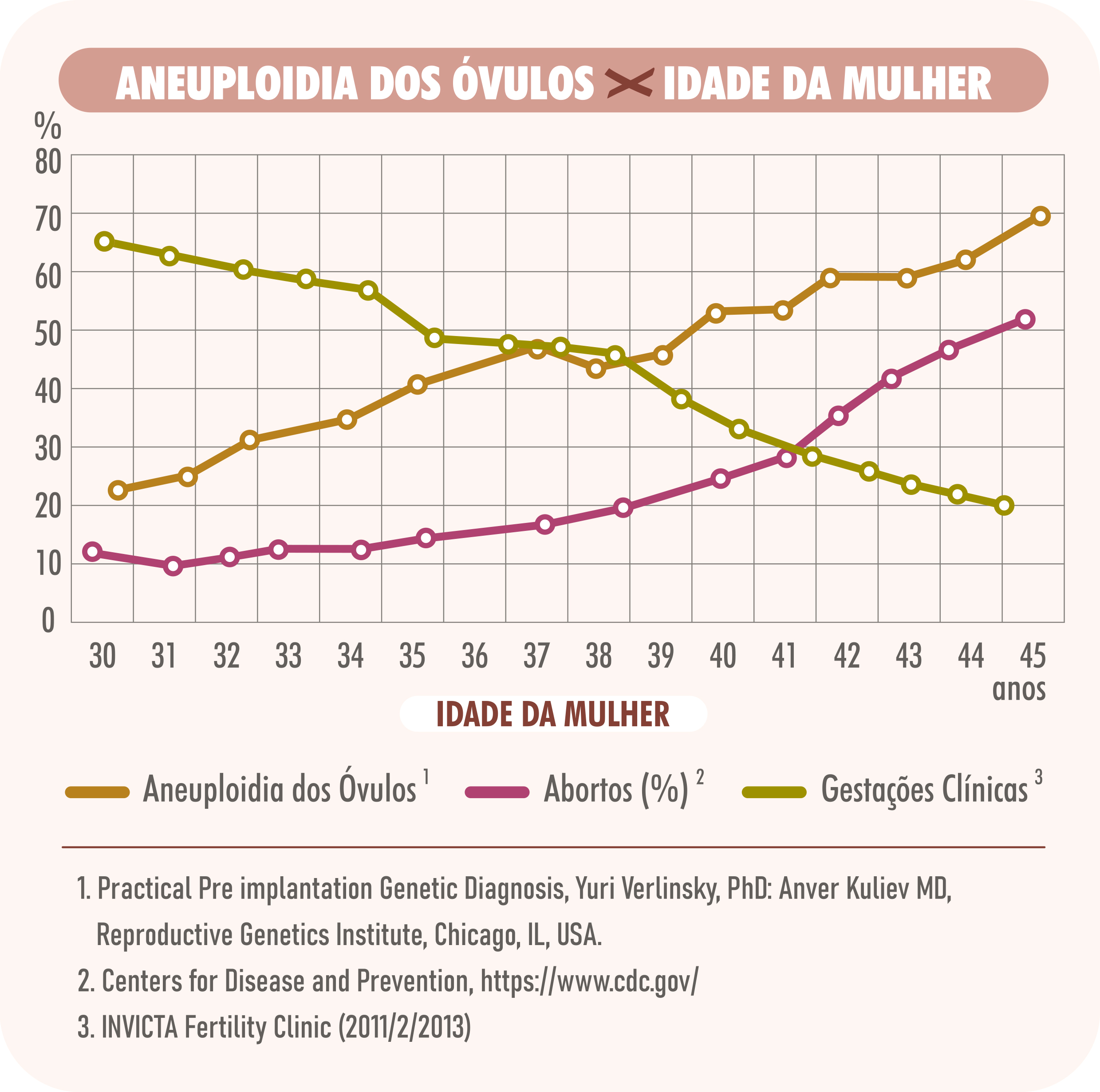
Quanto à idade materna, temos que lembrar que a mulher nasce com todo o seu estoque de óvulos, que não se renova. À medida que a mulher envelhece, os óvulos dela também envelhecem, e isso aumenta as chances de possuírem algum erro cromossômico. Assim, ao serem fertilizados, irão gerar embriões cromossomicamente alterados, que não se desenvolvem, evoluem para aborto ou geram crianças com alterações cromossômicas.
Índice
ToggleESSE É UM CONTEÚDO EXTENSO PARA QUE VOCÊ TENHA TODOS OS DETALHES QUE FAZEM A DIFERENÇA!
ALTERAÇÕES NO CARIÓTIPO
Em relação a alteração no cariótipo, temos que lembrar que este é um exame que analisa a quantidade e composição dos cromossomos de um indivíduo. Em uma pessoa normal, o cariótipo mostrará que ela tem 46 cromossomos (23 pares), sendo 22 chamados autossômicos e 2 sexuais (XX se mulher ou XY se homem). Entretanto, pessoas normais podem ter alterações no cariótipo que não causam repercussão, mas aumenta o risco de filhos de gerarem embriões com alteração cromossômica. Estas alterações são chamadas rearranjos cromossômicos e podem ser dos seguintes tipos:
-
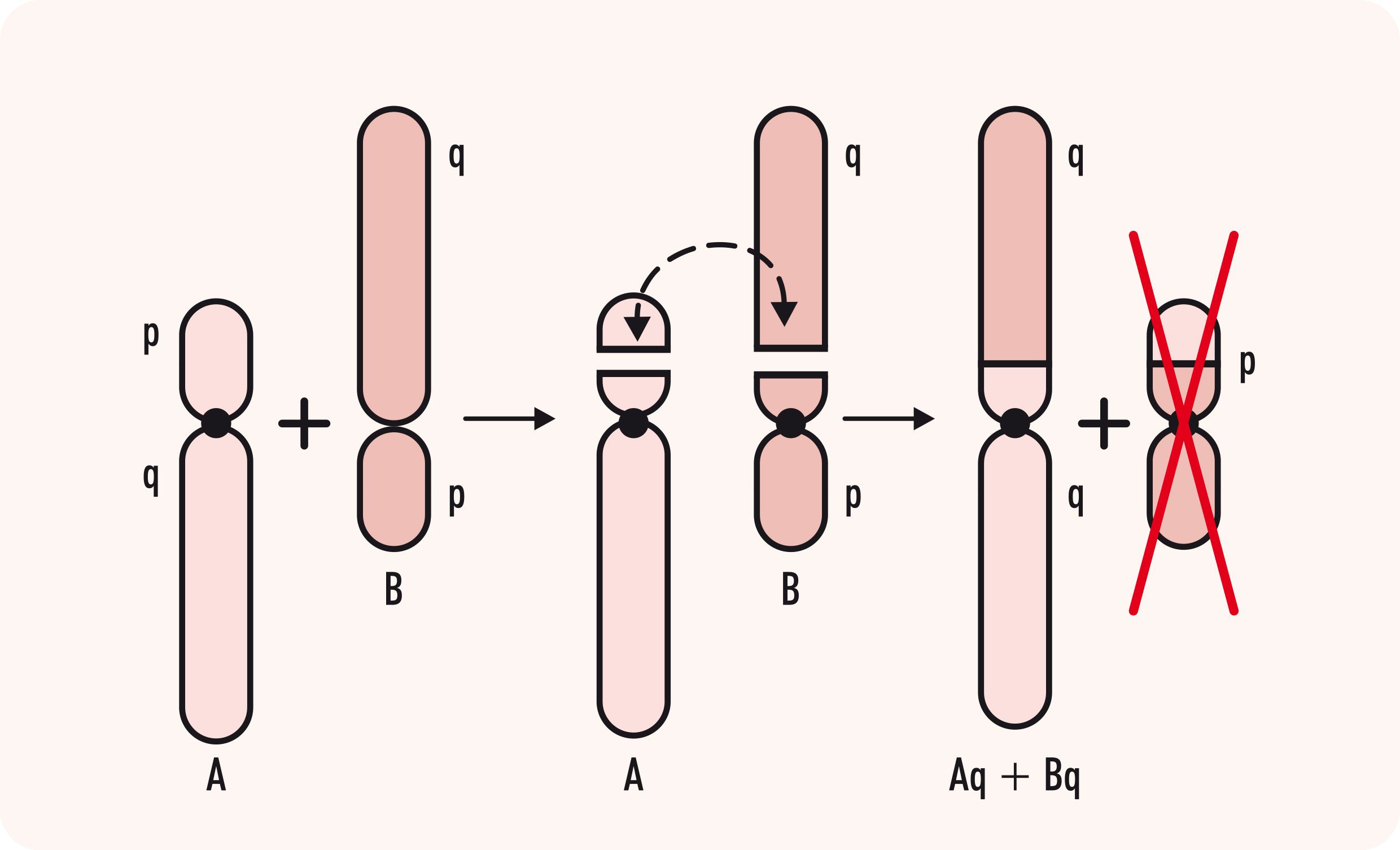
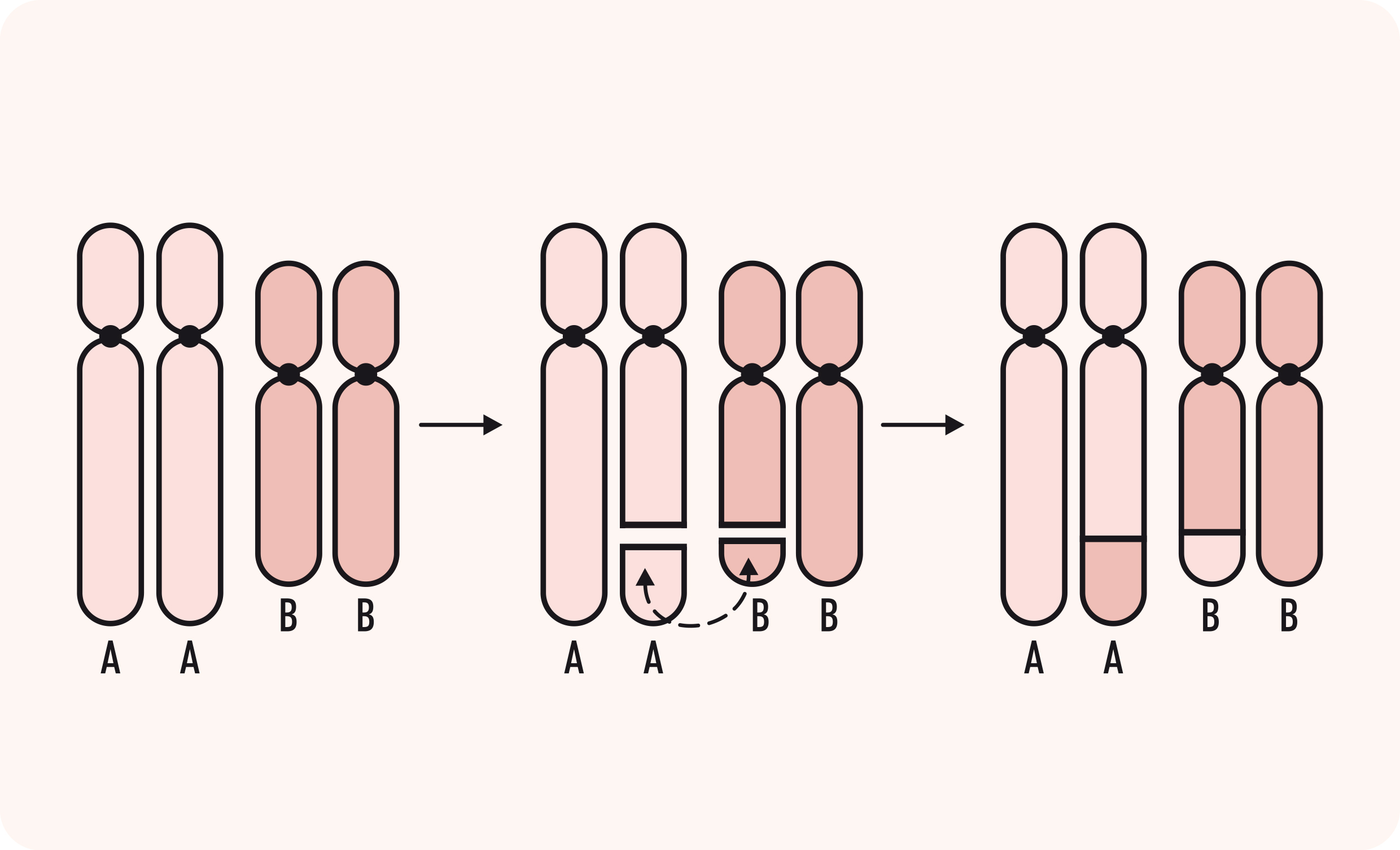
- Translocação cromossômica: uma anomalia cromossômica causada pelo rearranjo de partes entre cromossomos que não são pares, ou seja, parte de um cromossomo está trocada de lugar com um pedaço de outro cromossomo. É o mais comum dos rearranjos cromossômicos e pode ser de dois tipos principais: a Translocação Robertsoniana e a Translocação Recíproca, também conhecida como não-Robertsoniana. Para entendermos a diferença, temos que lembrar que cada cromossomo tem dois braços: um curto (p) e um longo (q), unidos por uma estrutura chamada centrômero. Em alguns cromossomos, o centrômero está na extremidade, tendo, assim, um braço longo e um braço muito curto. Esses cromossomos são chamados acrocêntricos e são os cromossomos 13, 14, 15, 21 e 22. Chama-se translocação Robertsoniana quando dois cromossomos acrocêntricos fundem seus braços longos, perdendo os curtos. Com isso, o indivíduo fica com um cromossomo a menos, mas com um cromossomo com 2 braços longos diferentes unidos pelo centrômero (Figura 2). Já nas translocações não Robertsonianas, somente alguns segmentos de cromossomos são trocados, podendo envolver qualquer cromossomo (Figura 3). Além disso, as translocações recíprocas podem ser balanceadas (sem perda ou acréscimo de material genético) ou não-balanceadas (quando a troca de material cromossômico é desigual resultando em genes extras ou ausentes).
Translocação Robertsoniana entre cromossomo A e B (acrocêntricos): ambos perderam o braço curto e os dois braços longos se fundem formando um cromossomo com dois braços longos enquanto que os braços curtos são perdidos.
Translocação Recíproca (Não-Robertsoniana) entre cromossomos A e B, onde um segmento do braço longo do cromossomo A trocou de lugar com um segmento do braço longo do cromossomo B, sem perda de material (translocação balanceada).
-
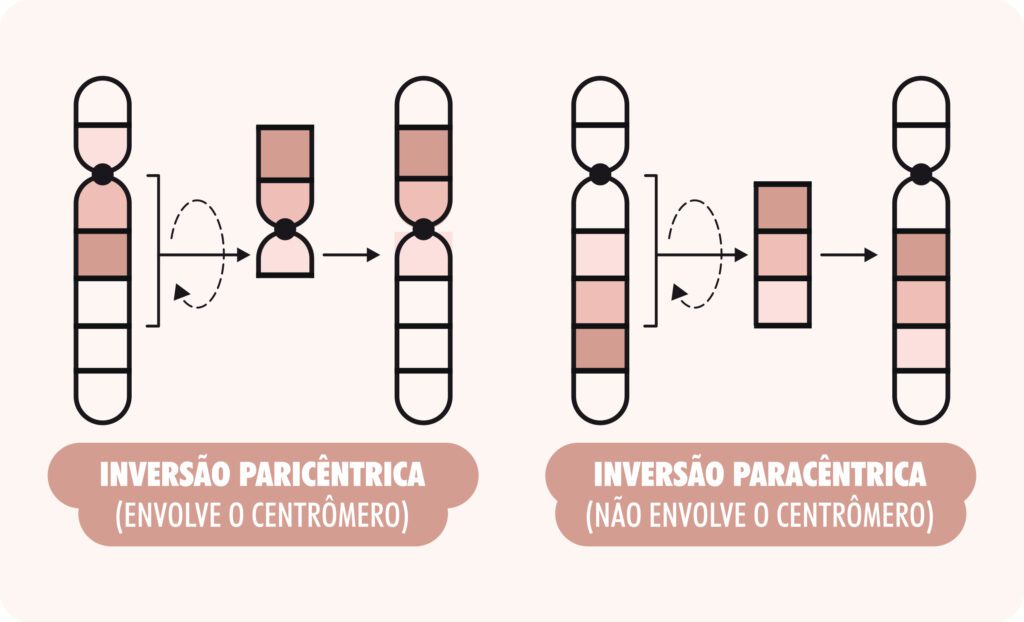
- Inversão cromossômica: que ocorre quando um segmento de um cromossomo se separa, gira 180o e se reintegra ao mesmo cromossomo, mas com a orientação invertida. A inversão é dita paracêntrica se as quebras ocorrerem em um mesmo braço cromossômico, e é denominada pericêntrica se o fragmento cromossômico invertido incluir o centrômero (Figura 4). Essa alteração pode ser equilibrada (quando não se perde material genético) ou pode ser desequilibrada (quando há perda ou ganho de material genético).
-
- Duplicações: um segmento do cromossomo é duplicado.
- Deleções: quando há perda de um segmento cromossômico.
- Polimorfismos cromossômicos: são alterações da estrutura cromossômica que não costumam ter impacto clínico, pois ocorrem em regiões com genes naturalmente inativos, sendo consideradas variação da normalidade. As mais importantes são as alterações da heterocromatina, uma parte do cromossomo formada por DNA compactado, com baixa ou nenhuma atividade genética. Existem alguns estudos que mostram associação destes polimorfismos com infertilidade e aborto de repetição, embora seja questionável sua repercussão na chance de a pessoa gerar embriões aneuploides, não havendo uma comprovação definitiva.
- Abortos de repetição e falhas repetidas em tratamentos de FIV: a principal causa de aborto e uma das principais causas de falhas de implantação em transferências embrionárias são devido a aneuploidias nos embriões. Selecionar embriões euploides pode ser útil para evitar um novo aborto ou falha.
- História familiar ou antecedente pessoal de doença genética (cromossômica ou de gene específico): quando se sabe que o/a paciente tem uma doença genética na família, é interessante avaliar os pais para saber se há risco aumentado dos filhos terem a mesma doença. Além disso, casais que já tiveram um filho com alguma alteração cromossômica costumam optar pelo exame para evitar passar por esse processo de novo.
PGT-A, PGT-M E PGT-SR: Siglas para Cada Tipo de Diagnóstico Genético Pré-Impantacional
Após a realização da biópsia embrionária, as células extraídas são encaminhadas para o teste genético pré-implantacional (PGT), que pode ser de quatro tipos, de acordo com a anomalia genética investigada.
Todos esses testes podem ser realizados por meio da tecnologia de sequenciamento de nova geração (NGS – Next Generation Sequencing), que se tornou a principal ferramenta utilizada atualmente devido à sua alta sensibilidade, precisão e capacidade de detecção de múltiplas alterações genéticas, incluindo ganhos e perdas cromossômicas, mutações específicas e desequilíbrios estruturais. A escolha do tipo de PGT a ser realizado depende do histórico genético do casal, das características dos embriões e dos objetivos do tratamento, sendo eles:
PGT-A
Lembre-se A de ANEUPLOIDIA, que significa alterações cromossômicas, ou seja, o diagnóstico que identifica a saúde cromossômica do embrião. Embriões aneuploides têm cromossomos a mais ou a menos e, dependendo do cromossomo envolvido, pode levar a falha de implantação, abortos e gestações que evoluem com alterações, como Síndrome de Down entre outras síndromes. Assim, este estudo é realizado para ajudar a oferecer um tratamento de FIV mais efetivo, pois permite identificar o embrião saudável com possibilidade ampliada de implantação e risco reduzido de abortamento e doenças cromossômicas, que estão principalmente relacionadas com a idade materna avançada e alterações no cariótipo do casal. Também é indicado em casos de abortos de repetição sem outra causa.
PGT-M
Lembre-se M de MONOGÊNICA (gene único), no qual o diagnóstico do embrião tem o objetivo de identificar aqueles que foram afetados por uma alteração genética específica herdada dos pais e que dá origem a uma doença hereditária. É um estudo indicado para famílias onde existem casos de doenças causadas por um gene específico, tais como anemia falciforme e fibrose cística, entre outras. O objetivo do PGT-M é estabelecer uma gravidez que não será afetada por doenças genéticas causadas por uma mutação genética conhecida, presente em um ou ambos os pais. Também é usado para selecionar embriões para transferência que possuam características imunológicas específicas compatíveis com um irmão afetado pela doença, cujo tratamento efetivo seja o transplante de células-tronco.
PGT-SR
(teste Genético Pré-Implantacional para Reorganizações Estruturais ou, em inglês, Strutural Rearrangements, por isso SR):
É um teste semelhante ao PGT-A, mas específico para casais com rearranjos cromossômicos estruturais como, por exemplo, as translocações. Os três principais tipos de rearranjos são: translocações recíprocas, translocações robertsonianas e inversões, já explicadas anteriormente. A translocação mais comum em humanos envolve os cromossomos 13 e 14 e é observada em cerca de 0,97/1000 recém-nascidos, mas existem outras consideradas importantes e que devem ser avaliadas caso a caso. O objetivo do PGT-SR é estabelecer uma gravidez que não seja afetada por essas anormalidades em um casal com uma translocação equilibrada ou deleção/duplicação. Rearranjos cromossômicos podem ser herdados ou podem ocorrer espontaneamente. Muitos portadores de rearranjos cromossômicos balanceados são saudáveis e desconhecem o status de portador até que tentem ter filhos. Os portadores de rearranjos equilibrados correm o risco de produzir embriões com a quantidade incorreta de material cromossômico, o que normalmente não leva a uma gravidez bem-sucedida. O PGT-SR pode ajudar a identificar embriões com a quantidade correta de material cromossômico com maior probabilidade de levar a uma gravidez bem-sucedida e a um nascimento saudável. A abreviação t(A;B)(p1;q2) é usada para denotar a translocação entre um cromossomo A e um cromossomo B. A informação no segundo conjunto de parênteses, quando fornecida, indica a localização precisa no cromossomo para os cromossomos A e B respectivamente – com p indicando o braço curto do cromossomo, q indicando o braço longo e os números após p e q se referindo às regiões, bandas e sub bandas quando os cromossomos são corados e observados em um microscópio.
PGT-P
Lembre-se P de Poligênica, ou seja, múltiplos genes. O exame PGT-P é um teste para avaliar o risco do embrião ter doenças poligênicas complexas, ou seja, determinadas por múltiplos genes. O exame PGT-P é uma ferramenta de triagem usada para ajudar a selecionar qual(is) embrião(ões) tem/têm menor risco de desenvolver determinadas doenças no futuro. Este teste é projetado para rastrear várias condições ao mesmo tempo. O objetivo do PGT-P é encontrar embriões com menor risco para o desenvolvimento de doenças poligênicas, determinando um risco e não um diagnóstico, tornando o exame alvo de muitas críticas. Lembramos que as doenças em questão têm causas multifatoriais, não sendo determinadas somente pela condição genética, mas também influenciadas por fatores ambientais, e ainda não totalmente conhecidas. Assim, este tipo de seleção embrionária levanta diversas questões éticas.
As principais doenças poligênicas pesquisadas são:
- Câncer de Próstata
- Melanoma Maligno
- Carcinoma Basocelular
- Esquizofrenia
- Doença Arterial Coronariana
- Hipercolesterolemia
- Hipertensão
- Risco de Ataque Cardíaco
PGT-A PLUS
O teste genético PGT-A tradicional é utilizado para verificar se o embrião tem algum(uns) cromossomo(s) (ou parte deles) a mais ou a menos, entretanto, não consegue perceber o erro se o conjunto inteiro de cromossomos estiver a mais ou a menos (erro de ploidia). As células humanas são diploides, ou seja, tem dois cromossomos de cada, com exceção dos óvulos e espermatozoides que são haploides, ou seja, tem somente um cromossomo de cada. Com a união dos dois gametas, a célula embrionária formada volta a ser diploide, entretanto, se houver algum erro na formação dos gametas ou na fertilização, o embrião pode ter erro na ploidia, sendo haploide (23 cromossomos), triploide (3 cromossomos de cada, ou seja, 69 cromossomos), ou até tetraploide (92 cromossomos). Alterações incompatíveis com o desenvolvimento embrionário saudável. Esses erros não conseguiam ser detectados pelo PGT-A tradicional, porém hoje, há um exame mais completo chamado PGT-A plus, ou PGT-A com teste de ploidia, capaz de detectar estas alterações, tornando o exame mais preciso.
Este teste é especialmente importante quando, logo após a fertilização, observamos alterações no número de pronúcleos (estruturas que contém o material genético do óvulo e do espermatozoide). O normal é a presença de dois pronúcleos (um do óvulo e um do espermatozoide). Porém, às vezes, encontramos apenas um pronúcleo (1PN) ou três (3PN). Essas alterações sugerem ter havido um erro na divisão do gameta ou na fertilização, aumentando o risco desse embrião ser haploide ou triploide, ou seja, ser inviável. Estes embriões costumavam ser descartados devido a esse risco, mas com esse teste é possível avaliar se eles são diploides, o que pode ocorrer, e, se normais, podem ser transferidos.
As principais indicações da Biópsia Embrionária
O PGT-A é o teste genético mais utilizado e está indicado nas seguintes situações:
- Idade materna avançada.
- Cariótipo alterado de pelo menos de um dos membros do casal, que apresentam risco elevado de alteração cromossômica na prole, como translocação, inversão ou polimorfismo (OBS: dependendo das translocações e inversões, o mais recomendado seria o PGT-SR).
- História familiar de doenças cromossômicas.
- Antecedente de filho com alteração cromossômica.
- Aborto de repetição.
- Falhas de tratamentos prévios de FIV.
- Apesar do PGT-A ser indicado nos casos acima, alguns casais que fazem a FIV optam por fazer o teste, independente da indicação. Isso é possível, mas não recomendado pelas controvérsias do exame descritas a frente nesse e-book.
Interpretação dos resultados da Biópsia Embrionária
O PGT-A é o teste genético mais utilizado e está indicado nas seguintes situações:
- Idade materna avançada.
- Cariótipo alterado de pelo menos de um dos membros do casal, que apresentam risco elevado de alteração cromossômica na prole, como translocação, inversão ou polimorfismo (OBS: dependendo das translocações e inversões, o mais recomendado seria o PGT-SR).
- História familiar de doenças cromossômicas.
- Antecedente de filho com alteração cromossômica.
- Aborto de repetição.
- Falhas de tratamentos prévios de FIV.
- Apesar do PGT-A ser indicado nos casos acima, alguns casais que fazem a FIV optam por fazer o teste, independente da indicação. Isso é possível, mas não recomendado pelas controvérsias do exame descritas a frente nesse e-book.
NICS - Análise Não Invasiva do Embrião
Entre os avanços tecnológicos que estarão em pauta, destacamos a possibilidade do teste genético pré-implantacional não invasivo (nicsPGT). É um método não invasivo de Screening Cromossômico (NICS) baseado no sequenciamento do DNA genômico secretado no meio de cultura a partir dos blastocistos. Esta nova avaliação genética do embrião ainda está em estudos e não está validada. O DNA livre de células identificado no meio de cultura pode ter contaminação de DNA materno, o que aumenta a complexidade do diagnóstico. A vantagem quando se compara ao PGT clássico e já conhecido, é não ser necessária a retirada de células do embrião e, por isso, é uma técnica não invasiva. Entretanto, ainda é considerada experimental e, no momento, não substitui a biópsia embrionária (PGT-A).
O uso de inteligência artificial para análise de embrião também vem avançando muito e talvez, no futuro, possa predizer a chance de embriões euploides de forma não invasiva, mas isso ainda não é possível. Vamos aguardar o futuro.
Como o PGT-A melhora as taxas de sucesso nos tratamentos de FIV?
O PGT-A, nas indicações listadas anteriormente, demonstrou inúmeros benefícios, entre eles:
- Reduz o tempo para se alcançar uma gestação, diminuindo número de transferências embrionárias necessárias, uma vez que exclui embriões que não implantariam por alteração cromossômica.
- Reduz o risco de abortos, já que a maior parte das perdas se deve às alterações do número de cromossomos.
- Pode aumentar a chance de implantação do embrião por transferência e o sucesso de dos tratamentos.
- Reduz o risco de gestações múltiplas pela transferência eletiva de um único embrião (single embryo transfer – SET)
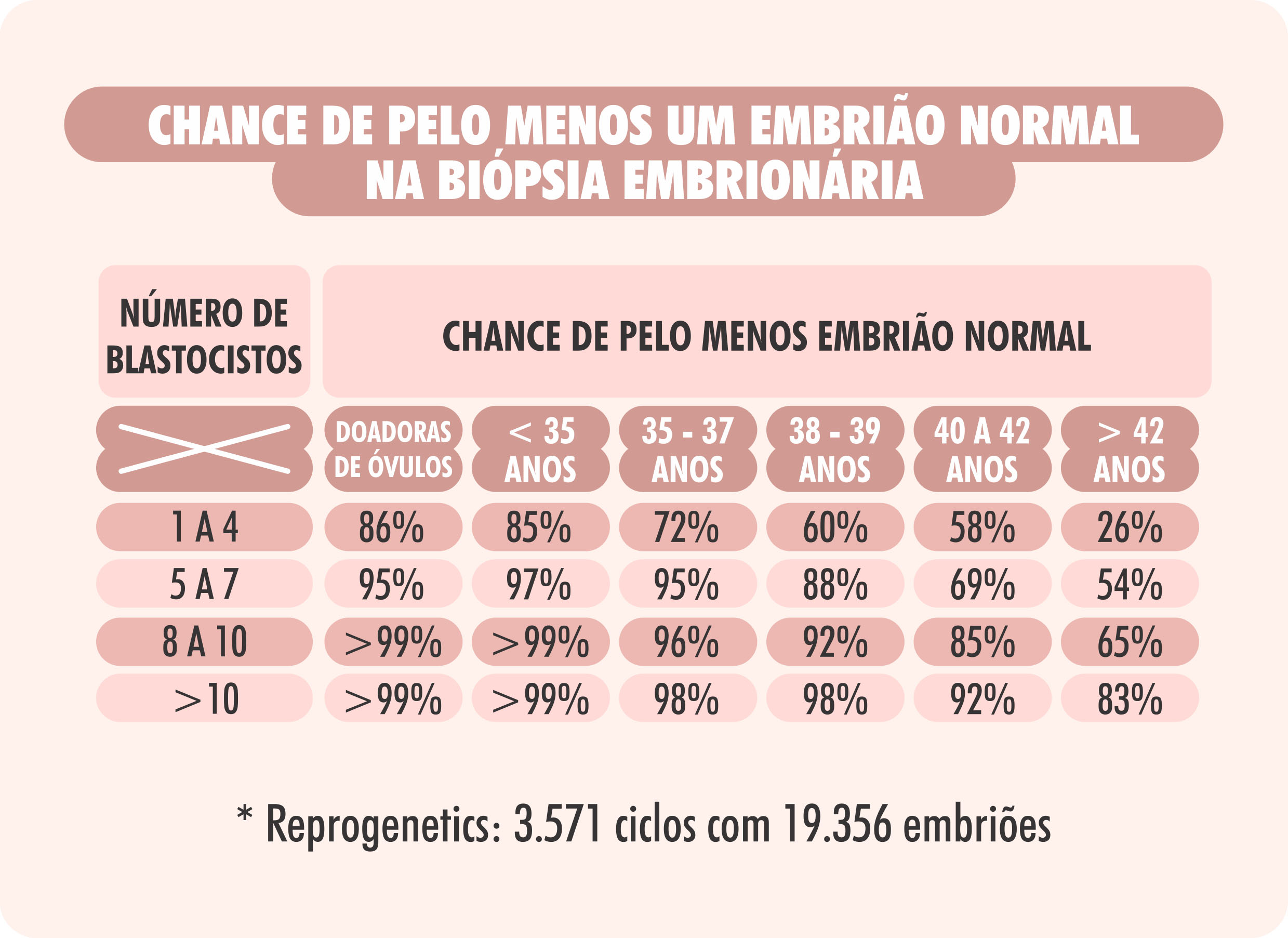
Veja as estatísticas apresentadas abaixo:
Qual a diferença entre Eficiência e Eficácia quando falamos em Biópsia Embrionária?
A diferença entre eficácia e eficiência é que enquanto a eficácia refere-se a fazer a tarefa certa, completar atividades e alcançar metas, a eficiência é sobre fazer as coisas de forma otimizada, de maneira mais rápida ou com menos gastos.
Em termos gerais:
- Eficaz: é algo adequado para atingir um propósito, de modo a alcançar o resultado pretendido ou esperado.
- Eficiente: quando a tarefa é executada da melhor maneira possível, com o menor desperdício de tempo, esforço e recursos.
Para alguns autores, o PGT-A torna o tratamento mais eficiente, pois selecionamos o embrião com mais chances e poupamos a paciente de transferir embriões que não implantariam por serem alterados. Entretanto, em algumas situações, pode tornar o tratamento menos eficaz, ou seja, com um pior resultado final, se levar a descarte de algum embrião normal.
Um dos motivos disso é o fato da biópsia ser realizada na porção do embrião que originará a placenta, onde pode ocorrer mosaicismo, ou seja, haver células alteradas entre as normais, e esta alteração nem sempre se reflete no embrião. Mosaicismo é a presença de duas ou mais linhagens de células com diferentes constituições cromossômicas.
Além disso, alguns estudos levantam ressalvas sobre uso do PGT-A. Orvieto et al, no congresso ESHRE de 2014, demostraram que 20% dos casos de PGT-A foram inconclusivos na biópsia e que mais 16% apresentavam mosaicismo. Esfandiari et al demonstraram algumas discrepâncias no resultado de PGT-A do mesmo embrião, enviado para diferentes centros. O mesmo embrião teve resultado normal ou alterado quando o exame era realizado em clínicas diferentes. Há, ainda, alguns relatos publicados de mais de 100 transferências de embriões considerados aneuploides pelo PGT-A que levaram a uma gravidez saudável. Com o avanço das técnicas de avaliação das biópsias embrionárias com novos protocolos de NGS, os resultados estão mais precisos atualmente, mas ainda há chance de erros. Estimase que mosaicismo pode estar presente em 4 a 5% dos embriões biopsiados.
Frente a tudo isso, alguns autores vêm ponderando a realização indiscriminada do exame, principalmente em pacientes com baixa resposta na estimulação ovariana, pois produzem menos óvulos e menos embriões, às vezes, um único embrião.
Outra preocupação é se realmente a biópsia embrionária é inócua para o embrião. Apesar de ser considerada segura, alguns autores questionam se pode afetar as chances do embrião. Um estudo randomizado (Munné et al, 2019) comparou transferências únicas de embriões congelados: um grupo tendo realizada PGT-A e outro sem o exame. Para pacientes abaixo de 35 anos, a taxa de gravidez em curso foi semelhante (49,5% para PGT-A e 53% para grupo controle). Considerando que, neste grupo de pacientes, somente 48% dos embriões eram normais na biópsia, esperava-se uma maior taxa de gravidez no grupo que realizou a biópsia, o que não foi observado, questionando-se se a vantagem de selecionar embriões euploides não foi balanceada por prejuízo causado pela biópsia. Concluiu-se, assim, que nesse grupo de pacientes, o PGT-A não mostrou benefício. Nesse mesmo estudo, também foram avaliadas pacientes entre 35 e 40 anos. Nesse grupo, houve uma taxa de embriões euploides de 35,5% e houve um aumento na taxa de gravidez em curso com a biópsia (51%), em relação aos controles (37%), mostrando benefício da biópsia em pacientes com mais risco de aneuploidia. Nesse estudo, não houve alteração na taxa de abortos com a biópsia.
Por tudo isso, PGT-A não deve se tornar um procedimento de rotina para todas as mulheres que desejam engravidar. Antes de mais nada, existem alguns princípios éticos do casal que devem ser respeitados, como a aceitação de uma seleção natural e a não concordância do descarte dos embriões que apresentarem problemas. Além disso, há o custo envolvido e o fato de não ser isento de riscos, como por exemplo resultados falso positivos, o que poderia levar a descarte de embriões com chance de uma gravidez saudável.
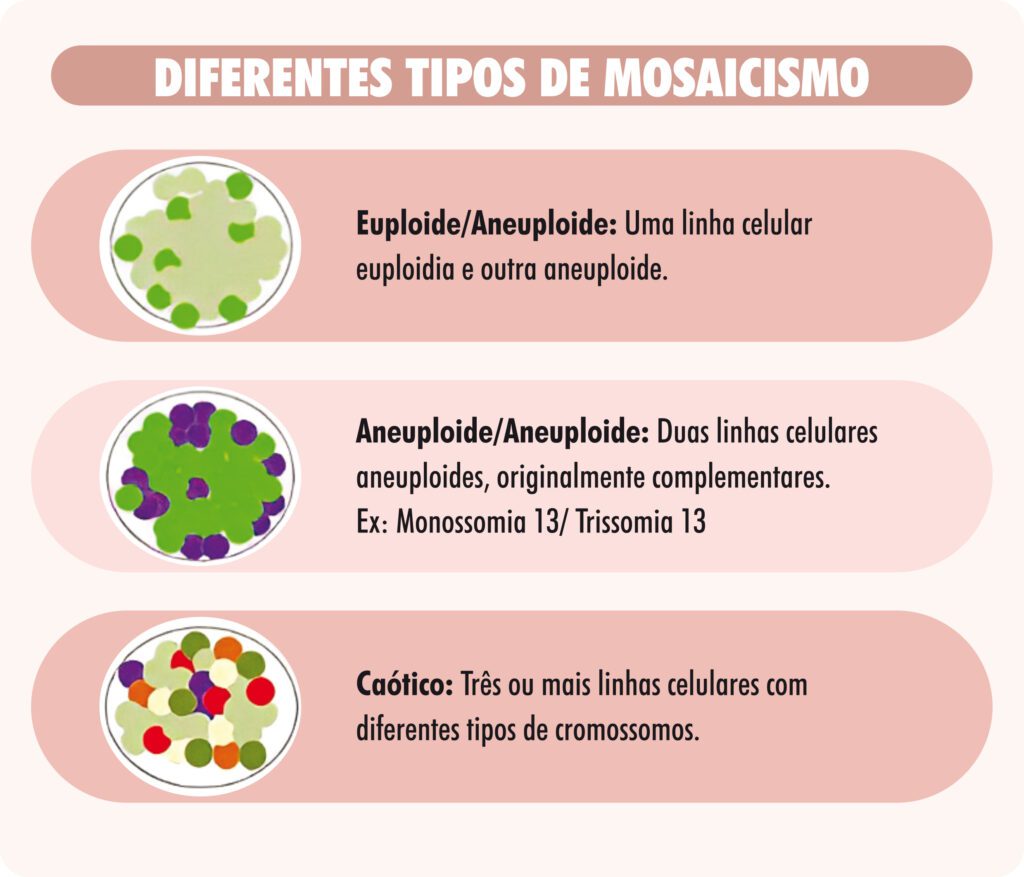
Tipos de mosaicismo encontrados na Biópsia Embrionária
Um embrião é considerado “mosaico aneuploide” quando há mais que um tipo celular, podendo ser parte normal e parte alterado (mosaico euploide/aneuploide) ou todo alterado, mas com mais de uma linhagem de células diferentes (mosaico aneuploide/aneuploide). No último caso, as alterações costumam ser complementares, ou seja, um grupo de células tem um cromossomo a mais, e o outro grupo, um cromossomo do mesmo tipo a menos (Figura 8). Quando há mais de 2 tipos de linhagens celulares aneuploides, chamamos de mosaicismo caótipo. Nessas duas situações, o embrião é classificado como aneuploide, não tendo tanta relevância clínica seu resultado. Entretanto, em situações onde há células euploides e aneuploides, o nível do mosaicismo é importante pois, quanto menor a porcentagem de células aneuploides, maior a chance do mosaicismo estar somente no trofectoderma, onde é feita a biópsia, sendo, muitas vezes, o embrião, propriamente dito, normal. Por outro lado, se há um grau maior de mosaicismo, a chance de ser um mosaico verdadeiro é maior. Assim, o teste do PGT-A classifica mosaicos euploides/aneuploides em dois tipos:
- Mosaico aneuploide de baixo grau: quando há mais de 30% e menos de 50% de células aneuploides na biópsia.
- Mosaico aneuploide de alto grau: quando há mais de 50% e menos de 70% de células aneuploides na biópsia. No caso de menos de 30% de aneuploidias, o embrião é classificado como euploide, enquanto que quando há mais de 70% de aneuploidia, ele é classificado como aneuploide.
Mosaicismo: A grande questão na Biópsia Embrionária
Mosaicismo, como dito, é a presença de dois ou mais tipos de linhagens celulares com diferentes cromossomos no mesmo embrião. Pode ser dividido em baixo grau (mais de 30% e menos de 50% de células aneuploides na biópsia) ou alto grau (mais de 50% e menos de 70% de células aneuploides na biópsia). O mosaicismo sempre existiu e vai continuar existindo, mas o avanço das tecnologias, novos protocolos de NGS e a bioinformática, estão possibilitando uma melhor compreensão desse tema. Veja no próximo capítulo alguns exemplos de como o mosaicismo pode se manifestar.
E AGORA? TRANSFERIR OU NÃO UM EMBRIÃO MOSAICO?
Dependendo do cromossomo envolvido nos casos de mosaicismo, a transferência pode ou não ser indicada. Diante desses casos, é importante seguir as recomendações da Sociedade Internacional de Diagnóstico Genético (PGDIS). Para simplificar o entendimento sobre os riscos envolvidos e recomendações sobre a transferência compartilhamos abaixo:
- Não existe uma resposta simples para a questão da transferência do embrião mosaico ao útero materno, porém existem alguns recursos que podem ajudar na decisão conjunta entre médicos e pacientes.
- Há novas discussões sobre as taxas e porcentagens de mosaicismo. As publicações mais recentes têm demonstrado que, com a evolução do diagnóstico, as taxas encontradas nos embriões estão em torno dos mesmos 5% encontrados em material de aborto estudado, revelando o real diagnóstico com a nova tecnologia.
- Recentemente, após inúmeras validações e quase dois anos de estudos, novos protocolos de diagnóstico para aneuploidias embrionárias foram aprovados para a utilização clínica. Com isso, os resultados do teste genético pré-implantacional para aneuploidias (PGT-A) consegue detectar e quantificar o grau de mosaicismo.
EMBRIÕES COM MOSAICISMO PODEM SER CONSIDERADOS NORMAIS?
Apesar que certos níveis de mosaicismo talvez não apresentem riscos para o desenvolvimento seguro do embrião, quando se trata de saúde, é preciso ter cuidado e envolver os pacientes em uma decisão dessa dimensão e importância. Não existe resposta padrão para o dilema de transferir um embrião com mosaicismo e arriscar a saúde de um futuro bebê, mas, sim, protocolos e referências baseados em evidências científicas para orientar a família e os especialistas nessa escolha. Especialistas de todo o mundo estão debatendo esta questão e, recentemente, a PGDIS, Sociedade Internacional que reúne especialistas e estudos sobre o diagnóstico genético pré-implantação, publicou posição sobre o mosaicismo cromossômico identificado em embriões em estágio de blastocisto.
O objetivo de obter o sucesso dos tratamentos de reprodução humana é comum para os pacientes, clínicas de reprodução assistida e laboratórios de genética. Quando a análise de embriões de casais que normalmente não estão em seu primeiro ciclo de FIV obtém como resultados somente embriões alterados por mosaicismo, o que muitos se perguntam é se interromper o tratamento é a única solução ou se, pelo contrário, a autocorreção celular de mosaicismo é uma realidade e os casais deveriam ter a chance de optar pela transferência embrionária.
RECOMENDAÇÕES E POSICIONAMENTO DA PGDIS (PREIMPLANTATION GENETICS DIAGNOSIS INTERNATIONAL SOCIETY) SOBRE O MOSAICISMO DE EMBRIÕES EM ESTÁGIO DE BLASTOCISTO
- Transferir embriões onde são identificadas aneuploidias de mosaicismo, ou seja, algumas células possuem aneuploidias e outras não, deve ser cogitado apenas quando não existem embriões euploides, ou seja, cromossomicamente normais.
- Para detectar com segurança o nível de mosaicismo é preciso que a biópsia embrionária extraia, de preferência 5 células, e que seja feita com o mínimo dano possível.
- É preciso que o laboratório de genética conte com uma plataforma de NGS validada que possa avaliar o nível de mosaicismo das células.
- Níveis de mosaicismos inferiores a 20% podem ser considerados normais e níveis maiores de 80% devem levar a um diagnóstico de embrião aneuploide, que não deveria ser transferido.
- Níveis de mosaicismos entre 20%-80% devem ser analisados individualmente, envolvendo especialistas da clínica de reprodução assistida, laboratório de genética e também os pacientes.
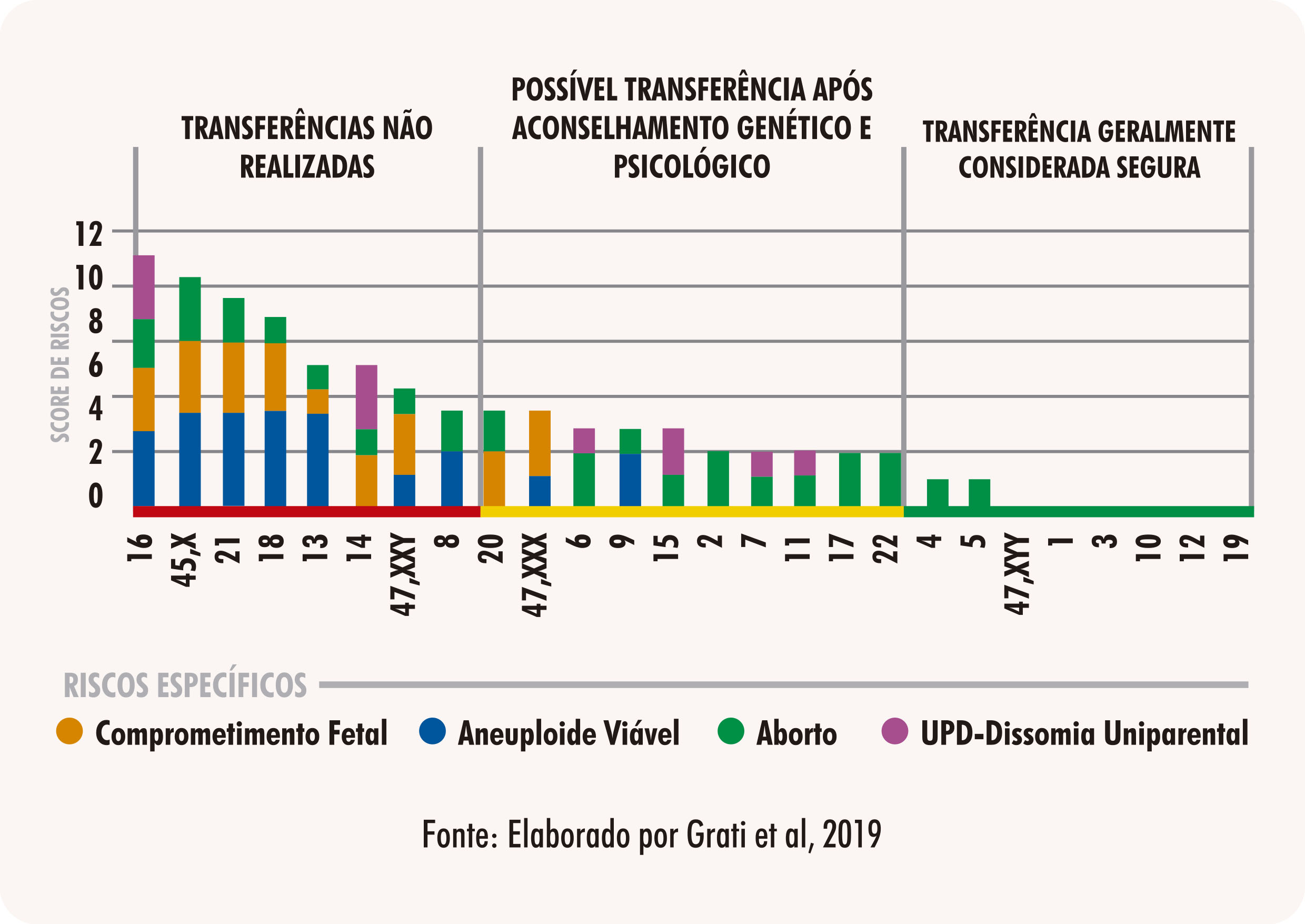
- Entre os embriões mosaicos para euploide/monossomia ou mosaico para euploide/trissomia, priorizar embriões euploide/trissomia, pois a maioria das monossomias, com exceção de 45,X não evoluem. Além disso, é importante considerar, entre opções de embriões com trissomia, qual é o cromossomo alterado para tomar a decisão (eliminar trissomias com 13,18,21).
Pacientes devem sempre estar envolvidos e conscientes dos riscos da transferência de embriões com mosaicismo e contarem com um aconselhamento genético para tomar uma decisão. É importante sempre considerar o cromossomo envolvido, priorizando aqueles em que, caso a alteração se confirme, não resulte no nascimento de uma criança com anomalias (vide Figura 09). Além disso, o acompanhamento de um pré-natal rigoroso, podendo incluir, dependendo do caso, testes como NIPT (Non-Invasive Prenatal Test ou, em português, Teste Prénatal Não Invasivo), realizado através de coleta do sangue materno a partir da 10ª semana de gestação; ou até amniocentese, um teste invasivo onde se extrai uma amostra de líquido amniótico para análise genética do embrião e que pode ser realizado a partir da 16ª semana de gestação. Para acessar a publicação completa com todas as recomendações para clínicas e laboratórios de genética acesse o Newsletter PGDIS.
RESULTADOS COM TRANSFERÊNCIA DE EMBRIÕES MOSAICOS
Apesar de preocupação com a transferência de embriões mosaicos, os resultados são animadores. Um estudo de Viotti et al comparou transferências de 5.561 embriões euploides com 1.000 transferências de embriões mosaicos. Neste estudo, com a transferência de embriões euploides, foi encontrada uma taxa de implantação de 57,2% e de nascidos vivos de 52,3%, enquanto a transferência de embriões mosaicos teve taxas menores (41,8% e 31,3%, respectivamente).
Em relação à taxa de aborto, embriões mosaicos tiveram maiores taxas (25% vs 8%). Entretanto, apesar da menor taxa de implantação, maior taxa de aborto e menor taxa de nascidos vivos, mais de 30% de nascidos vivos é uma taxa expressiva, incentivando a transferência de embriões mosaicos, na ausência de embriões euploides. Foi observado que o grau de mosaicismo (porcentagem de células anormais) e se aneuploidia envolve somente parte de um cromossomo ou um cromossomo inteiro também.
Em relação a chance do embrião se desenvolver e levar ao nascimento de uma criança com alteração, uma revisão da literatura avaliou 2.759 transferências de embriões mosaicos, demonstrando uma taxa de gravidez de 38%, sendo que somente em uma delas o cariótipo confirmou o mosaico diagnosticado no PGT-A, o que representa menos que 1% dos casos.
Uma possível explicação para os estes resultados é a origem do erro genético. Diferente das aneuploidias completas, que geralmente ocorrem durante a formação dos óvulos ou espermatozoides (fase da meiose), o mosaico costuma surgir após a fertilização, durante as primeiras divisões celulares do embrião – um processo chamado mitose. No primeiro caso, o embrião já se inicia a partir de uma célula alterada, logo, todo embrião é alterado. Já no mosaico, como o erro acontece depois, quando as células do embrião estão se dividindo, formam-se células normais e outras com alterações. Além disso, estudos mostram que esses erros na mitose tendem a acontecer com mais frequência nas células do trofectoderma (a parte que formará a placenta biopsiada no PGT-A) do que na massa celular interna (que formará o embrião). Como biopsiamos o trofectoderma, isso explica porque muitos embriões com PGT-A com resultado de mosaico têm massa celular interna normal e, portanto, podem implantar e se desenvolver normalmente.
Assim, diante das evidências atuais, observa-se uma tendência crescente à transferência de embriões mosaicos quando não há embriões euploides disponíveis. Embora as taxas de sucesso sejam inferiores às dos euploides e exista um risco aumentado de aborto, os resultados ainda são consideráveis, com taxas de nascidos vivos superiores a 30% e um risco muito baixo de nascimento com anomalias cromossômicas confirmadas. Assim, a transferência de embriões mosaicos pode ser uma alternativa viável, desde que precedida por aconselhamento genético adequado e que não envolva mosaicos de cromossomos associados a síndromes viáveis ao nascimento caso se confirmasse a alteração no embrião, como os pares de cromossomos 13, 18, 21 e os cromossomos sexuais.
Cuidados e reflexões nas indicações da Biópsia Embrionária (o "Falso Positivo")
Apesar de seus benefícios, este exame também tem alguns problemas. O primeiro é o fato de poder apresentar resultado “falso positivo”, ou seja, indicar que o embrião é alterado, quando na verdade é normal, o que levaria ao descarte de um embrião saudável. Esta possibilidade de “falso positivo” ou “falso negativo” é possível e esperada neste tipo de exame. Em outras palavras, o exame PGT pode levar a um tratamento mais eficiente por minimizar as possibilidades de anomalias no bebê e aumentar a probabilidade de resultados positivos em cada transferência embrionária, pois a maioria dos embriões com anomalias não chega a implantar ou termina em aborto no início da gestação e é esperado que parte dos embriões formados na FIV sejam anormais (não saudáveis), sendo uma importante causa de falha de implantação na FIV. Por outro lado, um ensaio clínico realizado por Scott et al demonstrou que a possibilidade de “falsos positivos” podem ocorrer em até 4% dos casos e tornar o tratamento menos eficaz.
Se houver falso positivo e nenhum embrião com resultado normal, podemos descartar a única chance de a paciente engravidar. Alguns estudos demonstram que este número pode chegar até a 20% (Paulson), embora haja dúvidas sobre a real frequência de falsos positivos.
PGT-A Um castelo de areia
O dilema dos embriões aneuploides e mosaicos. A angústia de cada paciente – TRANSFERIR OU NÃO estes embriões?
A análise genética dos embriões (PGT-A) nos tratamentos de fertilização in vitro representa um avanço tecnológico que pode trazer benefícios a estas pacientes que se submetem a este procedimento. Os benefícios são a redução do tempo para alcançar a gestação, diminuição da necessidade de vários ciclos de FIV para atingir o sucesso do tratamento e o risco de abortos (questionável) e a possibilidade de gestações múltiplas pela transferência de um único embrião. Mas, por outro lado, muitas vezes os resultados negativos, mesmo quando possíveis e esperados, geram muita angústia aos pacientes, por frustrarem as suas expectativas.
Ter embriões com cromossomos alterados, o que chamo de uma condição genética inadequada para uma gestação saudável, pode significar para muitas mulheres e casais o fim da linha de um grande sonho. A dor atinge a alma. Um verdadeiro “castelo de areia” que desmoronou. Principalmente quando já passaram por vários tratamentos sem sucesso e já gastaram uma boa quantidade de dinheiro. E esta tem sido a angústia de médicos e pacientes do mundo.
O teste genético pré-implantacional para aneuploidia (que tem a sigla PGT-A) tem sido muito frequente nos tratamentos de fertilização, mas também tem se tornando cada vez mais controverso, desde que nascimentos de bebês “normais” (euploides) foram relatados e considerados, antes da transferência para o útero como “anormais” pelo teste genético realizado no laboratório especializado no exame. Ultimamente, tem sido crescente a transferência de embriões “anormais (aneuploides)” e o nascimento de bebês saudáveis, mas ainda não se sabe quantos centros de fertilização in vitro transferem embriões “anormais” e com que eficiência. Explico sempre nas consultas que a análise genética embrionária (PGT-A) não é infalível e existem erros. O resultado pode ser tanto falso-negativo quanto falso-positivo. Isto é, no laudo pode constar que o embrião é saudável (indicação genética ideal) mas, na verdade não é, mas também o resultado pode ser que embrião está alterado, não saudável (condição genética inadequada) e na verdade é 100% normal. E esta é a grande preocupação que leva à grande angústia das pacientes e minha também. DESCARTAR UM EMBRIÃO SAUDÁVEL.
Questiona-se ainda a possibilidade de o ato da biópsia causar danos ao embrião, conforme está escrito no “CONSENTIMENTO INFORMADO” do laboratório de genética que realiza a pesquisa das aneuploidias. Neste “CONSENTIMENTO”, que deve ser assinado pela paciente (ou pelo casal), está escrito: “É possível que a capacidade de implantação de um embrião biopsiado e com o resultado do PGT-A normal seja ligeiramente reduzida em comparação com um embrião normal que não tenha sido biopsiado”. É importante ler este “CONSENTIMENTO” sempre com atenção.
A grande discussão
Esta preocupação não é só minha, mas também de vários médicos do mundo.
Na minha peregrinação por vários congressos internacionais, sempre estou atento quando surge esta discussão, converso com especialistas que, como eu, questionam as indicações exageradas e indiscriminadas deste exame. Em conversa com Prof. Norbert Gleicher da Universidade de New York, em um determinado congresso (na verdade eu sempre estou presente nas suas palestras), ele comentou, preocupado como eu, que o número de bebês nascidos saudáveis nos Estados Unidos por tratamentos de FIV, diminuiu nos últimos dez anos, o que coincide com o aumento de número de embriões que realizaram biópsia para estudo genético. A conclusão é que muitos embriões saudáveis estão sendo “jogados fora” (descartados). Este dado é bem interessante.
Outro profissional, Professor Pasquale Patrizio, Diretor da Universidade de Yale, apresentou em outro Congresso uma estatística de transferência de embriões aneuploides (alterados) que levaram a uma taxa de nascimento de bebês saudáveis ao redor de 35%.
Estes três artigos que mostro a seguir demostram bem a realidade.
O primeiro artigo tem o título Nascidos vivos em todo o mundo após a transferência de embriões cromossomicamente “anormais” após PGT/A: resultados de uma pesquisa mundial baseada na web (Título original em inglês “Worldwide live births following the transfer of chromosomally “Abnormal” embryos after PGT/A: results of a worldwide web-based survey”).
Neste artigo é descrita uma pesquisa feita pela web, com critérios científicos, sobre os bebês nascidos vivos em todo o mundo em que foi realizada a transferência de embriões cromossomicamente “anormais” após PGT-A. Esta pesquisa foi realizada nos centros de fertilização in vitro para elucidar os padrões relacionados ao PGT-A, incluindo a transferência de embriões diagnosticados como “anormais” pelo PGT-A (condição genética inadequada). Os centros participantes foram dos Estados Unidos, Canadá, Europa, Ásia, América do Sul e África. Quarenta e nove virgula três (49,3%) ciclos resultaram em gestações em andamento ou nascidos vivos, e os abortos foram raros 9,3%. PASME!
Portanto, nesta publicação, as transferências de embriões “anormais” por PGT-A ofereceram chances robustas de gravidez e nascidos vivos com baixas taxas de aborto. Esses dados reforçam ainda mais o argumento de que este exame não pode determinar com segurança quais embriões devem ou não ser transferidos e leva ao descarte de muitos normais com excelente potencial de gravidez
O segundo artigo é Preimplantation genetic testing for aneuploidy versus morphology as selection criteria for single frozen-thawed embryo transfer in good-prognosis patients: a multicenter randomized clinical trial – Teste genético pré-implantação para aneuploidia versus morfologia como critério de seleção para transferência única de embriões congelados e descongelados em pacientes de bom prognóstico: um ensaio clínico randomizado multicêntrico.
Neste artigo é descrita uma pesquisa feita pela web, com critérios científicos, sobre os bebês nascidos vivos em todo o mundo em que foi realizada a transferência de embriões cromossomicamente “anormais” após PGT-A. Esta pesquisa foi realizada nos centros de fertilização in vitro para elucidar os padrões relacionados ao PGT-A, incluindo a transferência de embriões diagnosticados como “anormais” pelo PGT-A (condição genética inadequada). Os centros participantes foram dos Estados Unidos, Canadá, Europa, Ásia, América do Sul e África. Quarenta e nove virgula três (49,3%) ciclos resultaram em gestações em andamento ou nascidos vivos, e os abortos foram raros 9,3%. PASME!
Portanto, nesta publicação, as transferências de embriões “anormais” por PGT-A ofereceram chances robustas de gravidez e nascidos vivos com baixas taxas de aborto. Esses dados reforçam ainda mais o argumento de que este exame não pode determinar com segurança quais embriões devem ou não ser transferidos e leva ao descarte de muitos embriões normais com excelente potencial de gravidez
Este artigo mostra que a biópsia embrionária não causa uma diferença significativa nas taxas de sucesso de gravidez quando comparamos embriões submetidas à análise genética com embriões que não fizeram este exame. Portanto, a possibilidade de resultados com esses erros é muito mais comum do que se imagina. E isso é considerado por muitos profissionais da saúde como UM DESASTRE!
O terceiro artigo foi publicado na revista Sterility&Fertility com o título “Healthy euploid dizygotic twin birth after transfer of nonmosaic aneuploid embryos” traduzido para o português “Nascimento de gêmeos dizigóticos euploides saudáveis após a transferência de embriões aneuploides não mosaico” https://www.fertstert.org/article/S0015-0282(25)00538-2/abstract. Esta publicação mostra um caso em que dois embriões classificados como aneuploides foram transferidos após fertilização in vitro.
Apesar do diagnóstico genético inicial indicar alterações cromossômicas, ocorreu implantação e evolução da gestação. A gravidez resultou no nascimento de gêmeos dizigóticos saudáveis e cromossomicamente normais. Isso sugere que alguns resultados de biópsia embrionária podem não refletir perfeitamente todo o embrião.
Pode haver correção biológica ao longo do desenvolvimento ou diferença entre as células analisadas e o restante do embrião. Esta publicação mostra que a genética embrionária ainda possui limitações diagnósticas.
Qual a minha opinião
Quando a paciente ou o casal deseja realizar este exame genético, ou foi feita a análise em outro serviço e foi alterado, eu explico à paciente, verbalmente, estas questões, dou referências e um E-Book de minha autoria em conjunto com Dr. Rogerio Leão, “Biópsia Embrionária verdades e mitos” .
Falo sobre estas possiblidades. Tenho como indicação para este exame:
-
- Paciente acima de 40 anos (acho razoável acima de 38 anos);
- Pacientes, homens e mulheres, que tenham alterações cromossômicas no seu cariótipo;
- Abortos repetidos;
- Homens que tenham uma quantidade de espermatozoide muito baixa sem um diagnóstico que explique o motivo.
PGT-M: DETECÇÃO DE GENES ESPECÍFICOS
Apesar das principais alterações genéticas serem as anomalias cromossômicas, muitas doenças genéticas são causadas por um único par de gene. O PGT-A detecta as alterações cromossômicas mas não avalia alterações em genes. Para pesquisar um gene específico existe um outro exame: PGT-M (Teste Genético Pré-implantacional para doenças monogênicas. Neste caso, é necessária a biópsia embrionária, como no PGT-A mas o material coletado será submetido a outro tipo de análise onde se pesquisará se há mutação em um determinado gene.
Existem milhares de doenças monogênicas (causadas por um determinado gene) e estas são, felizmente, raras. Portanto, o PGT-M não é feito de rotina mas somente quando um casal tem história familiar de alguma doença relacionada a algum gene específico ou quando sabem que têm mutação em um gene que pode causar alguma doença hereditária nos filhos. Isso geralmente é descoberto por meio de um teste de compatibilidade genética feito antes do tratamento, o que será explicado à frente neste ebook.
Para realizar o PGT-M, previamente, é necessária uma análise genética do casal e familiares para que se possa criar uma “sonda genética” específica para aquela família. Realiza-se então a biópsia embrionária e é feita a pesquisa dos embriões que não tenham a doença genética. É possível, ainda, realizar o PGT-A simultaneamente. São inúmeras as doenças possíveis de serem diagnosticadas como fenilcetonúria, distrofia muscular, fibrose cística, entre outras que estão listadas mais à frente nesse ebook.
Hoje, o Conselho Federal de Medicina permite que esta técnica seja também utilizada para selecionar embriões compatíveis com outro filho do casal que tenha alguma doença que necessite de transplante ou células-tronco como tratamento.