Alteração genética causa riscos de envelhecimento prematuro dos ovários, menopausa precoce e possibilidade de filhos com retardo mental
Muitas mulheres só descobrem que têm uma diminuição precoce da função ovariana quando realizam dosagens hormonais para avaliar sua fertilidade. Aí descobrem que têm chances aumentadas de menopausa precoce e, além disso, algumas vezes, esse problema pode estar associado ao risco de ter filhos com problemas mentais.
Normalmente, na idade fértil da mulher, os ovários produzem óvulos e hormônios em níveis satisfatórios, que indicam uma provável ovulação normal e boa capacidade de gerar filhos, desde que não haja outros problemas que impeçam a gravidez. Essa rotina deve ocorrer até a idade próxima dos 40 anos. Se os hormônios FSH, LH, estrogênio e o hormônio Anti-Mulleriano, que de algum modo comprovam o funcionamento equilibrado das funções reprodutivas estão normais, indicam nessa fase uma Reserva Ovariana compatível com a idade da mulher. Apenas será observado o envelhecimento natural dos cromossomos com o tempo, diminuindo a chance de ter filhos ao longo dos anos.
Quando a insuficiência ovariana ocorre precocemente, antes dos 40 anos, chamamos de INSUFICIÊNCIA OVARIANA PREMATURA, ENVELHECIMENTO PRECOCE DOS OVÁRIOS ou, em situações extremas FALÊNCIA OVARIANA PREMATURA, esta última também chamada de MENOPAUSA PRECOCE. Nesses casos, mesmo nas mulheres que apresentam as menstruações normais, o ovário tem comportamento de envelhecimento antes da época esperada, assim, elas não ovulam adequadamente, têm dificuldade de engravidar, respondem pouco ou nada aos medicamentos que estimulam os ovários e têm níveis do hormônio FSH aumentados e do hormônio Anti-Mulleriano diminuído. Isso pode acontecer por vários motivos, mas entre todos o que mais preocupa é a alteração do gene FMR-1 (Fragile X Mental Retardation 1), situado no cromossomo X da mulher (lembrando que os cromossomos são 46XX para a mulher e 46XY para o homem). Esse cromossomo X tem uma aparencia “frágil” sob o microscópio, um fenômeno que deu à síndrome o nome X frágil.
O Gene FMR-1 é formado por uma sequência de três substâncias chamadas nucleotídeos que se repetem. Cada sequência é abreviada pela sigla CGG: C (citosina), G (guanina), G (guanina). Uma mulher normal deve ter até 30 repetições dessa sequência. Quando existe uma expansão (um aumento) do número de repetições da mesma, chegando a acima de 200, o gene FMR-1 fica inativo e não produz a proteína FMRP, que é necessária para o normal desenvolvimento neurológico, provocando uma doença grave que leva à deficiência mental. É a Síndrome do X-FRÁGIL ou Síndrome de Martin Bell, uma desordem genética considerada a causa mais frequente de retardo mental herdado. São indivíduos desabilitados intelectualmente e com várias alterações físicas (orelhas proeminentes, cara longa pelo excesso de maxilar vertical, palato arqueado e outras). Na população, apresenta uma incidência estimada de 1/4.000 em homens e de 1/4.000 a 1/8.000 em mulheres.
Repetições entre 30 e 200 não causam essa doença, mas provocam repercussões de gravidade variável. As mulheres são saudáveis, mas apresentam manifestações ocultas que só serão observadas quando houver sinais de insuficiência ovariana ou alterações hormonais detectadas quando solicitadas. São as situações Intermediária e Pré-mutação, que são avaliadas pelo exame de sangue chamado PCR para X Frágil, que determina o número de repetições no gene desta sequência.
O QUE NOS PREOCUPA?
As duas situações que merecem maior atenção são a Intermediária e a Pré-mutação, por causarem alterações clínicas, na maioria das vezes ocultas e pouco evidentes para um diagnóstico antecipado, e provocarem complicações futuras.
1. Intermediário ou zona cinzenta (45-54 CGG repetições):
• associada à Insuficiência ovariana Prematura (POI);
• ocorre em 1 a cada 35 mulheres;
• recentes estudos demonstraram que mesmo repetições entre 35 e 44 podem levar ao ENVELHECIMENTO PRECOCE DOS OVÁRIOS (Karimov-2011 e Gleycher-2009).
2. Pré-mutação (55-200CGG repetições):
• ocorre em 1 a cada 300 mulheres;
• tem maior chance de desenvolver insuficiência ovariana, diminuição da fecundidade e uma insuficiência ovariana oculta. Tem ciclos regulares, mas FSH aumentado, Hormônio Antiulleriano e Inibina B diminuídos;
• 20% dos casos têm Insuficiência ovariana evidente e menopausa antecipada em 5 anos.
Insuficiência ovariana oculta pode ser observada em mulheres entre 18 e 40 anos com FSH aumentado e Inibina B e AMH diminuídos. Cerca de 4 a 7,5% dessas pacientes apresentam a pré-mutação. Apesar de não ser tão frequente, é importante pesquisar o número de repetições no gene FMR1 nessas pacientes pelo risco de ter filhos com a síndrome. Pacientes portadoras da pré-mutação, ao formar seus gametas, podem ter expansão das repetições para mais de 200 repetições, e assim ter filhos com a mutação completa, risco que é maior quanto maior o número de repetições da mãe. Assim, se a mãe tiver mais de 90 repetições, a chance de expandir à mutação completa é maior que 90%, enquanto que de 59 a 79 repetições essa chance é de menos de 50%. Mulheres com repetições entre 45 e 70 têm somente 4 a 5% de chance de ter essa expansão para sua prole, mas ela pode acabar evoluindo para a mutação completa após duas a três gerações.
Frente a tudo isso, o American College of Medical Genetics, o American College of Obstetricians and Gynecologists, a European Society for Human Genetics e a European Society for Human Reproduction and Embryology (ESHRE) recomendam a pesquisa da premutação do gene FMR1 em pacientes com alteração da função ovariana, principalmente se houver história familiar de FOP, X-frágil ou retardo mental de origem desconhecida.
Entretanto, deve-se observar que embora a presença da pré-mutação aumente o risco da Falência Ovariana Prematura, essa alteração não determina obrigatoriamente que isso ocorrerá. Parece haver outros genes envolvidos na determinação da idade da menopausa. Ela serve de alerta para fazer a pesquisa de reserva ovariana precocemente, para não adiar demais a maternidade e evitar hábitos como o cigarro, que pode diminuir ainda mais a idade da menopausa. Além disso, aconselhamento genético é importante nesses casos, para avaliar os riscos de filhos com a doença.
Perguntas e Respostas:
1) O qué é Insuficiencia Ovariana Primária Associada ao Cromossomo X-Frágil (abreviado em inglês FXPOI)?
FXPOI é uma condição na qual os ovários não estão funcionando a plena capacidade em uma paciente portadora da pré-mutação FMR1. Os sintomas comuns da FXPOI incluem menstruações ausentes ou irregulares, sintomas da menopausa, como ondas de calor etc., menopausa precoce e infertilidade.
2) Qual a função dos ovários?
Os ovários fazem parte do sistema reprodutivo de uma mulher. Eles são como um “ninho” que contém todos os ovos, que são liberados para o útero a cada mês no meio do ciclo menstrual, quando poderá ser fertilizado. Se não for fertilizado, será eleminado no período menstrual.
Ovários também produzem e liberam hormônios que são importantes para a fertilidade e para a preparação e manutenção do endométrio. Com o passar dos anos, os ovários diminuem a sua função reprodutiva e produzem menos óvulos e pouco saudáveis para o desenvolvimento de um bebê. Os ovários em mulheres com FXPOI não funcionam a plena capacidade e podem assemelhar-se aos ovários de uma mulher mais velha, tanto no número quanto na qualidade dos ovos disponíveis.
3) Qual a difrença entre FXPOI e Menopausa Precoce?
As mulheres com FXPOI podem desenvolver sintomas semelhantes aos da menopausa, como ondas de calor e secura vaginal, mas a FXPOI difere da menopausa em alguns aspectos importantes.
Mulheres com FXPOI ainda podem engravidar em alguns casos porque seus ovários podem, ocasionalmente, liberar óvulos viáveis. Mulheres na menopausa não conseguem engravidar, porque seus ovários não produzem mais óvulos.
Mulheres com FXPOI podem voltar a ter menstruações, mas as mulheres na menopausa não terão mais períodos menstruais.
Portadoras pré-mutação FMR1 podem ter a função ovariana normal, ainda que possam ter em um futuro breve a menopausa precoce (ao redor dos 40 anos). A menopausa ocorre normalmente ao redor dos 50 anos.
4) O que é Falência Ovariana Prematura (sigla em inglês = POF) e como difere da FXPOI ?
POF significa “Falência Ovariana Prematura”, que é a completa cessação dos períodos menstruais antes da idade de 40. Os sintomas da FXPOI incluem POF, que é o estágio final da síndrome, além de outros sintomas de insuficiência ovariana, como ciclos irregulares, infertilidade, ondas de calor etc. Os sintomas da FXPOI podem ser mais amplos do que os sintomas da POF sozinha.
5) Como uma mulher pode saber se tem FXPOI ?
Por definição, todas as mulheres que têm FXPOI têm a pré-mutação FMR1. Se uma mulher tiver os sintomas da FXPOI, ela deverá recorrer ao seu médico para os exames hormonais e o teste genético para o FMR1.
Se for confirmada a pré-mutação, será importante que os familiares próximos tenham ciência para identificar outros portadores na familia que possam estar em risco de ter a FXPOI e suas consequências.
Todas as mulheres portadoras FMR1 devem manter um registro de seus ciclos menstruais e anotar padrões incomuns como ausência de menstruações, ciclos anormalmente longos (mais de 35 dias) ou ciclos curtos (menos de 21 dias). Além disso, devem estar atentas a outras alterações físicas, tais como ondas de calor, insônia, ressecamento vaginal e/ou diminuição da libido, aumento da ansiedade etc.
6) Qual a frequência da FXPOI na população em geral?
A FXPOI ocorre em cerca de 20-25% dos adultos do sexo feminino portadores de pré-mutação FMR1. Também tem sido relatada em adolescentes, embora seja menos comum nessa população.
7) As mulheres com uma pré-mutação FMR1 podem engravidar?
Muitas mulheres que são portadoras da FMR1 podem engravidar. No entanto, todas correm o risco de ter filhos com síndrome do X frágil e por isso devem consultar um especialista em medicina reprodutiva ou genética para discutir questões reprodutivas.
As mulheres que tiverem a fertilidade normal podem tentar engravidar naturalmente ou avaliar com um especialista as opções reprodutivas, como o Diagnóstico Genético Pré-implantacional, que avalia o embrião antes de ser transferido para o útero (PGD – CGH). Se a concepção for natural, a avaliação poderá ser feita no pré-natal pela amniocentese ou biópsia do vilo corial (BVC). Em algunas casos, poderá ser discutido outras opções da medicina reprodutiva, como incluindo fertilização in vitro com os próprios óvulos ou fertilização in vitro com óvulos doados.
8) Como uma paciente pode saber se é portadora da pré-mutação FMR1?
Qualquer médico especialista em reprodução humana ou geneticista pode solicitar o exame PCR para X- frágil.
A Sociedade Americana de Medicina Reprodutiva (ASRM) e o Colégio Americano de Obstetrícia e Ginecologia (ACOG) recomendam que todas as mulheres com insuficiência ovariana ou níveis elevados de FSH façam esse teste. Cerca de 2% (1/50) das mulheres com insuficiência ovariana são encontrados para ter uma pré-mutação FMR1, assim como cerca de 7% (15/01) das pacientes com uma história pessoal e familiar de insuficiência ovariana.
Contato: saude@ipgo.com.br
Tel. (11) 3885-4333
Após esta leitura, leia também:
1. Por que a fertilização in vitro pode falhar
2. “Amazenamento” de embriões
3. Os tratamentos de fertilização in vitro
4. Fertilização in vitro em mulheres maduras
5. Fertilização em mulheres com FSH elevado
6. Vitrificação
7. Tratamentos que podem melhorar a fertilidade da mulher e os resultados dos tratamentos de fertilização
8. Qual o custo?
9. Videos
10. Home
Referências Bibliográficas:
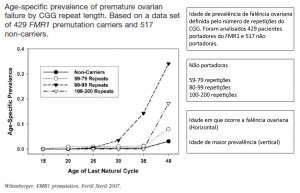
1- Wittenberger MD, Hagerman RJ, Sherman SL, McConkie-Rosell A, Welt CK, Rebar RW, Corrigan EC, Simpson JL, Nelson LM. The FMR1 premutation and reproduction. FertilSteril. 2007 Mar;87(3):456-65. Epub 2006 Oct.
2- Welt CK, Smith PC, Taylor AE. Evidence of early ovarian aging in fragile X premutation carriers. J ClinEndocrinolMetab 2004;89:4569–74.
3- Nolin SL, Brown WT, Glicksman A, Houck GE Jr, Gargano AD, Sullivan A, et al. Expansion of the fragile X CGG repeat in females with premutation or intermediate alleles. Am J Hum Genet 2003;72:454–64.
4- Hunter JE, Epstein MP, Tinker SW, Charen KH, Sherman SL. Fragile X-associated primary ovarian insufficiency: evidence for additional genetic contributions to severity. Genet Epidemiol. 2008 Sep;32(6):553-9.
5- Platteau P, Sermon K, Seneca S, Van Steirteghem A, Devroey P, Liebaers I. Preimplantation genetic diagnosis for fragile Xa syndrome: difficult but not impossible. Hum Reprod. 2002 Nov;17(11):2807-12.
6- Gleicher N, Weghofer A, Barad DH. A pilot study of premature ovarian senescence: I. Correlation of triple CGG repeats on the FMR1 gene to ovarian reserve parameters FSH and anti-Müllerian hormone. FertilSteril. 2009 May;91(5):1700-6. Epub 2008 Apr2.
7- Karimov CB, Moragianni VA, Cronister A, Srouji S, Petrozza J, Racowsky C, Ginsburg E, Thornton KL, Welt CK. Increased frequency of occult fragile X-associated primary ovarian insufficiency in infertile women with evidence of impaired ovarian function.HumReprod.2011 Aug;26(8):2077-83. Epub 2011 Jun6.
